
Акушерство для студентов / Запоражан том 1
.pdf
Розділ 15. Плодові ускладнення...
Маловоддя
Маловоддя за відсутності розриву плодових оболонок асоціюється з 40 разовим зростанням перинатальної смертності. До певної міри ця обставина пов’язана з тим, що редукція об’єму амніотичної рідини зменшує захист пупкового канатика плода і він стає більш сприйнятливим до компресії, що призводить до почастішання випадків асфіксії плода. Маловоддя також нерідко асоційовано з природженими аномаліями розвитку плода, особливо урогенітальної системи, і ЗВУР плода. Маловоддя з ІІ три местру гестації призводить до розвитку гіпоплазії легенів плода. При оцінці стану пло да нерідко виявляють нереактивний нестресовий тест, а під час пологів маловоддя асоціюється з такими ускладненнями, як несприятливі децелерації серцевого ритму плода, виділення меконія. Отже, через гіпоксію плода зростає частота кесаревого роз тину.
Етіологія. Маловоддя може бути спричинене як зменшенням продукції амніотич ної рідини, так і її збільшеною втратою. Амніотична рідина продукується переважно нирками і легенями плода. Резорбція амніотичної рідини відбуваєтся в плаценті; крім того, плід ковтає амніотичну рідину. В деяких випадках (при передчасному розриві плодових оболонок) амніотична рідина витікає через піхву. При недостатності мат ково плацентарного кровотоку (плацентарній недостатності) розвиток маловоддя пов’язаний з тим, що плід не має достатнього об’єму циркулюючої крові або достат нього живлення для підтримки ниркового кровотоку й адекватної клубочкової фільтрації. Недостатність матково плацентарного кровотоку (плацентарна недо статність) часто асоціюється з затримкою внутрішньоутробного розвитку та гіпок сією плода. Гіпоксія плода, в свою чергу, призводить до редукції об’єму плазми і змен шення синтезу гормону росту.
Природжені аномалії урогенітальної системи плода можуть призводити до змен шення вироблення сечі. Ці вади можуть бути представлені агенезією нирок (синд ром Поттера), полікістозом нирок або обструкцією урогенітального тракту.
Але найбільш частою причиною маловоддя є передчасний розрив плодових обо лонок. Навіть за відсутності скарг щодо витікання рідини з піхви, у кожної пацієнт ки з маловоддям слід виключити можливість передчасного розриву плодових оболо нок.
Діагностика. Діагноз маловоддя можна запідозрити при зменшенні окружності живота і висоти дна матки відповідно до гестаціного віку, але він повинен бути підтвердженим при ультразвуковому дослідженні (АФІ < 5 см). З’ясовують наявність симптомів передчасного розриву плодових оболонок, особливу увагу приділяють ви значенню точного гестаційного віку і стану плода (затримка внутрішньоутробного росту, переношеність). Отже, при визначенні діагнозу маловоддя подальшим кроком буде з’ясування його причини для здійснення адекватних лікувальних заходів.
Причини маловоддя
Хромосомні аберації Природжені вади розвитку плода
Хронічна гіпоксія плода Переношена вагітність Дегідратація матері Розрив плодових оболонок
Трансфузійний синдром близнят
359

Акушерство і гінекологія. Том 1
Лікування. Ведення і лікування пацієнток з маловоддям має пряму залежність від його причини. Якщо маловоддя асоціюється зі ЗВУР плода, основну увагу приділя ють об’єктивній оцінці стану плода (причина ЗВУР, точний гестаційний вік, біофі зичний профіль, кольорове допплерівське картування кровотоку). Індукцію пологів звичайно виконують у випадку, якщо плід доношений або переношений. При вияв ленні природжених аномалій розвитку плода пацієнтки повинні бути консультовані генетиком. У цьому разі спосіб і термін розродження обговорюється разом з неона тологами і дитячими хірургами. При глибокій недоношеності та нез’ясованій причині маловоддя звичайно обирається вичікувальна тактика з частим повторенням тестів антенатальної діагностики.
При розриві плодових оболонок у терміні доношеної вагітності та відсутності по логової діяльності проводиться індукція пологів. При наявності меконія в навколо плідних водах або при несприятливих децелераціях ЧСС плода рекомендується ам ніоінфузія (введення фізіологічного розчину в амніотичну порожнину за допомогою спеціального катетера). Амніоінфузія сприяє зменшенню концентрації амніотичної рідини і теоретично зменшує частоту несприятливих варіабельних децелерацій, по в’язаних з компресією пупкового канатика. Ведення пацієнток з передчасним розри вом плодових оболонок представлено у відповідному розділі підручника.
Багатоводдя
Багатоводдя — це збільшення об’єму амніотичної рідини (ІАР > 20–25). Частота багатоводдя становить 2–3 % усіх вагітностей.
Етіологія. Багатоводдя асоціюється з більшим ризиком аномалій кількості і струк тури хромосом; природжених вад розвитку плода (аненцефалія, інші дефекти нерво вої трубки, первинні нейром’язові захворювання, обструкція шлунково кишкового тракту (атрезія стравоходу і дванадцятипалої кишки), неімунна водянка плода); цук ровим діабетом матері та багатоплідною вагітністю. При обструкції шлунково киш кового тракту плід зменшує або втрачає можливість заковтувати амніотичну рідину, що призводить до багатоводдя. Багатоводдя також пов’язують із ризиком вад клапанів серця, діафрагмальної грижі, аритмій.
Але близько 2/3 випадків багатоводдя залишаються ідіопатичними, хоча вважа ють, що «ідіопатичне» багатоводдя поєднується з ризиком хромосомної анеуплоїдії.
У пацієнток, які хворіють на цукровий діабет, підвищений рівень глюкози в крові може виступати в ролі осмотичного діуретика для плода і спричинювати розвиток багатоводдя. Неімунна водянка плода внаслідок порушення серцевого викиду також може спричинювати багатоводдя. При монозиготних двійнятах у разі розвитку транс фузійного синдрому близнюків один плід може мати багатоводдя, а другий — мало воддя.
Причини багатоводдя
Анеуплоїдія хромосом Природжені аномалії
Цукровий діабет у матері (гестаційний або прегестаційний) Трансфузійний синдром близнят Водянка плода (імунна і неімунна)
Ідіопатичні
360

Розділ 15. Плодові ускладнення...
Діагностика. Діагноз багатоводдя звичайно запідозрюється при зовнішньому аку шерському обстеженні (збільшення окружності живота, висоти дна матки) і підтвер джується при ультразвуковому обстеженні, нерідко під час скринінгу пацієнток із ге стаційним діабетом, багатоплідною вагітністю, а також підозрою на велику масу пло да, що не відповідає гестаційному віку.
Ведення пацієнток. Як і при маловодді, діагноз багатоводдя потребує детальної оцінки перебігу вагітності. Багатоводдя є фактором ризику передчасних пологів і пе редчасного розриву плодових оболонок внаслідок перерозтягнення матки і значного збільшення маткового об’єму. Пацієнтки з багатоводдям також мають збільшений ризик аномального передлежання плода, що повинно бути встановлено до початку пологів. У пологах зростає ризик випадіння пупкового канатика, тому амніотомію слід виконувати лише при щільно вставленій в таз голівці плода. Під час амніотомії слід повільно випускати навколоплідні води з метою профілактики передчасного відшарування плаценти. При спонтанному розриві плодових оболонок слід провес ти вагінальне дослідження для уточнення передлежання плода і виключення діагнозу випадіння пупкового канатика.
РезусHконфліктна вагітність
і резусHімунізація (алоімунізація)
Якщо мати є резус негативною (Rh негативною), а плід є резус позитивним (Rh позитивним), вона може бути сенсибілізована до Rh антигену і утворювати антире зусні антитіла. Ці антитіла проходять через плаценту і спричинюють гемоліз ерит роцитів плода. Частота резус негативного типу крові залежить від раси, коливаєть ся від 1 (азіати і корінні американці) до 15 % у кавказців і може досягати 30 % (в іспанок). Більшість Rh негативних жінок сенсибілізуються під час вагітності або пе реливання крові. Антигени системи Rh визначаються в крові плода вже з 9–19 го тижнів вагітності, а системи АВ0 — з 5–6 го тижня, отже, можлива рання сенсибілі зація організму матері при попередніх вагітностях.
Зменшення частоти резус імунізації у США було досягнуто за рахунок покращан ня роботи служби переливання крові, а також профілактичного введення антирезус ного імуноглобуліну при вагітності. Цікавим є той факт, що внаслідок деякого транс плацентарного переходу клітин плода при будь якій вагітності несумісність матері та плода за системою АВ0 має протективний ефект щодо резус сенсибілізації завдя ки деструкції плодових клітин анти А і анти В антитілами.
У Rh негативних жінок, сенсибілізованих Rh позитивним плодом, антитіла про ходять через плаценту і спричинюють катастрофічні ускладнення для плода — гемо! літичну хворобу плода і новонародженого, яка може бути представлена анемією, жов! тяницею і водянкою. Анемія плода, що розвивається внаслідок гемолізу його еритро цитів (гемолітична анемія), призводить до екстрамедулярної продукції еритроцитів плода. Водянка плода (erythroblastosis fetalis) — є найтяжчою формою гемолітичної хвороби, небезпечним синдромом, який супроводжується тяжкою анемією, гіперди намічним станом, ураженням серця, перикардитом, гепатоспленомегалією, дифузним набряком та асцитом плода. Кінцевим продуктом розпаду еритроцитів є білірубін, який частково утилізується плацентою до пологів, але при високій концентрації може спричинювати жовтяницю та нейротоксичні ефекти у новонароджених.
361

Акушерство і гінекологія. Том 1
Несенсибілізовані RhHнегативні вагітні
Якщо вагітна є Rh негативною, але не має антирезусних антитіл (несенсибілізо вана) метою ведення вагітності є підтримання її у несенсибілізованому стані. Титр антирезусних антитіл (проба Кумбса) визначають при першому антенатальному візиті вагітної до лікаря (8–10 тиж) і повторюють щомісяця до 32 тиж, з 32 го до 35 го тижнів — 1 раз на 2 тиж; після 35 го тижня — щотижнево. Протягом вагітності паці єнтка має значний ризик бути сенсибілізованою (при проведенні амніоцентезу, ми мовільному аборті, позаматковій вагітності, вагінальній кровотечі, передчасному відшаруванні плаценти, в пологах). У всіх цих випадках вводять антирезусний гам маглобулін (анти D імуноглобулін, анти Rh IgD). Крім того, анти Rh IgD вводять у терміні 28 тиж вагітності і відразу після пологів, якщо дитина є резус позитивною.
Стандартна доза антирезусного гамма глобуліну становить 0,3 мг, яка нейтралі зує 15 мл еритроцитів плода (30 мл крові плода з гематокритом 50). Ця доза звичай но є адекватною для одноплідної вагітності. Але у разі відшарування плаценти чи інших допологових кровотеч, доцільним є виконання тесту Кляйгауера — Бетке (Kleihauer — Betke) для визначення кількості плодових еритроцитів у материнсько му кровотоку. Якщо кількість плодових еритроцитів у крові матері є більшою, ніж може нейтралізувати стандартна доза антирезусного гаммаглобуліну, додатково при значають 1–2 дози анти Rh IgD.
Сенсибілізовані RhHнегативні вагітні
При виявленні антирезусних антитіл у вагітної при першому пренатальному візиті, виконують їх ретельний скринінг, визначають тип крові батька дитини. Якщо бать ко є Rh негативним, небезпеки для плода немає. Якщо батько є резус позитивним, бажано дослідження його гомозиготності або гетерозиготності за D генним локусом. Зростання титру антирезусних антитіл до 1:16 і вище асоціюється з водянкою пло да. Титр антирезусних антитіл визначають не рідше, ніж через кожні 4 тиж. Якщо титр антитіл є меншим 1:16, продовжують спостереження за вагітною і станом пло да.
Антенатальна діагностика стану плода полягає у проведенні ультразвукових до сліджень, біофізичного профілю, нестресового тесту, допплерометрії кровотоку в ар теріях плода. При тяжкій формі гемолітичної хвороби (водянка плода) при ультра звуковому дослідженні можуть бути виявлені багатоводдя, подвійний контур голів ки плода (набряк м’яких тканин), асцит у плода, кардіомегалію, вилив у перикарді, гепатоспленомегалію, розширення пупкової вени.
Синусоїдальний ритм ЧСС плода протягом нестресового тесту може свідчити про тяжку анемію.
Прогностичну цінність має дослідження швидкості кровотоку в середній мозковій артерії плода методом допплерометрії: швидкість систолічного кровотоку зростає при тяжкій анемії плода.
При зростанні титру антирезусних антитіл до 1:16 і вище показано проведення серії амніоцентезів через 1–3 тиж, починаючи з 16–20 го тижнів гестації. При пер шому амніоцентезі оцінюють групу і резус крові плода. Якщо плід є резус негатив ним, продовжують спостереження за вагітною. Якщо плід є резус позитивним, про водять серію амніоцентезів для аналізу оптичної щільності амніотичної рідини, яка свідчить про рівень білірубіну у навколоплідних водах. Білірубін накопичується в
362

Розділ 15. Плодові ускладнення...
амніотичній рідині при зростанні гемолізу плодових еритроцитів. При спектрофото метрії навколоплідних вод присутність білірубіну спричинює девіацію стандартної кривої при довжині хвилі близько 450 нм, що визначається як ∆ OD450. Оцінку ри зику для плода проводять за допомогою кривої Лілі (Liley), яка поділяється на 3 зони (рис. 15.1).
Показник ∆ OD450, що знаходиться в зоні І, свідчить про незначне ураження плода і контрольні подальші амніоцентези виконують кожні 2–3 тиж. Присутність ∆ OD450 у зоні 2 свідчить про помірний ризик ураження плода, й амніоцентез повторюють кожні 1–2 тиж. ∆ OD450 у зоні 3 свідчить про анемію плода і необхідність виконан ня кордоцентезу шляхом транскутарної пункції пупкової вени для визначення гема токриту плода і виконання внутрішньоматкової гемотрансфузії (замінного перели вання крові плода). Замінне переливання крові плода проводять при дефіциті пло дового гемоглобіну > 20 г/л (відмиті еритроцити групи 0 (І), Rh позитивні). Якщо кордоцентез і внутрішньоматкове переливання крові не можуть бути виконані, мож ливе здійснення інтраперитонеальної гемотрансфузії плода.
Інші причини гемолітичної хвороби (імунної водянки) плода
Існує значна кількість інших антигенів системи крові, включаючи систему АВ0, антигени C, D, E, в якій D — це резусний (Rh) антиген, системи Kell, Duffy, Lewis та ін. Деякі з цих антигенних систем можуть спричинювати гемолітичну хворобу пло да (Kell, Duffy), інші — тяжкий гемоліз, але не тяжку імунну водянку плода (AB0, Lewis). При імунізації за системою Kell критичний титр антитіл становить 1:8. За умо ви профілактичного застосування антирезусного імуноглобуліну частота резус іму нізації зменшується і частіше спостерігаються інші причини гемолітичної хвороби плода. Ведення вагітності в таких випадках є аналогічним такому у резус негатив них пацієнток (серійне дослідження титру антитіл, амніоцентез, кордоцентез і замі нне переливання крові за наявності показань).
Гемолітична хвороба новонародженого
За відсутності лікування гемолітичної хвороби плода після народження дитини розвивається гемолітична хвороба новонародженого, яка може бути представлена ге молітичною анемією, жовтяницею (з гемолітичною анемією) і водянкою (з гемолі тичною анемією та жовтяницею).
Гемолітична анемія новонародженого виявляється протягом 2–3 тиж життя і швидко прогресує внаслідок пригнічення гемопластичної функції кісткового мозку. Кількість еритроцитів плода зменшується до 2× 1012 в 1 л, гемоглобіну — до 60–80 г/л, рівень білірубіну підвищується. Анемія є нормо або гіпохромною і мікроцитарною; ретикулоцитоз відсутній.
Жовтяниця новонародженого є найбільш частою, особливо при несумісності крові матері та плода за системою АВ0. Спостерігається підвищення рівня білірубіну, по мірна анемія. При швидкому зростанні рівня білірубіну може розвиватись ядерна жов тяниця або білірубінова енцефалопатія, яка характеризується ураженням централь ної нервової системи (базальних гангліїв), порушенням процесів тканинного дихан ня. У новонароджених з ядерною жовтяницею розвиваються спастичні синдроми, м’я зова дискоординація, розлади дихання, судоми, гіпертермія і смерть внаслідок кро вовиливів у життєво важливі органи (за відсутності термінового лікування — замін
363

Акушерство і гінекологія. Том 1
ного переливання крові). Віддалені наслідки ядерної жовтяниці можуть проявляти ся органічними ураженнями ЦНС і тяжкими порушеннями інтелектуального розвит ку дитини.
Водянка — найтяжча форма гемолітичної хвороби, яка частіше призводить до внутрішньоутробної смерті плода. При народженні дитина має бліді шкірні покри ви, загальний набряк, асцит, гепатоспленомегалію, тяжку анемію. Вміст еритроцитів у крові не перевищує 1,5× 1012 в 1 л, вміст гемоглобіну < 80 г/л, наявне збільшення вмісту фетальних еритроцитів (еритробластоз плода).
Лікування гемолітичної хвороби новонародженого полягає у негайному замінному переливанні крові для зменшення і стабілізації рівня білірубіну та профілактики білірубінової енцефалопатії.
Показаннями до замінного переливання крові є позитивна пряма проба Кумбса (наявність фіксованих еритроцитами новонародженого антирезусних антитіл), вміст Hb < 90 г/л, білірубіну вище 342 мкмоль/л, швидкість зростання рівня білірубіну > 6 мкмоль/год, рівень білірубіну в пупкових судинах > 60 мкмоль/л.
Кров донора тимчасово виконує звичайну функцію крові, власне кровотворення дитини спочатку пригнічується. В тяжких випадках використовують Rh негативну кров. При несумісності за системою АВ0 вводять кров групи 0(І), що збігається з кро в’ю дитини за резус фактором. Об’єм крові, яку вливають, вираховують залежно від гестаційного віку, маси новонародженого, вмісту Hb і Ht (звичайно 150–160 мл на 1 кг маси тіла). В середньому під час замінного переливання крові вводиться 500 мл крові донора і виводиться 450–500 мл крові дитини. У разі необхідності (зростання рівня білірубіну) проводять повторні замінні переливання крові.
|
|
|
|
|
|
Профілактика гемолітичної хвороби |
|
|
|
|
|
|
плода і новонародженого полягає у недо |
|
|
|
|
|
|
пущенні Rh сенcибілізації, профілактич |
|
|
|
|
|
|
ному введенні анти Rh–IgD при всіх ста |
|
|
|
|
|
|
|
|
|
|
|
|
|
нах, які можуть спричинювати імунізацію |
|
|
|
|
|
|
матері (аборти, позаматкова вагітність, |
|
|
3 |
|
|
|
пологи, амніоцентез тощо), недопущенні |
|
|
в |
|
переливання Rh несумісної крові. |
||
|
|
|
|
|||
|
|
|
|
|
||
450 нм |
|
|
|
|
|
Антенатальна |
|
|
|
|
|
||
при |
|
2 |
|
|
|
(внутрішньоутробна) |
|
|
|
|
|
||
∆ ОД |
|
|
|
|
смерть плода |
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
б |
|
|
Антенатальна смерть плода (АСП) є |
|
|
|
|
|
|
|
|
|
|
|
|
|
рідкісним (1:1000 народжень) явищем. |
|
|
1 |
|
|
|
Частота антенатальної смерті плода зро |
|
|
|
|
|
стає при материнських захворюваннях і |
|
|
|
|
а |
|
|
|
|
|
|
|
|
ускладненнях вагітності, включаючи пе |
|
|
|
|
|
|
|
редчасне відшарування плаценти, приро |
|
|
|
|
|
|
джені вади розвитку плода, переношу |
|
26 28 30 32 34 36 38 40 |
вання вагітності. Хронічна плацентарна |
||||
|
|
тижні вагітності |
недостатність, яка розвивається вторин |
|||
|
Рис. 15.1. Крива Лілі для оцінки ризику ге |
но, внаслідок системних колагенових, су |
||||
молітичної хвороби плода: а — низький ризик |
динних або гіпертензивних хвороб, може |
|||||
ГХП; б — помірний ризик ГХП; в — високий |
призвести до ЗВУР і подальшої антена |
|||||
ризик ГХП; 1 — зона ; 2 — зона 2; 3 — зона 3 |
тальної смерті плода. Якщо точну причи |
|||||
364

Розділ 15. Плодові ускладнення...
ну антенатальної смерті встановити неможливо, її звичайно вважають пов’язаною з патологію пупкового канатика. Затримка мертвого плода в матці протягом 3–4 тиж призводить до вторинної гіпофібриногенемії (коагулопатії споживання) внаслідок ви ділення тромбопластичних субстанцій з тканин плода. В деяких випадках розвиваєть ся синдром дисемінованої внутрішньосудинної коагуляції крові або її дисемінованого внутрішньосудинного згортання (ДВЗ синдром).
Діагностика. В І половині вагітності внутрішньоутробну смерть плода (missed abortion) можна запідозрити при відсутності темпів росту матки, зникненні ознак і симптомів вагітності. Діагноз підтверджується при ультразвуковому дослідженні та визначенні рівня ХГЛ. Після 20 тиж гестації про смерть плода може свідчити зник нення його рухів, відсутність збільшення висоти дна матки, що уточнюється під час ультразвукової діагностики.
Ведення пацієнток і розродження. У разі внутрішньоутробної смерті плода важ ливою є психологічна підтримка вагітної. Враховуючи ризик розвитку ДВЗ синдро му при антенатальній смерті плода, оптимальним веденням таких пацієнток буде за вершення вагітності (розродження) в оптимально короткі терміни. До 20 тиж гестації виконують штучне переривання вагітності, після 20 тиж — індукцію пологів шляхом застосування простагландинів або високих доз окситоцину. Дослідження причини внутрішньоутробної смерті плода включають тести на наявність колагенових судин них захворювань, антифосфоліпідного синдрому, гіперкоагуляційного стану, визна чення каріотипу плода, титру антитіл до TORCH інфекцій (токсоплазмозу, красну хи, цитомегаловірусу, герпесу та ін). Важливим є одержання даних аутопсії плода, що може визначити етіологію АСП. Але в 90 % випадків причина внутрішньоутроб ної смерті плода залишається невідомою.
Переношена вагітність
Переношена вагітність — це вагітність, яка триває більше 42 тиж гестаційного віку або більше 294 днів, рахуючи з першого дня останньої менструації. Частота перено шеної вагітності коливається від 3 до 10 % випадків. Переношена вагітність зали шається складною акушерською проблемою, тому що супроводжується зростанням ризику макросомії плода, маловоддя, аспірації меконія, антенатальної смерті плода і синдрому перезрілості новонародженого. Ризик для матері при переношеній вагіт ності зростає у зв’язку з майже дворазовим збільшенням частоти кесаревого розтину та макросомії плода. Численні дослідження свідчать про суттєве зростання цих ус кладнень при збільшенні терміну вагітності понад 40–41 тиж.
Етіологія. Найбільш частою причиною переношування вагітності є неправильне визначення гестаційного віку плода; отже, визначення точного гестаційного віку є ключовим моментом у діагностиці переношеної вагітності. У зв’язку з тим, що фізіо логічні основи початку пологової діяльності точно не встановлені, механізм перено шування вагітності також залишається невідомим. Більшість дослідників вважають, що зменшення рівня естрогенів сприяє переношуванню вагітності. Визначені деякі стани плода, які асоціюються з переношуванням вагітності, а саме: аненцефалія, гіпоплазія надниркових залоз, відсутність гіпофіза у плода.
Діагностика. Як уже зазначалося, діагностика переношеної вагітності базується на точному визначенні гестаційного віку плода. Помилка у визначенні гестаційного віку при ультразвуковому дослідженні в кінці вагітності може становити 3 тиж. Отже, діаг
365

Акушерство і гінекологія. Том 1
ноз підтверджують встановленням точної дати першого дня останньої менструації, дати запліднення, даних гінекологічного обстеження (розміри матки) та ультразву кової діагностики в І триместрі вагітності. При невизначеній даті останньої менст руації або наявності даних ультразвукового дослідження тільки у ІІ триместрі вагіт ності діагноз є непевним.
Ведення вагітності і пологів. Тактика ведення вагітності при підозрі на перено шування полягає у збільшенні частоти антенатальних візитів або госпіталізації, ан тенатальній оцінці стану плода шляхом частого проведення нестресового і стресо вих тестів, оцінки біофізичного профілю або об’єму амніотичної рідини, підготовці до індукції пологів. Алгоритм дій лікаря при переношеній вагітності такий:
1.Після закінчення 40 тиж гестації вагітній призначають нестресовий тест (НСТ); при непевному стані плода проводять індукцію пологів.
2.Протягом 41 го тижня досліджують біофізичний профіль плода (БПП) з подаль шим контролем НСТ, або модифікований біофізичний профіль плода, який включає НСТ і визначення об’єму амніотичної рідини. При непевному стані плода або зрілості шийки матки (за шкалою Бішопа > 6 балів) виконують індукцію пологів.
3.На 42 му тижні гестації незалежно від стану шийки матки проводиться індук ція пологів.
Багатоплідна вагітність
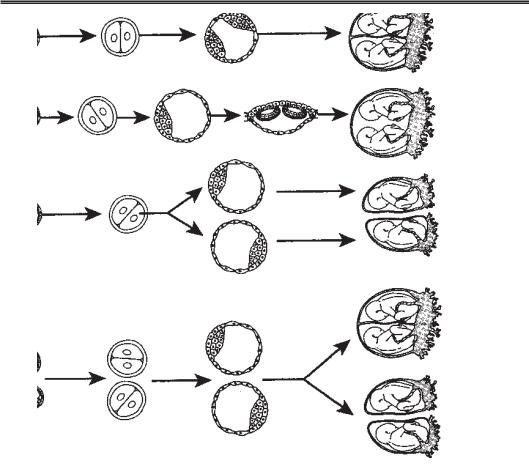
Якщо запліднена яйцеклітина розділяється на дві подільні клітини, утворюються
монозиготні, або однояйцеві, ідентичні близнята. Якщо під час овуляції звільнюють ся дві яйцеклітини і обидві запліднюються, утворюються дизиготні, споріднені близ! нята (рис. 15.2).
Суперфекундація — запліднення двох яйцеклітин в одному менструальному циклі двома сперматозоїдами (протягом двох роздільних статевих актів).
Суперфетація — дві яйцеклітини запліднюються протягом різних менструальних циклів, тобто друга овуляція настає після настання першої вагітності, такі факти є рідкісними.
Без допоміжних репродуктивних технологій частота багатоплідної вагітності в популяції дорівнює близько 1:80–1:100 вагітностей, причому 30 % із них є монози готними. Природна частота трійнят значно менша (1:7000–1:8000 вагітностей). По чинаючи з 1990 р., прогрес новітніх репродуктивних технологій (стимуляція овуляції та суперовуляції, фертилізація in vitro) сприяє зростанню частоти багатоплідної ва гітності. Так, застосування кломіфену збільшує ризик багатоплідної вагітності до 7– 13 %, індукція суперовуляції — до 25–30 % і застосування хоріонічного гонадотро піну — до 16–40 %.
Ускладнення багатоплідної вагітності. Багатоплідна вагітність супроводжується значною кількістю різноманітних акушерських ускладнень, включаючи передчасні пологи, передлежання плаценти, випадіння пупкового канатика, післяпологові кро вотечі, неповноцінність шийки матки (істміко цервікальну недостатність), гестацій ний діабет і прееклампсію. Плід підлягає значному ризику недоношеності, приро джених аномалій розвитку, низької маси тіла при народженні, ЗВУР та аномалій пе редлежання.
Народження двійнят звичайно відбувається в терміні 36–37 тиж, трійнят — 33– 34 тиж (з кожним подальшим плодом тривалість вагітності зменшується на 3 тиж). Монохоріальні діамніотичні близнята часто мають плацентарні судинні анастомози,
366
Розділ 15. Плодові ускладнення...
а
б
в
г
д
Рис. 15.2. Варіанти розвитку близнят:
а — найпоширеніший тип розвитку монозиготних близнят з поділом внутріш ньої маси бластоцисти (2 амніони, 1 хоріон, 1 плацента);
б — рідкісний тип розвитку монозиготних близнят з повним поділом зарод кового диска (1 амніон, 1 хоріон, 1 плацента);
в — монозиготні близнята з поділом, який виникає між стадією двох клітин і морулою з утворенням ідентичних бластоцист (2 амніони, 2 хоріони, 2 плаценти);
г — дизиготні близнята зі злитою плацентою; д — дизиготні близнята з 2 плацентами
що призводить до розвитку у них трансфузійного синдрому близнят (рис. 15.3). Мо нохоріальні моноамніотичні близнята мають надзвичайно високу перинатальну смертність (40–60 %), зокрема внаслідок патології пупкового канатика (заплутуван ня).
Трапляються випадки багатоплідної вагітності, що діагностується в І триместрі, які закінчуються народженням одного плода. Один із близнюків може загинути у пер шому триместрі або на початку другого триместру (резорбція, або «зникнення» близ нюка), або один з близнюків муміфікується і утворюється так званий «паперовий плід» (fetus papyraceus) (рис. 15.4).
367

Акушерство і гінекологія. Том 1
Патогенез. Монозиготні близнюки утворюються внаслідок розділення заплідне ної яйцеклітини або клітин ембріонального диска. Якщо розділення відбувається до диференціації трофобласта, утворюються два хоріони і два амніони (дихоріальні та діамніотичні, ди ді близнята). Після диференціації трофобласта, але до утворення ам ніона (3–8 й день ембріонального розвитку) розділення веде до розвитку однієї пла центи і двох амніонів. Розділення після утворення амніона (8–13 й день ембріональ ного розвитку) веде до розвитку однієї плаценти, одного хоріона і одного амніона. Розділення після 13 го і до 15 го дня є рідкісним і вже буде неповним, що може при звести до утворення зрощених, або «сіамських» близнят (1:60 000 пологів). При роз діленні після 15–16 го дня утворюється один плід.
Фактором ризику утворення монозиготних близнят признаний лише старший вік матері. Жінки, які народили двозиготних близнят, мають двократний ризик повто рення багатоплідної вагітності. Допоміжні репродуктивні технології сприяють збільшенню частоти як дизиготних, так і монозиготних двійнят до 25–30 %, трійнят
— до 5 %, вагітності з більшою кількістю плодів — до 0,5–1 %.
Дизиготні близнята утворюються внаслідок фертилізації двох яйцеклітин двома сперматозоїдами. Факторами ризику дизиготних близнят є наявність близнят у сімей ному анамнезі, африканська раса. Так, частота дизиготних близнят коливається від 1:1000 в Японії до 1:20 — у Нігерії.
Діагностика. Багатоплідну вагітність можна запідозрити при збільшенні темпів зростання матки, надмірному збільшенні маси тіла вагітної, пальпації трьох або більше великих частин плода при зовнішньому акушерському обстеженні (прийоми Лео польда). Діагноз звичайно підтверджується при ультразвуковому дослідженні. Рівень ХГЛ, альфа фетопротеїну (АФП) і плацентарного лактогену є більшим для гестацій ного віку. Інколи діагноз може бути визначений після народження І плода.
Ведення вагітності та пологів. Враховуючи значну кількість ускладнень, багато плідна вагітність вважається станом високого ризику в акушерстві і потребує уваж ного ведення пацієнтки акушером гінекологом, перинатологом і неонатологом. Крім антенатального догляду і профілактики ускладнень вагітності, найважливіше значен ня при багатоплідній вагітності мають спосіб і термін розродження.
Ведення вагітних починається з ультразвукової верифікації діагнозу, визначення кон кордантності (рівномірності) розвитку близнят, об’єму амніотичної рідини. Дискордан тний розвиток діагностується при відставанні розвитку І плода > 20 % (див. рис. 15.3). У ІІІ триместрі гестації проводять серійні ультразвукові дослідження, біофізичний профіль і нестресовий тест. Пацієнтки підраховують щоденну кількість рухів плодів. Зменшення кількості рухів може свідчити про маловоддя одного з плодів. При ознаках водянки плода виконують кесарів розтин. При багатоводді може бути використаний ліку вальний амніоцентез (амніоредукція) для зменшення розтягнення матки. При амніоцен тезі слід повільно випускати навколоплідні води для запобігання передчасному відша руванню плаценти. Вагітність пролонгують до 34 тиж, термін 24–32 тиж є найбільш кри тичним. Монозиготні двійнята мають високий ризик антенатальної смерті внаслідок пе рекручування пуповини, тому такі вагітні потребують особливо ретельного нагляду. Па цієнток госпіталізують і проводять постійний електронний моніторинг ЧСС плодів з 28 го до 34 го тижнів гестації, в 34 тиж виконують кесарів розтин.
Отже, алгоритм пренатального ведення багатоплідної вагітності включає такі най важливіші кроки:
1)рання діагностика сприяє кращим перинатальним результатам;
2)часті антенатальні візити (кожні 1–2 тиж після 26–30 тиж гестації); переваж но ліжковий режим;
3)додаткове вживання 300 ккал/день та 80 г/день білка, 60–100 мг/день заліза, 1 мг/день фолієвої кислоти;
368
