
Карцев В.Г. - Избранные методы синтеза и модификации гетероциклов. Том 1 (2003)(ru)
.pdf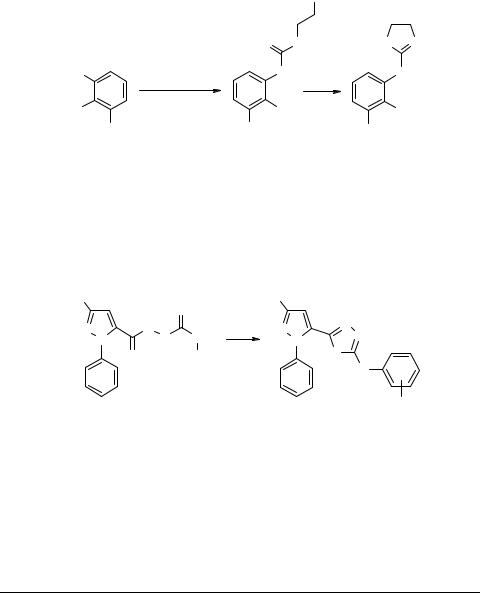
Запатентован метод получения замещенных 2-анилинооксазолидинов 21, основанный на конденсации β-хлорэтилизоцианата с ароматическими аминами и последующей циклизацией образовавшихся β-хлорэтилмочевин 20 длительным кипячением последних в водном метаноле [17]. 2-(2,6-Дихлорфениламино)оксазо- лидин, обладающий антиспазмолитическим действием [18], был получен циклоконденсацией N-(2,6-дихлорфенил)дихлорметанамина с моноэтаноламином в щелочной среде с выходом 90%.
|
|
|
Cl |
|
|
|
|
O NH |
O N |
H2N |
OCN(CH ) Cl |
NH |
NH |
|
|
2 |
2 |
|
|
R1 |
|
|
R1 |
R1 |
|
R |
|
R |
R |
|
|
|
20 |
21 |
Мягким |
окислением замещенных |
тиосемикарбазидов |
22 раствором иода |
|
в KI получены соответствующие 2-анилино-5-(3-метокси-1-фенил-1Н-пиразолил- 5)-1,3,4-оксадиазолы 23 [19]. В качестве окислителя также был использован оксид ртути(II) [20]. 2-Анилино-1,3,4-оксадиазолы, содержащие в пятом положении системы фрагмент имидазо[1,2-a]пиридина, были синтезированы в работе [21].
MeO |
|
S |
|
MeO |
|
|
H |
I2 |
|
N N |
|
|
|
N N |
|||
N N |
N N NH |
||||
O |
H |
Ar |
KI |
|
O |
|
|
|
|
|
N |
|
|
|
|
|
H |
|
|
|
|
|
R |
22 |
|
|
|
23 |
|
2-Ариламино-5-фенил-1,3,4-оксадиазолы также получены реакции нуклеофильного замещения 2-метилтио-5-фенил-1,3,4-оксадиазола с анилинами [22].
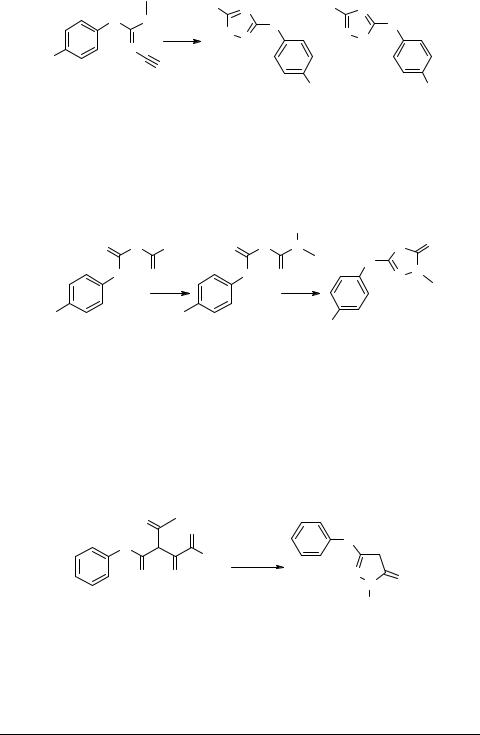
При конденсации 1-арил-3-циано-S-метилизотиомочевин 24 с гидроксиламином, в случаях электронодонорных заместителей в бензольном кольце, образуется смесь 5-амино-3-ариламино-1,2,4-оксадиазолов 25 и 3-амино-5-ариламино-1,2,4- оксадиазолов 26 с преобладанием изомера 25 [23]. В случае электроноакцепторных заместителей образуется только изомер 25.
Избранные методы синтеза и модификации гетероциклов, том 1 |
121 |
H |
|
H2N |
|
N H |
H N |
|
N H |
S |
|
|
2 |
|
|||
N |
NH2OH |
O |
N |
|
N |
N |
|
|
|
N |
+ |
O |
|||
|
N |
|
|||||
R |
|
|
|
|
|
||
|
N |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
R |
|
R |
24 |
|
|
|
25 |
|
|
26 |
Обработкой 1-(4-хлорфенил)-3-феноксикарбонилтиомочевины 27 метилгидразином в тетрагидрофуране при комнатной температуре получена 1-(2-метил- карбазоил)-3-(4-хлорфенил)тиомочевина 28. Кипячением последней в этаноле в течение 8 дней с выходом 42% выделен 5-(4-хлорфениламино)-2-метил-2,4-ди-
гидро-3Н-1,2,4-триазол-3-он 29 [24].
H |
|
H |
NH2 |
H |
O |
|
S N |
OPh |
S N |
N |
H N |
||
|
||||||
NH O |
|
NH |
O |
N |
N |
|
|
N |
|||||
Cl |
Cl |
|
|
Cl 29 |
|
|
27 |
|
28 |
|
|
Конденсацией натрий ацетоуксусного эфира с фенилизотиоцианатом была получена натриевая соль α-карбэтоксиацетоацетанилида 30. Кипячением последней с избытком гидразингидрата с выходом 76% образуется 3-анилино-5-пиразо- лон (31, R = H). Замена гидразингидрата в данной реакции на метилгидразин приводит к образованию 1-метил-3-анилинопиразол-5-он (31, R = CH3) с выходом 11% [25], но использование фенилгидразина не приводит к ожидаемому 1-фенил- 3-анилино-пиразол-5-ону. 1-Фенил-3-анилино-пиразол-5-он был получен с выходом 43% при кипячении 1-фенил-3-амино-5-пиразолона в избытке анилина до прекращения выделения аммиака [26].
|
O |
O |
H |
|
|
H |
|
|
|
||
|
|
N |
|
|
|
N |
|
OEt |
H2NNHR |
|
|
|
|
|
|
||
|
S O |
|
N |
N |
O |
|
|
|
|
|
|
30 |
|
|
31 |
R |
|
|
|
|
|
R = H, Me
Взаимодействием бромидов 2-амино-3-фенацил-5-метил-1,3,4-оксадиазолия 32 с ароматическими аминами в результате перегруппировки оксадиазолиевого кольца получены соответствующие 1-N-ацетамидо-2-ариламино-4-арилимидазолы
33 [27].
122 |
Серия монографий InterBioScreen |

|
|
NH2 |
|
O |
|
|
|
H |
|
|
N + Br |
|
|
|
|
|
N |
|
|
O |
N |
R1 |
N |
H |
R |
|
|||
|
|
N |
N |
|
|
NH2 O |
R |
|
|
|
32 |
|
33 |
R1 |
2-Ариламинобензоксазолы 36 синтезированы в результате реакции 2-мер- капто-, 2-метилтио- 34 или 2-феноксибензоксазолов 35 с соответствующими замещенными ароматическими аминами [28, 29].
O |
X + H2N |
N |
H |
N |
O |
N |
|
R |
R1 |
||
|
|
R1 |
|
34, 35 |
|
36 |
|
R = H, Me, Ph X = S, O |
|
|
|
R1 = H, OMe, NO2, Me |
|
|
|
о-Аминотиофенол присоединяется к диарилкарбодиимидам с образованием соответствующих замещенных изотиомочевин, которые в кислой среде легко циклизуются в 2-ариламинобензотиазолы с выделением ариламина [30]. 2-Ани- линобензотиазол образуется с высоким выходом в результате реакции калиевой соли 2-бензотиазолсульфокислоты с анилином [31].
Замещенные диарилтиомочевины 37, полученные взаимодействием о-фени- лендиамина с арилизотиоцианатами, при кипячении в спирте с иодистым метилом, циклизуются в 2-ариламинобензимидазолы (38 X = NH). Используя данную реакцию, на основе о-аминотиофенола получены 2-ариламинобензтиазолы (38 Х = S), а из о-аминофенолов – 2-ариламинобензоксазолы (38 Х = О) [32].
|
|
R |
|
|
S |
NH |
MeI |
|
|
NH2 ArNCS |
NH |
или |
N |
|
HgCl2 |
H |
|||
|
|
|
X |
N |
XH |
XH |
|
|
|
|
|
|
||
37 |
|
|
38 |
R |
X = NH, O, S |
|
|
|
|
Избранные методы синтеза и модификации гетероциклов, том 1 |
123 |
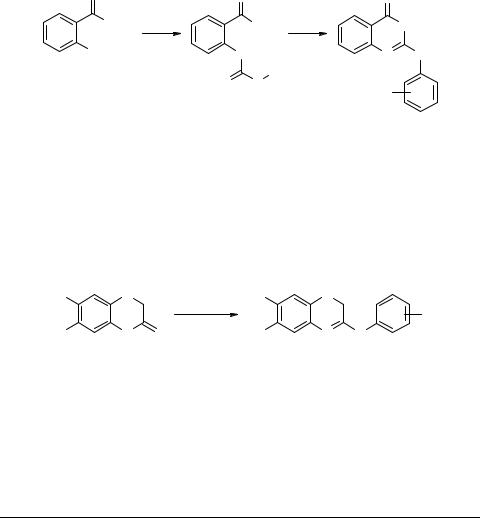
Общим методом синтеза замещенных 2-анилинобензимидазолов, бензтиазолов и бензоксазолов является десульфуризация оксидом или хлоридом ртути (II) продуктов 37, получаемых конденсацией о-фенилендиамина, о-амино- фенола или о-аминотиофенола с соответствующим арилизотиоцианатом [33–37]. В качестве циклодесульфуризующего агента предложен [38] дициклогексилкарбодиимид.
Обработка продукта 39 концентрированной серной кислотой приводит к образованию 2-ариламино-4Н-3,1-бензоксазин-4-онов 40 [39]. Последние также были получены [40] реакцией антранилата калия и N-арилдитиокарбамата в присутствии красной окиси ртути (II) в диметилформамиде при комнатной температуре.
O |
O |
O |
OMe ArNCO |
OMe H2SO4 |
O |
NH2 |
NH |
N NH |
O |
N Ar |
R |
|
H |
|
|
39 |
40 |
Нагреванием замещенных 2,3-дигидро-4Н-бензоксазин-3-тионов (41 Х = О) или, соответственно, 2,3-дигидро-4Н-бензотиазин-3-тионов (41 Х = S) с ароматическими аминами в присутствии хлорокиси фосфора и триэтиламина при 130°С в течение 3–5 ч получены [41] соответствующие 3-ариламино-2Н-бензоксазины (42 Х = О) и бензотиазины (42 Х = S).
R1 |
X |
R1 |
X |
|
|
ArNH2 |
R |
|
|
|
|
R2 |
N |
S POCl3, Et3N R2 |
N N |
|
H |
|
H |
|
41 |
|
42 |
X = O, S
Замещенные N-(о-цианофенил)-тиомочевины 43 при кипячении в водном ДМФА или без растворителя циклизуются, и в результате последующей перегруппировки Димрота образуют 4-(ариламино)-2-тиоксо-1,2-дигидрохиназолины
44 [42].
124 |
Серия монографий InterBioScreen |

H |
|
HN Ar |
|
S N Ar |
|
|
|
NH |
t° |
N |
|
|
|
||
CN ДМФА |
N |
S |
|
|
|
H |
|
43 |
|
44 |
|
Кипячением 4-N-окиси 2-гидразино-6-хлорхиноксалина 45 с избытком ортомуравьиного эфира в диметилформамиде с выходом 83% был получен 7-хлор- 1,2,4-триазоло[4,3-a]хиноксалин-5-N-оксид 46. Обработкой последнего фенилизоцианатом и разложением образовавшегося промежуточного продукта осуществлен синтез 7-хлор-4-анилино-1,2,4-триазоло[4,3-a]хиноксалина 47 [43]. Интересно отметить, что замена фенилизоцианата в данной реакции на фенилизотиоцианат приводит только к восстановлению N-оксида и образованию 7-хлор-1,2,4-три- азоло[4,3-a]хиноксалина.
|
O |
|
O |
|
|
|
Cl |
N+ |
HC(OEt)3 Cl |
N+ |
PhNCO Cl |
N |
NH |
|
N |
NH |
N |
t°, −CO2 |
N |
N |
|
N |
|||||
|
45 |
NH2 |
46 |
N |
47 |
N |
|
|
|
|
Одним из разнообразных способов синтеза, замещенных 2-анилиноимидазо- лина, является нуклеофильное замещение метилмеркаптогруппы ариламинами в 2-метилтиоимидазолине [44–46].
2-Анилино-1,4,5,6-тетрагидропиримидин 49 был получен при сплавлении фенилцианамида 48 с 1,3-пропандиамином с выходом 29% [47].
|
N |
HN |
|
|
|
HN |
|
HN N |
|
|
NH2 |
|
|
+ |
|
|
NH2 |
48 |
|
49 |
Обработкой N-(3-нитрофенил)тиомочевины 50 иодистым метилом в ацетонитриле получен N-(3-нитрофенил)-S-метилизотиуроний иодид 51. Последний без
Избранные методы синтеза и модификации гетероциклов, том 1 |
125 |
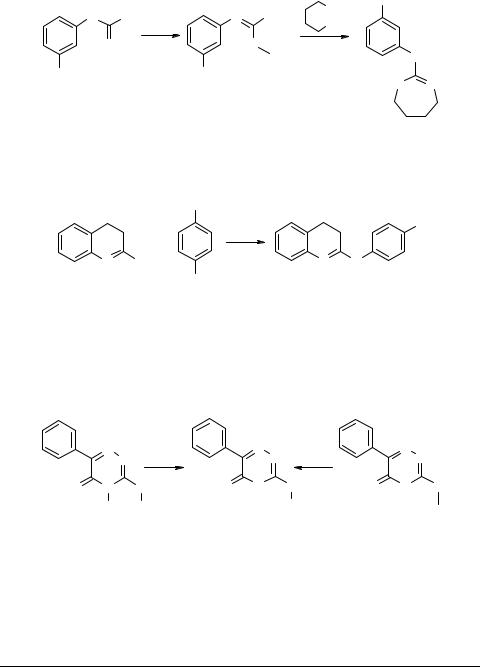
дополнительной очистки вводили в реакцию с двукратным количеством 1,4-бутан- диамина в среде ДМСО при температуре 110°С. В результате был получен 2-(3-нитрофенилимино)-2,3,4,5,6,7-гексагидро-1Н-1,3-диазепин 52 [48].
H |
|
|
|
NO2 |
NH2 MeI |
N |
NH2 |
NH2 |
|
N |
NH |
|||
|
|
|
|
2 |
|
S |
HI |
S |
NH |
|
|
|
||
NO2 |
|
NO2 |
|
HN N |
|
|
|
|
|
50 |
|
51 |
|
52 |
При кипячении эквимолярной смеси 2-этокси-3,4-дигидрохинолина 53 с ариламинами в ксилоле получены 2-ариламино-3,4-дигидрохинолины 54 [49].
NH2
R
+
N OEt |
|
N N |
|
|
R |
H |
|
53 |
54 |
||
|
|||
R = Br, OMe |
|
|
Дезаминированием 4-амино-3-анилино-5-оксо-6-фенил-4,5-дигидро-1,2,4-три- азина 55 с выходом 85% синтезирован 3-анилино-5-оксо-6-фенил-4,5-дигидро- 1,2,4-триазин 56 [50]. Последний также получают кипячением 3-метилмеркапто- 5-оксо-6-фенил-4,5-дигидро-1,2,4-триазина 57 в избытке анилина [51].
N |
N |
HNO2 |
|
N |
N |
PhNH2 |
|
N |
N |
|
|
|
|
|
|
||||
O N |
|
NH |
O |
N |
|
NH |
O |
N |
S |
NH2 |
Ph |
|
H |
|
Ph |
|
H |
|
|
|
|
|
|
|
|
||||
55 |
|
|
|
56 |
|
|
|
57 |
|
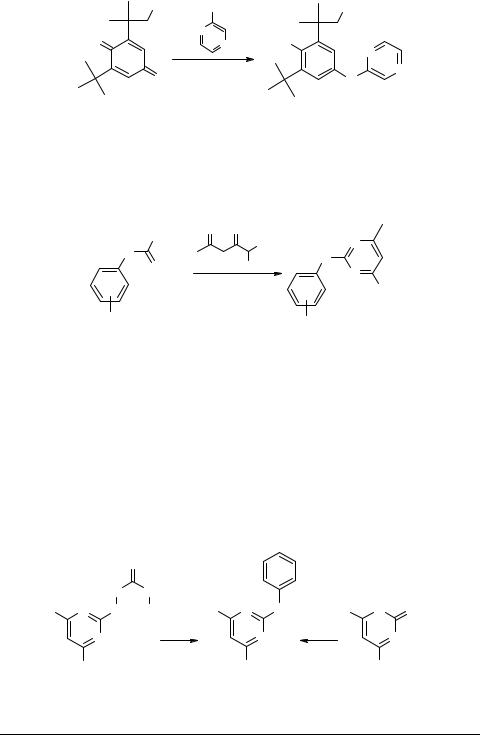
Нагревание 2-(1,1-диметилэтил)-6-(1,1-диметил-2-гидроксиэтил)-1,4-бензохи- нона 58 с эквимолярным количеством 2-аминопиперазина в хлористом метилене при катализе пиридином и четыреххлористым титаном получают соответствующий имин [52]. Гидрированием последнего в присутствии платинового катализатора осуществлен синтез 2-(1,1-диметилэтил)-6-(1,1-диметил-2-гидроксиэтил)- 4-(2-пиперазиниламино)фенола 59.
126 |
Серия монографий InterBioScreen |
OH |
NH2 |
|
OH |
|
O |
N |
HO |
|
|
N |
|
N |
||
|
|
|
|
|
O |
H2 (Pt) |
|
N |
N |
|
|
|
||
58 |
|
|
H |
|
|
|
59 |
|
Взаимодействие карбонатов арилгуанидина 60 с 1,1-диэтоксипентандионом- 2,4 [54–56] или с R1СOCH=CHNMe2 [57] приводит к ряду замещенным 2-анилино- пиримидинам 61, содержащим в четвертом положении системы диэтилацетальную группу [53]. На основе последней были синтезированы нитрилы, оксимы и другие производные 61.
|
O |
O |
|
H |
NH2 |
OEt |
H N |
N |
NH |
OEt |
N |
|
|||
|
N |
||
|
|
|
|
|
H2CO3 |
|
R1 |
R |
|
|
R |
60 |
|
|
61 |
2-Метилтиопиримидин-4(3Н)-он, полученный алкилированием 2-тиоурацила, вступает в реакцию нуклеофильного замещения с замещенными ароматическими аминами, образуя N2-арилизоцитозины с хорошими выходами [57].
2-Анилинопиримидины были получают в результате нуклеофильного замещения 2-сульфонилметильной группы [58] или атома галогена [59–65]. Кипячением в спирте в присутствии триэтиламина производных 2-хлорпиримидина с соответствующими ароматическими аминами получены 2-ариламинопиримидины [66–69]. Кратковременным нагреванием 1-(41-окси-61-фенил-21-пиримидинил)- 4-фенил-3-тиосемикарбазида 62 до 250°С выделен 2-анилино-4-окси-6-фенилпири- мидин 63 [70]. Последний также был получен из 2-нитрамино-4-окси-6-фенил- пиримидина 64 и анилина.
S |
|
|
|
|
|
|
HN |
NH |
|
|
|
H |
|
|
|
Ph |
N NH |
|
NNO2 |
|
Ph N NH |
Ph |
Ph N |
||||
N |
|
250°C |
N |
PhNH2 |
N |
|
|
|
190°C |
|
|||
OH |
|
|
OH |
OH |
|
|
|
|
|
|
|||
62 |
|
|
63 |
|
64 |
|
Избранные методы синтеза и модификации гетероциклов, том 1 |
127 |
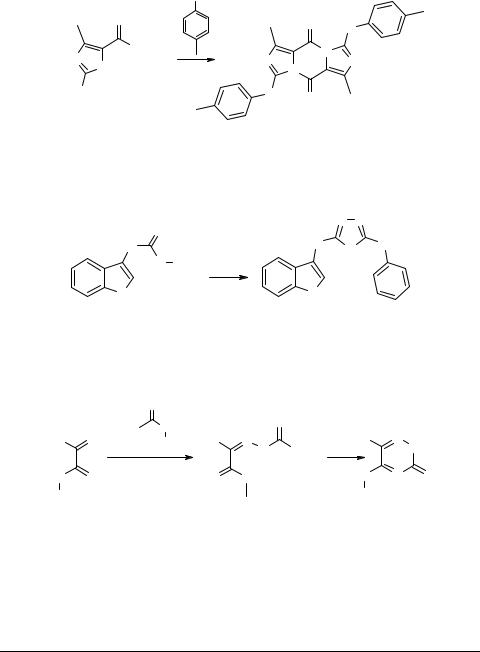
Взаимодействием ароматических аминов с двукратным количеством этилового эфира 2-бром-4-метилимидазол-5-карбоновой кислоты 65 получены соответствующие диимидазо[1,5-a:11,51-d]пиразиндионы 66. Строение последних установлено методом рентгеноструктурного анализа [71].
|
|
|
NH2 |
|
|
|
|
|
O |
|
O |
|
H |
|
|
|
|
|
|
N |
2 |
N |
OEt |
N |
|
N |
N |
NH |
N |
|
||||
|
|
|
|
|
||
|
Br |
|
N |
O |
|
|
|
|
|
H |
|
|
|
|
|
|
|
|
|
|
|
|
65 |
|
|
66 |
|
Конденсацией N-(бензофурил-3)гидразинокарбоксамида 67 с фенилизотиоцианатом и последующей циклоконденсацией промежуточной тиомочевины получен 2-анилино-5-(31-бензофуриламино)-1,3,4-оксадиазол 68 [72].
H |
O |
|
N N |
|
HN O NH |
||
N |
N NH2 |
|
|
|
PhNCS |
|
|
|
H |
|
|
O |
|
−H2S |
O |
67 |
|
|
68 |
Замещенные 5-ариламино-6-фенил-1,2,4-триазин-3-оны (70 R = Ph) получены конденсацией α-бензоилтиоформанилидов (69 R = Ph) с семикарбазидом в щелочной среде и последующей обработкой иодистым метилом [73].
O
|
HN2 |
NH |
|
|
|
O |
R |
N |
|
R |
O |
NH2 R |
N |
N |
NH2 |
NH |
|||
|
|
|
|
|
|
|
|||
HN |
S |
MeI |
ArN |
|
H |
|
HN |
N O |
|
S |
|
|
|||||||
|
|
|
|||||||
Ar |
|
|
|
|
|
|
Ar |
|
|
69 |
|
|
|
|
|
|
|
70 |
|
R = Ph, Me
Кипячением в пиридине эквимолярных количеств замещенных α-ацетилтио- форманилидов (69 R = Me) с о-фенилендиамином получены [74, 75] 2-ариламино- 3-метилхиноксалины. Следует отметить, что взаимодействие этих же исходных реагентов в метаноле при комнатной температуре приводит к образованию 3-метил-2-меркаптохиноксалина [76].
128 |
Серия монографий InterBioScreen |
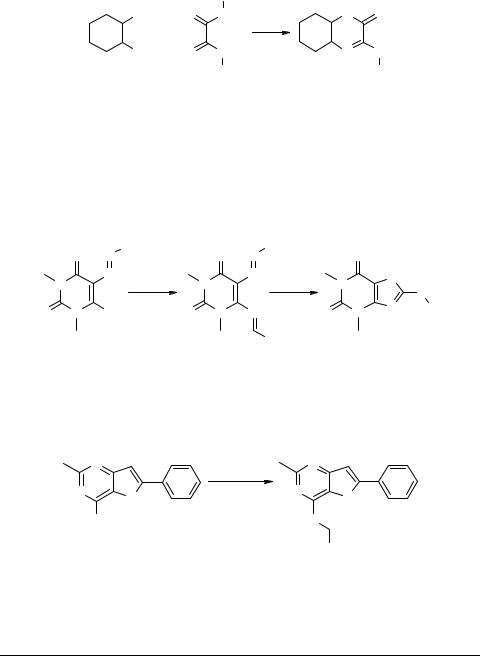
Взаимодействием N,N1-бис(4-метилфенил)дитиооксамида 71 с транс-1,2-цик- логександиамином в ДМСО при 40°С с выходом 71% получен 3-(4-толуидино)- 4а,5,6,7,8,8а-гексагидрохиноксалинтион-2 72 [77].
|
Ar |
H |
|
NH2 |
|
|
|
S NH |
N |
S |
NH2 |
+ |
−ArNH2 |
N NH |
|
S NH |
||||
|
||||
|
Ar |
|
Ar |
|
|
71 |
|
72 |
Конденсацией 6-амино-5-арилазо-1,3-диметилурацилов 73 с ортомуравьиным эфиром получены соответствующие 5-арилазо-6-этоксиметиленамино-1,3-ди- метилурацилы 74. Кратковременным их нагреванием с дитионитом натрия в муравьиной кислоте синтезированы 8-ариламинотеофиллины 75 [78]. Последние также получают обработкой 8-хлор(бром)теофиллина избытком замещенного анилина при 180°С в течение трех часов [79, 80].
|
O N Ar |
O |
N Ar |
O |
H |
|
||
|
N |
HC(OEt)3 |
|
N Na2S2O4 |
|
|
||
N |
N |
N |
N |
H |
||||
|
|
|
|
|
HCO2H |
|
N |
N |
O N NH2 |
|
O N |
N |
O N |
Ar |
|||
|
|
|||||||
|
73 |
|
74 |
|
OEt |
75 |
|
|
|
|
|
|
|
|
|||
Нуклеофильным замещением атома хлора в 4-хлор-2-метил-6-фенил-5Н-пир- роло[3,2-d]пиримидине 76 путем кипячения в избытке бензиламина синтезирован 4-бензиламино-2-метил-6-фенил-5Н-пирроло[3,2-d]пиримидин 77 [81].
|
N |
N |
|
|
|
PhCH2NH2 |
|
N |
N |
N |
N |
|
H |
HN |
H |
|
Cl |
|
|
|
76 |
Ph |
77 |
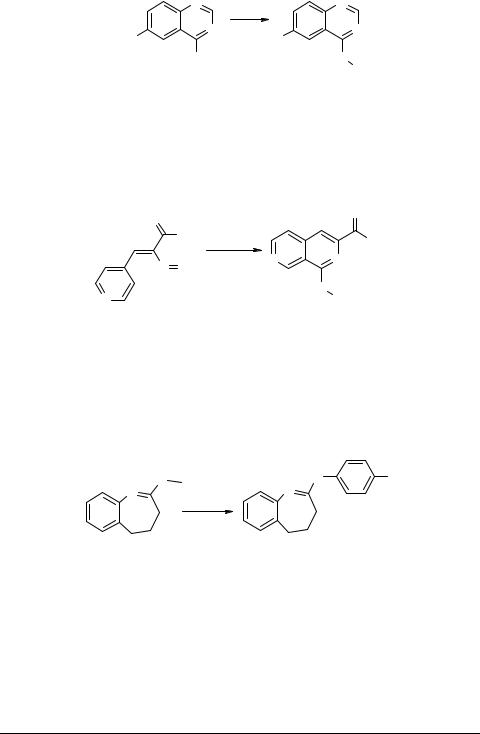
Запатентован способ получения 4-арил-6-нитрохиназолонов 79 из 4-хлор-6- нитрохиназолона 78 и ароматических аминамов [82–86].
Избранные методы синтеза и модификации гетероциклов, том 1 |
129 |
|
N |
ArNH2 |
N |
|
|
|
|
||
O2N |
N |
O2N |
N |
|
Cl |
HN Ar |
|||
|
|
|||
|
78 |
|
79 |
Этиловый эфир 1-ариламино(2,7-нафтиридин)-3-карбоновой кислоты 81 получают обработкой замещенного иминофосфорана 80 арилизоцианатом в толуоле с последующим термическим разложением промежуточного продукта [87].
O |
|
O |
|
|
|
OEt |
ArNCO |
OEt |
|
||
N PPh3 |
160°C N |
N |
|
|
|
N |
|
HN Ar |
80 |
|
81 |
Нагреванием иодистоводородной соли 2-метилтио-4,5-дигидро-3Н-1-бензазе- пина 82 с алифатическими и ароматическими аминами в спиртах с высокими выходами были получены 2-ариламино-4,5-дигидро-3Н-1-бензазепины 83, обладающие широким спектром биологической активности [88].
S |
H |
R |
N |
||
N |
N |
|
|
ArNH2 |
|
82 |
83 |
|
При изучении реакции 6-хлорфенантридина 84 с аминами, найдено, что наилучший выход конечного продукта 85 достигается при кипячении исходного имидоилхлорида 84 непосредственно в растворе соответствующего амина: в случае алифатических аминов реакция заканчивается за 4 ч, тогда как реакция с замещенными анилинами требует семичасового кипячения. Во всех случаях эффективному протеканию реакции благоприятствует наличие в реакционной смеси следов POCl3 [89–90].
130 |
Серия монографий InterBioScreen |
