
- •80 Теория цветности органических соединений
- •Часть 1 Теория цветности органических соединений
- •1. Физические основы цветности
- •1.1. Природа света и происхождение цветоощущения
- •1.2. Спектральный способ регистрации поглощенного света и спектральная терминология
- •1.3. Взаимодействие электромагнитного излучения с веществом
- •1.3.1. Конфигурация электронно-колебательных уровней
- •1 Лекция 3.3.2. Принцип Франка-Кондона и форма полос поглощения
- •2. Анализ электронной структуры методами квантовой химии.
- •2.1. Способы описания энергетических состояний молекул.
- •2.2. Основные принципы метода возмущения молекулярных орбиталей
- •2.3. Формирование мо и основные типы электронных переходов
- •3. Экспериментальные методы изучения электронной структуры
- •3.1. Фотоэлектронная спектроскопия
- •3.2. Электронная трансмиссионная спектроскопия
- •4. Основные положения теории цветности
- •4.1. Электронные переходы в молекулах углеводородов
- •4.1.1. Энергии электронных переходов в насыщенных углеводородах
- •4.1.2. Энергии электронных переходов в сопряженных системах
- •4.1.3. Энергия электронных переходов в ароматических углеводородах
- •4.1.4. Альтернантные и неальтернантные -системы
- •4.1.5. Типы возмущений и их влияние на энергию –мо
- •4.2. Электронные переходы в молекулах, содержащих гетероатомы
- •4.2.1. Переходы в гетероцепных четных альтернантных системах
- •4.2.2. Переходы в гетероцепных нечетных альтернантных системах
- •4.3. Влияние поляризующих заместителей на поглощение света сопряженными системами
- •4.3.1. Классификация заместителей
- •4.3.2. Электронодонорные заместители
- •4.3.3. Электроноакцепторные заместители
- •4.3.4. Совместное действие поляризующих эд и эа заместителей
- •4.3.5. Полосы переноса заряда
- •4.4. Влияние ионизации на поляризующее действие заместителей
- •4.4.1. Ионизация эд-заместителей
- •4.4.2. Ионизация эа-заместителей
- •4.4.3. Ионизация сложных молекул
- •4 Лекция 9.5. Сложные конкурирующие и перекрещивающиеся сопряженные системы
- •4.5.1. Разветвленные сопряженные системы
- •4.5.2. Объяснение спектральных закономерностей при образовании разветвленных сопряженных систем методом возмущения мо
- •4.5.3. Перекрещивающиеся сопряженные системы
- •4 Лекция 10.6. Влияние пространственных факторов на поглощение света
- •4.6.1. Нарушение копланарности сопряженной системы
- •4.6.2. Искажение валентных углов
- •4.7. Комплексообразование с металлами
- •4.7.1. Комплексообразование с углублением цвета
- •4.7.2. Комплексообразование без углубления цвета
- •5. Хромофорная система красителей
3.2. Электронная трансмиссионная спектроскопия
Э
Лекция
5
M + e = M
По выходе из ионизационной камеры пучок электронов попадает в коллектор, где и регистрируется изменение его интенсивности (число электронов в секунду). Время жизни образовавшихся анион-радикалов невелико. При распаде они освобождают "вторичные" электроны, которые оказываются в общем потоке. Однако вектор скорости "вторичных" электронов не ориентирован, в коллектор они не попадают и рассеиваются. Поэтому фактически измеряют интенсивность потока только нерассеянных, "первичных" электронов.
При плавном увеличении энергии ионизирующих электронов создаются другие условия для их рассеивания. Таким образом, в выбранном диапазоне изменения энергии электронов регистрируется ЭТ-спектр в виде кривой в координатах: интенсивность рассеянного потока I(осьyординат) - энергия электроновЕ, эВ(осьxабсцисс).

Резонанс в ЭТ спектре находят как точки перехода минимума в максимум пропущенного тока электронов при возрастании энергии электронов, направляемых в ионизационную камеру. Проекция этих точек на ось х дает энергию внедрения на вакантную МО, которую называют сродством молекулы к электрону А (эВ).
В свою очередь величину сродства соотносят с собственной энергией вакантной МО в рамках теоремы Купманса: Аi = – Еi .
Форма кривых ЭТ-спектра зависит от продолжительности жизни анион-радикала.
Короткоживущая частица (этилен) дает плавную кривую с двумя экстремумами. Если время жизни анион-радикала больше периода колебания ядер (формальдегид), то в спектре проявляется колебательная структура резонансного сигнала. Она отвечает заселению отдельных колебательных уровней НВМО. В этом случае по первому пику можно измерить адиабатическую энергию присоединения электрона, Аад. В остальных случаях ограничиваются определением вертикальной энергии, Аверт.
4. Основные положения теории цветности
4.1. Электронные переходы в молекулах углеводородов
4.1.1. Энергии электронных переходов в насыщенных углеводородах
С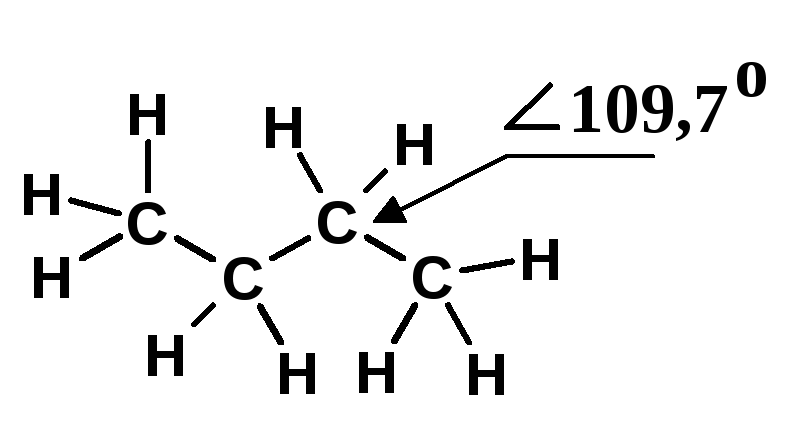 огласно
данным рентгеноструктурного анализа
в метане и всех алканах линейного
строения валентные углы у атомов углерода
близки к тетраэдрическому углу (109,7о),
свойственному дляsp3-состояния,
и сохраняются стандартные длины связей
(С-С равная 1,53Å и С-Н равная 1,10Å).
огласно
данным рентгеноструктурного анализа
в метане и всех алканах линейного
строения валентные углы у атомов углерода
близки к тетраэдрическому углу (109,7о),
свойственному дляsp3-состояния,
и сохраняются стандартные длины связей
(С-С равная 1,53Å и С-Н равная 1,10Å).
Эти связи и соответствующие МО формируются в результате фронтального перекрывания базисных орбиталей водорода (1s) и углерода (2sp3) и являются-связями. Смешивание базовых орбиталей сопровождается наибольшим расщеплением между связывающими и разрыхляющими -и*- электронными уровнями, что связано с большими значениями интеграла перекрыванияS, например, для (sp3-sp3) смешивания он равен 0,78.
Поэтому связывающиеС-С и С-Н-МОалкановимеют низкую энергиюи располагаются в диапазоне11-15 эВ, При этом различие в значениях энергии для верхних С-Hи С-С МО невелико и не превышает 0,5 эВ. При удлинении углеродной цепочки в гомологическом ряду алканов энергия ВЗМО возрастает незначительно. Это следствие малого перекрывания (геометрический фактор)и незначительного смешивания новых -и*-МОс уже имеющимися МО. Наблюдаемое приращение энергииЕ невелико и с ростом числа атомов углерода быстро падает., Об этом свидетельствует характер изменения значений первых потенциалов ионизацииI1из данных ФЭС.
|
n в CnH2n+2 |
1 |
2 |
3 |
4 |
5 |
6 |
8 |
10 |
|
I1эксп, эВ |
13,61 |
11,76 |
11,21 |
10,70 |
10,55 |
10,41 |
10,25 |
10,19 |
Напротив, вакантные*-МОв алканах обладаюточень высокой энергией, например, электронное сродствон-гексана, отвечающее расположению НВМО, оценивается в – 0,9эВ. Значительные величины энергетической щели (E> 10 эВ) между граничными- и*-МО в алканах приводит к тому, что энергия* электронных переходов велика и составляет 850-870кДж/моль.
Поэтому соответствующие полосы поглощения в электронных спектрах этих соединений располагаются в далекой УФ-области.
|
* переход |
Соединение |
Метан |
Этан |
н-Октан |
н-Декан |
|
максв ЭСП (нм) |
128 |
135 |
142 |
146 |
Например, в спектре метана макснаходится при128нм, этанамакспри135нм, октанамакспри142нм. Все линейные алканы и даже полиэтилен, который содержит до 1 000 000 простых С-С связей, бесцветны. Сказанное справедливо и для разветвленных алканов и циклоалканов.
Таким образом молекулярные структуры, которые содержат только простые -связи, не представляют интереса для химии красителей.
