
- •Кафедра оФиФнгп
- •Сборник задач по физике
- •И примеры их решения
- •Часть
- •Предисловие
- •Программа курса физики
- •Молекулярная физика и термодинамика
- •Электростатика
- •Библиографический список
- •Методические указания к решению задач и выполнению контрольных работ
- •Контрольная работа № 1
- •Механика
- •Основные формулы
- •Кинематика
- •Динамика
- •Законы сохранения
- •Динамика твердого тела
- •Механические колебания
- •Примеры решения задач
- •Решение
- •Решение
- •Решение
- •Решение
- •Решение
- •Решение
- •3,8.1016 Дж.
- •Задачи для самостоятельного решения
- •Контрольная работа №2
- •Термодинамика
- •Электростатика
- •Примеры решения задач
- •Решение
- •Решение
- •Решение
- •Решение
- •Решение
- •Решение
- •Решение
- •Решение
- •Решение
- •Решение
- •Решение
- •Решение
- •Решение
- •Задачи для самостоятельного решения
- •1. Основные физические константы
- •2. Молярная масса м, 10–3 (кг/моль)
Примеры решения задач
Пример 1.
В двух теплоизолированных сосудах
объемами
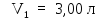 и
и находится одинаковый идеальный газ при
давлениях
находится одинаковый идеальный газ при
давлениях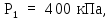
 и температурах
и температурах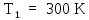 ,
, .
Сосуды соединяют трубкой. Какая
температура установится в сосудах после
смешивания газов?
.
Сосуды соединяют трубкой. Какая
температура установится в сосудах после
смешивания газов?
Решение
Внутренняя энергия
газов, находящихся в первом и втором
сосудах до их смешивания, равна (см.
(8Ф)):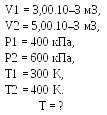
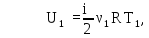
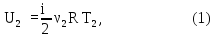
где
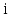
 число степеней свободы молекул газа;
число степеней свободы молекул газа;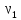 ,
,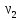 – число
молей газов в первом и втором сосудах;
R
=
8,31 Дж/(моль.К)
–
универсальная
газовая постоянная (находится из
таблицы). Используем уравнение Менделеева
–
Клапейрона (2Ф) для газов
в первом и
втором сосудах
– число
молей газов в первом и втором сосудах;
R
=
8,31 Дж/(моль.К)
–
универсальная
газовая постоянная (находится из
таблицы). Используем уравнение Менделеева
–
Клапейрона (2Ф) для газов
в первом и
втором сосудах
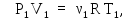

Сравнивая первые и вторые формулы в равенствах (1), (2), имеем:
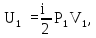
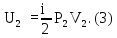
Общая энергия
газов в сосудах до их соединения
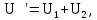 или учитывая (3), получим:
или учитывая (3), получим:
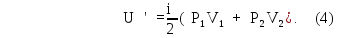
После смешивания
газов (соединение сосудов трубкой)
установится искомая температура
 и внутренняя энергия газа (8Ф)
и внутренняя энергия газа (8Ф)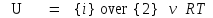 ,
или учитывая
,
или учитывая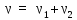 ,
получим:
,
получим:
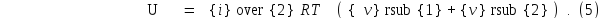
Число молей
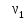 и
и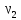 найдем из уравнений (2) и подставим их в
(5). В результате получим
найдем из уравнений (2) и подставим их в
(5). В результате получим
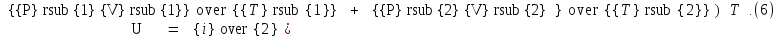
Сосуды
теплоизолированные, поэтому
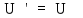 (закон
сохранения энергии), откуда с учетом
(4) и (6), найдем искомую температуру:
(закон
сохранения энергии), откуда с учетом
(4) и (6), найдем искомую температуру:
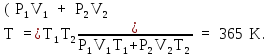
Пример 2.
Кислород массой
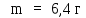 находится при температуре
находится при температуре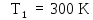 и расширяется при постоянном давлении,
при этом объем увеличивается в
n
=
V2/V1
=
2,0
раза. Найти
количество
теплоты, сообщенной газу.
и расширяется при постоянном давлении,
при этом объем увеличивается в
n
=
V2/V1
=
2,0
раза. Найти
количество
теплоты, сообщенной газу.
Решение
Используем первое
начало термодинамики (9Ф)

Количество
теплоты, сообщенной газу, идет на
приращение внутренней энергии
 газа и на совершение газом работы
газа и на совершение газом работы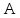 против внешних сил. Приращение внутренней
энергии
против внешних сил. Приращение внутренней
энергии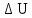 =
U2
–
U1,
или, учитывая (8Ф), получим:
=
U2
–
U1,
или, учитывая (8Ф), получим:

где
 =
5 –
число степеней свободы молекул
двухатомного кислорода;
=
5 –
число степеней свободы молекул
двухатомного кислорода;
R
=
8,31 Дж/(моль.К)
–
универсальная газовая постоянная
(находится из таблицы);
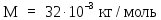 –
молярная масса кислорода (находится из
таблицы);
–
молярная масса кислорода (находится из
таблицы);
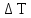 –
приращение
температуры. Работа газа при изобарном
процессе (11Ф)
–
приращение
температуры. Работа газа при изобарном
процессе (11Ф)
 (3)
(3)
С учетом (2) и (3) количество теплоты (1) запишется
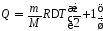 ,
(4)
,
(4)
где
ΔТ
=
Т2
–
Т1.
Применяя уравнение Менделеева –
Клапейрона (2Ф) для изобарного процесса,
имеем:
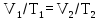 ,
откуда, с учетом условия задачи конечная
температура после изобарного расширения
,
откуда, с учетом условия задачи конечная
температура после изобарного расширения
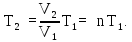
Тогда приращение температуры

Подставляя это выражение в (4), получим:

Учитывая условие задачи и табличные данные, найдем искомое количество теплоты:
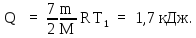
Пример 3.
Объем одного моля (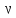 =
1) идеального газа с числом степеней
свободы молекул
=
1) идеального газа с числом степеней
свободы молекул
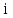 изменяется по законуV
=
а/Т,
где
изменяется по законуV
=
а/Т,
где
 – постоянная величина. Найти количество
теплоты, полученной газом в этом процессе,
если его температура испытала приращение
– постоянная величина. Найти количество
теплоты, полученной газом в этом процессе,
если его температура испытала приращение .
.
Решение
Количество теплоты
находится из первого начала термодинамики
(9Ф)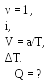
Q = ΔU + A. (1)
Приращение
внутренней энергии одного моля газа
 =
U2
–
U1,
или, учитывая (8Ф), имеем:
=
U2
–
U1,
или, учитывая (8Ф), имеем:
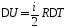 ,
(2)
,
(2)
где R = 8,31 Дж/(моль.К) – универсальная газовая постоянная (берется из таблицы). Работа газа (10Ф)

Воспользуемся уравнением Менделеева – Клапейрона (2Ф) для одного моля газа (ν = 1)
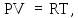
откуда, учитывая условие задачи,
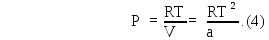
Продифференцируем условие задачи V = а/Т

Подставляя (4) и (5) в формулу (3), найдем работу:
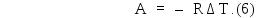
С учетом (2) и (6) количество теплоты (1) равно

Пример 4.
Два моля идеального газа находятся при
температуре
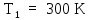 и охлаждаются изохорно, в результате
давление газа уменьшилось вn
=
P1/P2
=
2,0 раза. Затем
газ изобарно расширяется так, что в
конечном состоянии его температура
стала равной первоначальной. Найти
количество теплоты, сообщенной газу в
данном процессе.
и охлаждаются изохорно, в результате
давление газа уменьшилось вn
=
P1/P2
=
2,0 раза. Затем
газ изобарно расширяется так, что в
конечном состоянии его температура
стала равной первоначальной. Найти
количество теплоты, сообщенной газу в
данном процессе.
