
- •Содержание
- •Билет №1
- •2. Определение катаболизма. Катаболизм и анаболизм. Стадии катаболизма биомолекул в организме.
- •Билет№2.
- •1.Ферменты. Специфичность ферментов. Активный центр фермента.
- •2.Экзергонические и эндергонические биохимические реакции. Роль атф и других макроэргических фосфатов в сопряжении экзергонических процессов и эндергонических процессов.
- •3.Пути внутриклеточного метаболизма глюкозы. Гликолиз и глюконеогенез. Обратимые и необратимые реакции.
- •Билет №3
- •1.Регуляция активности ферментов. Проферменты. Изоферменты. Ингибиторы ферментов.
- •2.Реакции биологичемкого окисления.Типы реакций( дегидрогеназные, оксидазные, оксигеназные. Их биологическое значение.
- •3 Цитохромы Катализируют окисление веществ путем отдачи электронов Гемовое железо в одном из цитохромов имеется так же атом меди.
- •Билет№4
- •1.Ферментативный катализ
- •2.Митохондриальный транспорт
- •3.Аэробное окисление пирувата (окислительное декарбоксилирование пировиноградной кты).
- •Билет№5
- •1.Кинетика ферментативного катализа. Уравнение Михаэлиса-Ментен. Уравнение Лайнуивера-Берка.
- •2.Окислительное фосфорилирование. Пункты сопряжения окисления и фосфорилирования. Атф-синтетаза митохондрий.
- •3 Субъединицы (γ,δ,ε) способствуют целостности атф-синтазы
- •3.Полное окисление глюкозы. Энергетический баланс
- •Билет№6
- •1.Аллостерические ферменты. Ингибиторы и активаторы аллостерических ферментов. Аллостерические центры.
- •Деградация жирных кислот: β-окисление
- •Билет№7
- •1.Опять ферменты
- •2. Ингибиторы и разъединители транспорта электронов окислительного фосфорилирования
- •3.Глюконеогенез
- •Билет №8
- •1. Витамины
- •2. Микросомальная цепь транспорта электронов
- •3. Глюкозолактонный цикл
- •1. Витамин в2
- •3.Гипергликемия
- •Билет 10
- •Билет 11
- •1. Витамин в6(пиридоксин, пиридоксаль, пиридоксамин)
- •3 Существуют три источника аминокислот в клетке – поступление из крови, распад собственных внутриклеточных белков и синтез заменимых аминокислот.
- •Билет 12
- •1.Биотин
- •2. Нарушение обмена гликогена
- •3. Существуют три источника аминокислот в клетке – поступление из крови, распад собственных внутриклеточных белков и синтез заменимых аминокислот.
- •Билет 13. Фолиевая кислота. Биологическая роль. Пути поступления в организм. Коферментная функция.
- •2.Катаболизм триацилглицеролов. Реакции, механизм регуляции активности триглицеридлипазы. Нейрогуморальная регуляция липолиза (адреналин, глюкагон, инсулин).
- •3.Трансаминирование амк. Аминотрансферазы. Отдельные аминотрансферазы. Реакции. Биохимическое значение трансаминирования амк.
- •Билет 14
- •1.Витамин в12. Биологическая роль. Пути попадания в организм. Коферментная функция.
- •3.Пути превращения аммиака в организме человека. Механизмы обезвреживания аммиака.
- •Билет №15
- •1.Витамин с.
- •2.Окисление пальмитиновой кослоты.
- •3.Биосинтез мочевины.
- •Билет №16
- •1.Витамин а.
- •2.Окисление ненасыщенных жирных кислот.
- •3.Превращение безазотистого скелета ак
- •Билет №17
- •1.Витамин д
- •2. Биосинтез высших жирных кислот.
- •3. Метаболизм ак с разветвленной цепью.
- •Билет №25 Репликация днк
- •Свойства процесса репликации:
- •Желчные кислоты
- •Стероидные гормоны
- •2.Специализированные пути метаболизма цикл. А,к- фенилаланина и тирозина.. Заболевания, связанные с нарушением обмена фенилаланина и тирозина.
- •3.Биосинтез гема
- •Билет 19
- •2.Биосинтез пуриновых нуклеотидов
- •3.Основные закономерности генетического кода. Адапторная гипотеза ф. Крика и её развитие в wobble-гипотезе.
- •Билет №20
- •2. Кинетика ферменативного катализа. График зависимости скорости ферментативной реакции от концентрации субстрата при постоянной концентрации фермента.
- •Билет №21
- •Транскрипционные факторы: Механизмы действия тф , связавающиеся с днк, могут влиять на транскрипцию генов через несколько механизмов:
- •Билет№22
- •Билет 23
- •2. Полное окисление глюкозы. Энергетический баланс полного окисления глюкозы.
- •Билет№24
- •1.Антибиотические вещества, подавляющие синтез белка
- •24.2 Функционирование малат-аспартатного и глицерофосфатного шунта.
- •Билет №26
- •3. Окисление капроновой кислоты
- •Билет №27
- •Репликация
- •Билет 28
- •Билет29
- •29.2.Метаболизм аминокислот
- •Билет №30
- •1.Особенности молекулярной организации и экспрессии генома эукариот (экзоны, интроны, сплайсинг)
- •2.Образование кетоновых тел и их утилизация.
- •3.Цикл трикарбоновых кислот. Реакции
2.Окислительное фосфорилирование. Пункты сопряжения окисления и фосфорилирования. Атф-синтетаза митохондрий.
Окислительное фосфорилирование — один из важнейших компонентов клеточного дыхания, приводящего к получению энергии в виде АТФ. Субстратами окислительного фосфорилирования служат продукты расщепления органических соединений — белки, жиры и углеводы.
Окислительное фосфорилирование, синтез АТФ из аденозиндифосфата и неорганического фосфата, осуществляющийся в живых клетках, благодаря энергии, выделяющейся при окислении орг. веществ в процессе клеточного дыхания. В общем виде окислительное фосфорилирование и его место в обмене веществ можно представить схемой:
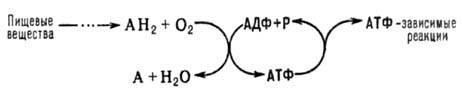
Механизм
окислительного фосфорилирования
можно представить схемой:
Перенос электронов
(дыхание)
![]() А
~ В
А
~ В![]() АТФ
А ~ В-высокоэнергетич. интермедиат
Предполагалось, что А ~ В - хим. соед. с
макроэргич. связью, напр. фосфорилир.
фермент
дыхат. цепи (хим. гипотеза сопряжения),
или напряженная конформация
к.-л. белка,
участвующего в окислительном
фосфорилировании
(конформац. гипотеза сопряжения). Однако
эти гипотезы не получили эксперим.
подтверждения. Наиб. признанием пользуется
хемиосмотич. концепция сопряжения,
предложенная в 1961 П. Митчеллом. Согласно
этой теории, своб. энергия транспорта
электронов
в дыхат. цепи затрачивается на перенос
из митохондрий
через митохондриальную мембрану
на ее наружную сторону ионов
Н+.
В результате на мембране
возникает разность электрич. потенциалов
АТФ
А ~ В-высокоэнергетич. интермедиат
Предполагалось, что А ~ В - хим. соед. с
макроэргич. связью, напр. фосфорилир.
фермент
дыхат. цепи (хим. гипотеза сопряжения),
или напряженная конформация
к.-л. белка,
участвующего в окислительном
фосфорилировании
(конформац. гипотеза сопряжения). Однако
эти гипотезы не получили эксперим.
подтверждения. Наиб. признанием пользуется
хемиосмотич. концепция сопряжения,
предложенная в 1961 П. Митчеллом. Согласно
этой теории, своб. энергия транспорта
электронов
в дыхат. цепи затрачивается на перенос
из митохондрий
через митохондриальную мембрану
на ее наружную сторону ионов
Н+.
В результате на мембране
возникает разность электрич. потенциалов
![]() и
разность хим. активностей
ионов
Н+
и
разность хим. активностей
ионов
Н+
![]() (внутри
митохондрий
рН выше, чем снаружи). В сумме эти
компоненты дают трансмембранную разность
электрохим. потенциалов ионов
водорода
(внутри
митохондрий
рН выше, чем снаружи). В сумме эти
компоненты дают трансмембранную разность
электрохим. потенциалов ионов
водорода
![]() между
матриксом митохондрий
и внеш. водной фазой, разделенными
мембраной.
Энергия
между
матриксом митохондрий
и внеш. водной фазой, разделенными
мембраной.
Энергия
![]() ,
выделяющаяся при движении протонов
внутрь митохондрий
по электрич. полю в сторону меньшей их
концентрации,
используется
АТФ-синтетазой для
синтеза
АТФ.
Т. обр., схему окислительного
фосфорилирования,
согласно этой концепции, можно представить
в след. виде:Перенос электронов
(дыхание)
,
выделяющаяся при движении протонов
внутрь митохондрий
по электрич. полю в сторону меньшей их
концентрации,
используется
АТФ-синтетазой для
синтеза
АТФ.
Т. обр., схему окислительного
фосфорилирования,
согласно этой концепции, можно представить
в след. виде:Перенос электронов
(дыхание)
![]() АТФ
АТФ
Сопряжение
окисления
и фосфорилирования
через![]() позволяет объяснить, почему окислительное
фосфорилирование,
в отличие от гликолитич. ("субстратного")
фосфорилирования,
протекающего в р-ре, возможно лишь в
замкнутых мембранных структурах, а
также почему все воздействия, снижающие
электрич. сопротивление и увеличивающие
протонную проводимость мембраны,
подавляют ("разобщают") окислительное
фосфорилирование.
Энергия
позволяет объяснить, почему окислительное
фосфорилирование,
в отличие от гликолитич. ("субстратного")
фосфорилирования,
протекающего в р-ре, возможно лишь в
замкнутых мембранных структурах, а
также почему все воздействия, снижающие
электрич. сопротивление и увеличивающие
протонную проводимость мембраны,
подавляют ("разобщают") окислительное
фосфорилирование.
Энергия
![]() ,
помимо синтеза
АТФ,
может непосредственно использоваться
клеткой
для др. целей - транспорта метаболитов,
движения (у бактерий), восстановления
нико-тинамидных коферментов
и др.
,
помимо синтеза
АТФ,
может непосредственно использоваться
клеткой
для др. целей - транспорта метаболитов,
движения (у бактерий), восстановления
нико-тинамидных коферментов
и др.
Показано, что окислительное фосфорилирование сопряжено с переносом электронов по цепи дыхательных ферментов, встроенных во внутреннюю мембрану митохондрий. Электроны поступают в дыхательную цепь от восстановленного НАД (или НАДФ) и через кофермент Q последовательно передаются от соединений с более отрицательным окислительно-восстановительным потенциалом к соединениям с более положительным потенциалом. Перенос электронов по цепи завершается восстановлением O2 с помощью цитохромоксидазы. Таким образом, процесс окисления субстрата кислородом опосредован серией окислительно-восстановительных реакций; в результате энергия, запасённая в молекуле окисляемого субстрата, освобождается небольшими порциями, что позволяет клетке использовать её более полно. Утилизация высвобождаемой энергии происходит в так называемых пунктах энергетического сопряжения. Синтез АТФ осуществляется ферментным комплексом — АТФ-синтетазой, который может катализировать и обратную реакцию. Эффективность окислительного фосфорилирования оценивают с помощью коэффициента фосфорилирования Фн/O — отношения числа молекул неорганического фосфата, связанного при фосфорилировании АДФ, к поглощённому O2; величина этого коэффициента зависит от окисляемого субстрата, физиологического состояния клеток и состава окружающей клеток среды.
Упрощённая схема цепи дыхательных ферментов, локализованных в митохондриях. Перенос электронов по цепи на трёх этапах (так называемым пунктах сопряжения) сопровождается запасанием выделяющейся энергии в форме электрохимического градиента ионов водорода, далее энергия расходуется для синтеза АТФ.

Работа АТФ-синтазы
Н+-транслоцирующая АТФ-синтаза состоит из двух частей: встроенного в мембрану протонного канала (F0) из по меньшей мере 13 субъединиц и каталитической субъединицы (F1), выступающей в матрикс. «Головка» каталитической части образована тремя α- и тремя β-субъединицами, между которыми расположены три активных центра. "Ствол" структуры образуют полипептиды F0-части и γ-, δ- и ε-субъединиц головки.
Каталитический цикл подразделяется на три фазы, каждая из которых проходит поочередно в трех активных центрах. Вначале идет связывание АДФ (ADP) и Ρi (1), затем образуется фосфоангидридная связь (2) и, наконец, освобождается конечный продукт реакции (3). При каждом переносе протона через белковый канал F0 в матрикс все три активных центра катализируют очередную стадию реакции. Предполагается, что энергия протонного транспорта прежде всего расходуется на поворот γ-субъединицы, в результате которого циклически изменяются конформации α- и β-субъединиц.
Процесс окислительного фосфорилирования осуществляется пятым комплексом дыхательной цепи митохондрий — Протонная АТФ-синтаза, состоящая из 9 субъединиц 5 типов:
