
- •Содержание
- •Билет №1
- •2. Определение катаболизма. Катаболизм и анаболизм. Стадии катаболизма биомолекул в организме.
- •Билет№2.
- •1.Ферменты. Специфичность ферментов. Активный центр фермента.
- •2.Экзергонические и эндергонические биохимические реакции. Роль атф и других макроэргических фосфатов в сопряжении экзергонических процессов и эндергонических процессов.
- •3.Пути внутриклеточного метаболизма глюкозы. Гликолиз и глюконеогенез. Обратимые и необратимые реакции.
- •Билет №3
- •1.Регуляция активности ферментов. Проферменты. Изоферменты. Ингибиторы ферментов.
- •2.Реакции биологичемкого окисления.Типы реакций( дегидрогеназные, оксидазные, оксигеназные. Их биологическое значение.
- •3 Цитохромы Катализируют окисление веществ путем отдачи электронов Гемовое железо в одном из цитохромов имеется так же атом меди.
- •Билет№4
- •1.Ферментативный катализ
- •2.Митохондриальный транспорт
- •3.Аэробное окисление пирувата (окислительное декарбоксилирование пировиноградной кты).
- •Билет№5
- •1.Кинетика ферментативного катализа. Уравнение Михаэлиса-Ментен. Уравнение Лайнуивера-Берка.
- •2.Окислительное фосфорилирование. Пункты сопряжения окисления и фосфорилирования. Атф-синтетаза митохондрий.
- •3 Субъединицы (γ,δ,ε) способствуют целостности атф-синтазы
- •3.Полное окисление глюкозы. Энергетический баланс
- •Билет№6
- •1.Аллостерические ферменты. Ингибиторы и активаторы аллостерических ферментов. Аллостерические центры.
- •Деградация жирных кислот: β-окисление
- •Билет№7
- •1.Опять ферменты
- •2. Ингибиторы и разъединители транспорта электронов окислительного фосфорилирования
- •3.Глюконеогенез
- •Билет №8
- •1. Витамины
- •2. Микросомальная цепь транспорта электронов
- •3. Глюкозолактонный цикл
- •1. Витамин в2
- •3.Гипергликемия
- •Билет 10
- •Билет 11
- •1. Витамин в6(пиридоксин, пиридоксаль, пиридоксамин)
- •3 Существуют три источника аминокислот в клетке – поступление из крови, распад собственных внутриклеточных белков и синтез заменимых аминокислот.
- •Билет 12
- •1.Биотин
- •2. Нарушение обмена гликогена
- •3. Существуют три источника аминокислот в клетке – поступление из крови, распад собственных внутриклеточных белков и синтез заменимых аминокислот.
- •Билет 13. Фолиевая кислота. Биологическая роль. Пути поступления в организм. Коферментная функция.
- •2.Катаболизм триацилглицеролов. Реакции, механизм регуляции активности триглицеридлипазы. Нейрогуморальная регуляция липолиза (адреналин, глюкагон, инсулин).
- •3.Трансаминирование амк. Аминотрансферазы. Отдельные аминотрансферазы. Реакции. Биохимическое значение трансаминирования амк.
- •Билет 14
- •1.Витамин в12. Биологическая роль. Пути попадания в организм. Коферментная функция.
- •3.Пути превращения аммиака в организме человека. Механизмы обезвреживания аммиака.
- •Билет №15
- •1.Витамин с.
- •2.Окисление пальмитиновой кослоты.
- •3.Биосинтез мочевины.
- •Билет №16
- •1.Витамин а.
- •2.Окисление ненасыщенных жирных кислот.
- •3.Превращение безазотистого скелета ак
- •Билет №17
- •1.Витамин д
- •2. Биосинтез высших жирных кислот.
- •3. Метаболизм ак с разветвленной цепью.
- •Билет №25 Репликация днк
- •Свойства процесса репликации:
- •Желчные кислоты
- •Стероидные гормоны
- •2.Специализированные пути метаболизма цикл. А,к- фенилаланина и тирозина.. Заболевания, связанные с нарушением обмена фенилаланина и тирозина.
- •3.Биосинтез гема
- •Билет 19
- •2.Биосинтез пуриновых нуклеотидов
- •3.Основные закономерности генетического кода. Адапторная гипотеза ф. Крика и её развитие в wobble-гипотезе.
- •Билет №20
- •2. Кинетика ферменативного катализа. График зависимости скорости ферментативной реакции от концентрации субстрата при постоянной концентрации фермента.
- •Билет №21
- •Транскрипционные факторы: Механизмы действия тф , связавающиеся с днк, могут влиять на транскрипцию генов через несколько механизмов:
- •Билет№22
- •Билет 23
- •2. Полное окисление глюкозы. Энергетический баланс полного окисления глюкозы.
- •Билет№24
- •1.Антибиотические вещества, подавляющие синтез белка
- •24.2 Функционирование малат-аспартатного и глицерофосфатного шунта.
- •Билет №26
- •3. Окисление капроновой кислоты
- •Билет №27
- •Репликация
- •Билет 28
- •Билет29
- •29.2.Метаболизм аминокислот
- •Билет №30
- •1.Особенности молекулярной организации и экспрессии генома эукариот (экзоны, интроны, сплайсинг)
- •2.Образование кетоновых тел и их утилизация.
- •3.Цикл трикарбоновых кислот. Реакции
Билет№22
1.Собственно трансляция происходит в рибосомах и включает три стадии: 1. Инициация: образование инициирующего комплекса, который включает метионин-тРНКи (инициирующая), мРНК и рибосомальные белки. Комплекс состоит из 40S и 60S субъединиц, объединенных в 80S-рибосому. Целостная рибосома имеет аминоацильный (А-сайт) и пептидильный участок (Р-сайт). Первый отвечает за связывание аминоацил-тРНК, а второй – за связывание растущей полипептидной цепи. В состав инициирующего комплекса входит мРНК, которая на 5’-конце имеет 7-метилгуанозиновый «кэп». Начиная с кэпа, рибосома движется по мРНК и сканирует один кодон за другим, пока не наткнется на инициирующий (стартовый) кодон AUG. мРНК ориентируется таким образом, чтобы напротив пептидильного сайта рибосомы размещался инициирующий кодон AUG (кодирует метионин). Инициирующая метиониновая тРНК (мет-тРНКи) поставляет в рибосому первую аминокислоту – метионин, который становится N-концевой аминокислотой для большинства эукариотических белков (у прокариот это формилметионин). Для формирования инициирующего комплекса необходимо присутствие фактора eIF2 и более десяти других факторов инициации трансляции (eIF1, eIF3, eIF4, eIF6 и других). Роль факторов инициации различна. Так, фактор eIF3 препятствует объединению субъединиц рибосом в отсутствии мРНК; фактор eIF2 распознает инициирующую мет-тРНКи и поставляет энергию для инициации, расщепляя ГТФ; фактор eIF4A раскручивает мРНК и позволяет рибосоме двигаться по ней; фактор eIF4E распознает кэп. Благодаря взаимодействию между рРНК и мРНК последняя правильно фиксируется на рибосомных частицах, что способствует инициации. 2. Элонгация. Суть элонгации заключается в возникновении пептидных связей между остатками аминокислот с образованием полипептидной цепи, в которой последовательность аминокислот отвечает последовательности кодонов в мРНК. Элонгации нуждается в энергии ГТФ и факторах элонгации – EF1 и EF2. Элонгация начинается после того, как мет-тРНКи займет пептидильний центр рибосомы. В свободный аминоацильний сайт рибосомы могут поступать любые аминоацил-тРНК, но остается в нем лишь та, антикодон которой комплементарен кодону на мРНК. В результате метионил-тРНК и вторая аминоацил-тРНК сближаются между собой, а пептидилтрансфераза (точнее пептидилтрансферазный центр), катализирует образование пептидной связи между ними. Заметим, что пептидилтрансферазный центр есть рибозимом и образуется как рибосомальной РНК (28S рРНК), так и белками большой субъединицы рибосом. После образования пептидной связи со второй аминокислотой высвобождается мет тРНКи и происходит транслокация (перемещение) образованного дипептида (дипептидил-тРНК) из аминоацильного сайта в пептидильный. Процессу нужна энергия ГТФ и фактор элонгации ЕF2. В результате транслокации освобождается аминоацильний сайт, в который поступает новая аа-тРНК, антикодон которой комплементарен очередному кодону на мРНК, а пептидилтрансфераза наращивает цепь белка еще на одну аминокислоту. Этот конвеер работает непрерывно до того момента, пока на мРНК не появятся терминирующие кодоны (UAA, UGA, UAG). 3.Терминация трансляции. Появление терминирующих кодонов на мРНК способствует завершению трансляции, поскольку этим кодонам не отвечает ни одна из аа-тРНК. С этими кодонами связываются факторы терминации (eRF1 и eRF2), которые стимулируют гидролазную активность пептидильного центра. От новообразованного пептида отщепляется тРНК, и он отделяется от пептидильного центра. Рибосома диссоциирует на две субъединицы, а мРНК гидролизуется на свободные мононуклеотиды. Полисомы (полирибосомы). В трансляции мРНК могут принимать участие несколько рибосом. Как только первая рибосома покидает инициирующий кодон на мРНК, он становится доступным для другой рибосомы и т.д. Поэтому на одну цепь мРНК может быть нанизано 5- 6 рибосом. Конвеерный характер трансляции существенно повышает скорость синтеза белка. Ингибиторы трансляции у прокариот: стрептомицин блокирует стадию инициации; тетрациклин - связывание аминоацил-тРНК с рибосомами, хлорамфеникол - пептидилтрансферазную активность, эритромицин - процесс транслокации. Циклогексимид тормозит пептидилтрансферазную активность у эукариот, а пуромицин конкурирует с аминоацил-тРНК за аминоацильний сайт рибосомы. Ингибитором трансляции является дифтерийный токсин. А-фрагмент токсина имеет активность АДФ-рибозилтрансферазы и переносит АДФ-рибозу с НАД на фактор элонгации eEF2, инактивируя его. Интерфероны – белки, которые продуцируются лимфоцитами при заражении организма вирусами, активируют протеинкиназы, фосфорилирующие фактор инициации eIF2 и инактивируют его. Блокируется синтез вирусных и клеточных белков, наступает гибель инфицированных клеток, чем предупреждается распространение вируса.
2.ЦТК
Первая реакция ацетильная группа ацетил-КоА конденсируется с оксалоацетатом, в результате чего образуется лимонная кислота:
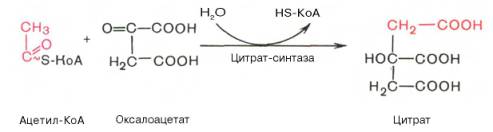
В
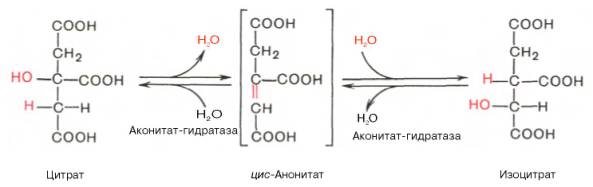
результате второй реакции
образовавшаяся лимонная
кислота подвергается
дегидратированию с образованием
цис-аконитовой кислоты,
которая, присоединяя молекулу
воды,
переходит в изолимонную
кислоту (изоцитрат).
Третья реакция, по-видимому, лимитирует скорость цикла Кребса. Изолимонная кислота дегидрируется в присутствии НАД-зависимой изо-цитратдегидрогеназы.
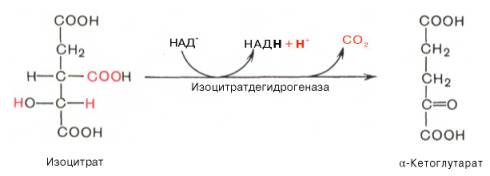
В ходе изоцитратдегидрогеназной реакции изолимонная кислота одновременно декарбоксилируется. НАД-зависимая изоцитратдегидрогеназа является аллостерическим ферментом, которому в качестве специфического активатора необходим АДФ. Кроме того, фермент для проявления своей активности нуждается в ионах Mg2+или Мn2+.
Во
время четвертой реакции
происходит окислительное декарбокси-лирование
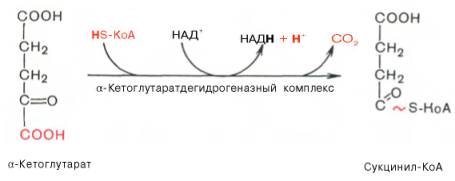
Пятая реакция происходит образование высокоэргической фосфатной связи ГТФ за счет высокоэргической тиоэфирной связи сукцинил-КоА:
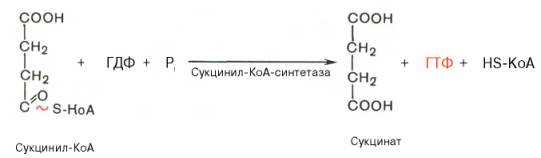
В результате шестой реакции сукцинат дегидрируется в фумаровую кислоту.
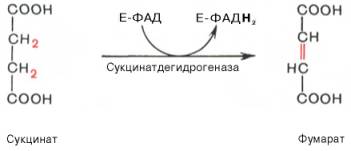
Седьмая реакция гидратируется
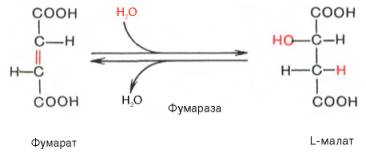
8 реакция

Энергетический баланс 1 молекулы ацетил-КоА: 3НАДН = 9 молекул АТФ, ФАДН2 =2 молекулы АТФ, в реакции субстратного фосфорилирования обр. ГТФ = 1 АТФ. Итого обр. 12 молекул АТФ.
ЦТК выполняет следующие биохимические функции: Интергративная(обьеденяет катаболические пути углеводов, липидов и белков), амфиболическая (выполняет как катаболическую, так и анаболическую функции (все р-ции ЦТК), энергетическая (синтез АТФ), водорододонорная (генератор водорода для дыхательной цепи). Значение: цитрат участвует в синтезе ЖК, альфа-КГ участвует в образовании глутамата, пуриновых оснований, пролина и др., Сукцинил-КоА участвует в синтезе гемма, оксалоацетат – обр. аспарагин – пиримидиновые основания. , оксалоацетат- фосфорный пируват – серин, глицин, цистеин, триптофан. (анаболическая роль)
Как правило работа цикла Кребса не прерывается за счёт анаплеротических реакций, которые пополняют цикл субстратами: Пируват + СО2 + АТФ = Оксалоацетат(субстрат Цикла Кребса) + АДФ + Фн.
3.Глицеролфосфатного челночного механизма. Цитоплазматический НАДН сначала реагирует с цитоплазматическим дигидроксиацетонфосфатом, образуя глицерол-3-фосфат. Реакция катализируется НАД-зависимой цитоплазматической глицерол-3-фосфат-дегидрогеназой:Дигидроксиацетонфосфат + НАДН + Н+ <=> Глицерол-3-фосфат + НАД+. Образовавшийся глицерол-3-фосфат легко проникает через митохондриальную мембрану. Внутри митохондрии другая (митохондриальная)глицерол-3-фосфат-дегидрогеназа (флавиновый фермент) снова окисляетглицерол-3-фосфат до диоксиацетонфосфата: Глицерол-3-фосфат + ФАД <=> Диоксиацетонфосфат + ФАДН2.
Восстановленный флавопротеин (фермент-ФАДН2) вводит на уровне KoQ приобретенные им электроны в цепь биологического окисления и сопряженного с ним окислительного фосфорилирования, а диоксиацетонфосфат выходит из митохондрий в цитоплазму и может вновь взаимодействовать с цитоплазматическим НАДН + Н+. Таким образом, пара электронов (из одной молекулы цитоплазматического НАДН + Н+), вводимая в дыхательную цепь с помощью глицеролфосфатного челночного механизма, дает не 3, а 2 АТФ. В дальнейшем было показано, что с помощью данного челночного механизма лишь в скелетных мышцах и мозге осуществляется перенос восстановленных эквивалентов от цитозольного НАДН + Н+ в митохондрии.
В клетках печени, почек и сердца действует более сложная малат-аспартатная челночная система. Действие такого челночного механизма становится возможным благодаря присутствию малатдегидрогеназы и аспартатаминотрансферазы как в цитозоле, так и в митохондриях. Установлено, что от цитозольного НАДН + Н+ восстановленные эквиваленты сначала при участии фермента малатдегидрогеназы переносятся на цитозольный оксалоацетат. В результате образуется малат, который с помощью системы, транспортирующей дикарбоновые кислоты, проходит через внутреннюю мембрану митохондрии в матрикс. Здесь малат окисляется в оксалоацетат, а матриксный НАД+ восстанавливается в НАДН + Н+, который может теперь передавать свои электроны в цепь дыхательных ферментов, локализованную на внутренней мембране митохондрии. В свою очередь образовавшийся оксалоацетат в присутствии глутамата и фермента Аспартатаминотрансфераза вступает в реакцию трансаминирования. Образующиеся аспарат и α-кетоглутарат с помощью специальных транспортных систем способны проходить через мембрану митохондрий.
Транспортирование в цитозоле регенерирует оксалоацетат, что вызывает к действию следующий цикл. В целом процесс включает легкообратимые реакции, происходит без потребления энергии, ≪движущей силой≫ его является постоянное восстановление НАД+ в цитозоле глицеральдегид-3-фосфатом, образующимся при катаболизме глюкозы.
