
- •Содержание
- •Билет №1
- •2. Определение катаболизма. Катаболизм и анаболизм. Стадии катаболизма биомолекул в организме.
- •Билет№2.
- •1.Ферменты. Специфичность ферментов. Активный центр фермента.
- •2.Экзергонические и эндергонические биохимические реакции. Роль атф и других макроэргических фосфатов в сопряжении экзергонических процессов и эндергонических процессов.
- •3.Пути внутриклеточного метаболизма глюкозы. Гликолиз и глюконеогенез. Обратимые и необратимые реакции.
- •Билет №3
- •1.Регуляция активности ферментов. Проферменты. Изоферменты. Ингибиторы ферментов.
- •2.Реакции биологичемкого окисления.Типы реакций( дегидрогеназные, оксидазные, оксигеназные. Их биологическое значение.
- •3 Цитохромы Катализируют окисление веществ путем отдачи электронов Гемовое железо в одном из цитохромов имеется так же атом меди.
- •Билет№4
- •1.Ферментативный катализ
- •2.Митохондриальный транспорт
- •3.Аэробное окисление пирувата (окислительное декарбоксилирование пировиноградной кты).
- •Билет№5
- •1.Кинетика ферментативного катализа. Уравнение Михаэлиса-Ментен. Уравнение Лайнуивера-Берка.
- •2.Окислительное фосфорилирование. Пункты сопряжения окисления и фосфорилирования. Атф-синтетаза митохондрий.
- •3 Субъединицы (γ,δ,ε) способствуют целостности атф-синтазы
- •3.Полное окисление глюкозы. Энергетический баланс
- •Билет№6
- •1.Аллостерические ферменты. Ингибиторы и активаторы аллостерических ферментов. Аллостерические центры.
- •Деградация жирных кислот: β-окисление
- •Билет№7
- •1.Опять ферменты
- •2. Ингибиторы и разъединители транспорта электронов окислительного фосфорилирования
- •3.Глюконеогенез
- •Билет №8
- •1. Витамины
- •2. Микросомальная цепь транспорта электронов
- •3. Глюкозолактонный цикл
- •1. Витамин в2
- •3.Гипергликемия
- •Билет 10
- •Билет 11
- •1. Витамин в6(пиридоксин, пиридоксаль, пиридоксамин)
- •3 Существуют три источника аминокислот в клетке – поступление из крови, распад собственных внутриклеточных белков и синтез заменимых аминокислот.
- •Билет 12
- •1.Биотин
- •2. Нарушение обмена гликогена
- •3. Существуют три источника аминокислот в клетке – поступление из крови, распад собственных внутриклеточных белков и синтез заменимых аминокислот.
- •Билет 13. Фолиевая кислота. Биологическая роль. Пути поступления в организм. Коферментная функция.
- •2.Катаболизм триацилглицеролов. Реакции, механизм регуляции активности триглицеридлипазы. Нейрогуморальная регуляция липолиза (адреналин, глюкагон, инсулин).
- •3.Трансаминирование амк. Аминотрансферазы. Отдельные аминотрансферазы. Реакции. Биохимическое значение трансаминирования амк.
- •Билет 14
- •1.Витамин в12. Биологическая роль. Пути попадания в организм. Коферментная функция.
- •3.Пути превращения аммиака в организме человека. Механизмы обезвреживания аммиака.
- •Билет №15
- •1.Витамин с.
- •2.Окисление пальмитиновой кослоты.
- •3.Биосинтез мочевины.
- •Билет №16
- •1.Витамин а.
- •2.Окисление ненасыщенных жирных кислот.
- •3.Превращение безазотистого скелета ак
- •Билет №17
- •1.Витамин д
- •2. Биосинтез высших жирных кислот.
- •3. Метаболизм ак с разветвленной цепью.
- •Билет №25 Репликация днк
- •Свойства процесса репликации:
- •Желчные кислоты
- •Стероидные гормоны
- •2.Специализированные пути метаболизма цикл. А,к- фенилаланина и тирозина.. Заболевания, связанные с нарушением обмена фенилаланина и тирозина.
- •3.Биосинтез гема
- •Билет 19
- •2.Биосинтез пуриновых нуклеотидов
- •3.Основные закономерности генетического кода. Адапторная гипотеза ф. Крика и её развитие в wobble-гипотезе.
- •Билет №20
- •2. Кинетика ферменативного катализа. График зависимости скорости ферментативной реакции от концентрации субстрата при постоянной концентрации фермента.
- •Билет №21
- •Транскрипционные факторы: Механизмы действия тф , связавающиеся с днк, могут влиять на транскрипцию генов через несколько механизмов:
- •Билет№22
- •Билет 23
- •2. Полное окисление глюкозы. Энергетический баланс полного окисления глюкозы.
- •Билет№24
- •1.Антибиотические вещества, подавляющие синтез белка
- •24.2 Функционирование малат-аспартатного и глицерофосфатного шунта.
- •Билет №26
- •3. Окисление капроновой кислоты
- •Билет №27
- •Репликация
- •Билет 28
- •Билет29
- •29.2.Метаболизм аминокислот
- •Билет №30
- •1.Особенности молекулярной организации и экспрессии генома эукариот (экзоны, интроны, сплайсинг)
- •2.Образование кетоновых тел и их утилизация.
- •3.Цикл трикарбоновых кислот. Реакции
Желчные кислоты
ЖЕЛЧНЫЕ КИСЛОТЫ, монокарбоновые гидроксикислоты, относящиеся к классу стероидов. Почти все желчные кислоты - производные прир. холановой к-ты, синтезируемой из холестерина в печени.
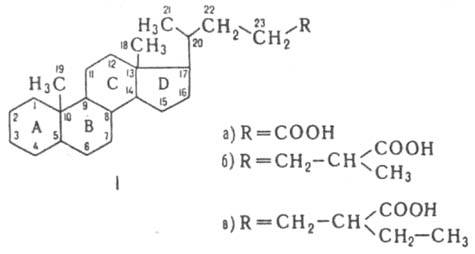
Сначала синтезируются две первичные желчные кты – холевая и хенодезоксихолевая. Потом вторичные: дезоксихолевая и литохолевая. Функционируют они в виде конъюгантов с глицином или таурином. Конъюганты в печени образуются в две стадии:
R-COOH+ATP+KoASH = R – CO~SKoA+AMP+PP
R-CO~SKoA+H2N-CH2-COOH(глицин) = R-CO-NH-CH2-COOH+KoASH
Или
R-CO~SKoA+ H2N-CH2-CH2-SO3H(таурин) = R-CO-NH-CH2-CH2-SO3H+KoASH
Желчные кислоты эмульгируют жиры.
Стероидные гормоны
Общим предшественником стероидных гормонов является холестерин.
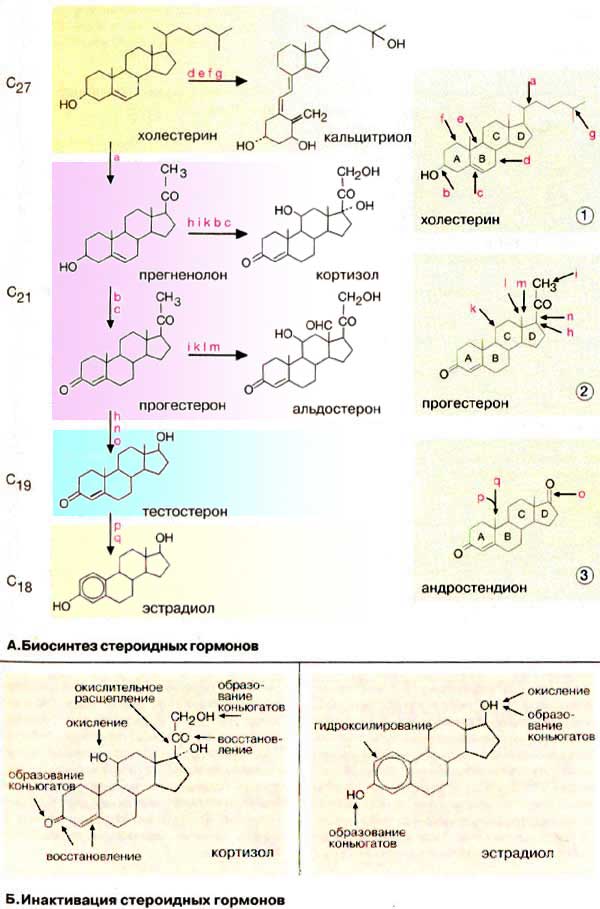
Путь биосинтеза. Биосинтез каждого гормона состоит из множества последовательных ферментативных реакций. В качестве примера рассмотрим биосинтез прогестерона (А) см. рис. 397). Биосинтез начинается с расщепления боковой цепи холестерина между С-20 и С-22 (а). Стероидное соединение с укороченной боковой цепью носит название прегненолон. Последующие стадии, окисление гидроксигруппы при С-3 (b) и сдвиг двойной связи от С-5 к С-4 (с) приводят к образованию прогестерона.
Приведенные на схеме стероиды объединены в подгруппы по числу углеродных атомов. Холестерин и кальцитриол являются С27-стероидами. Соединения с укороченной на 6 атомов углерода боковой цепью, прогестерон, кортизол и альдостерон, составляют группу С21-стероидов. В ходе биосинтеза тестостерон полностью утрачивает боковую цепь и поэтому его относят к С19-стероидам. При биосинтезе эстрадиола на стадии образования ароматического цикла теряется ангулярная метильная группа и, следовательно, эстрадиол является С18-стероидом.
В процессе биосинтеза кальцитриол подвергается фотохимической реакции раскрытия кольца В. Поэтому его относят к «секостероидам». Однако по своим биохимическим свойствам он является типичным стероидным гормоном.
2.Специализированные пути метаболизма цикл. А,к- фенилаланина и тирозина.. Заболевания, связанные с нарушением обмена фенилаланина и тирозина.
Фенилаланин относится к незаменимым аминокислотам, поскольку ткани животных не обладают способностью синтезировать его бензольное кольцо. В то же время тирозин полностью заменим при достаточном поступлении фенилаланина с пищей. Объясняется это тем, что основной путь превращения фенилаланина начинается с его окисления (точнее, гидрокси-лирования) в тирозин (рис. 12.6). Реакция гидроксилирования катализируется специфической фенилаланин-4-монооксигеназой, которая в качестве кофермента содержит, как все другие гидроксилазы, тетрагидро-биоптерин. Блокирование этой реакции, наблюдаемое при нарушении синтеза фенилаланин-4-монооксигеназы в печени, приводит к развитию тяжелой наследственной болезни – фенилкетонурии (фенилпировиноградная олигофрения). В процессе трансаминирования тирозин превращается в n-оксифенилпировиноградную кислоту, которая под действием специфической оксидазы подвергается окислению, декарбоксилированию, гидро-ксилированию и внутримолекулярному перемещению боковой цепи с образованием гомогентизиновой кислоты; эта реакция требует присутствия аскорбиновой кислоты, роль которой пока не выяснена. Дальнейшее превращении егомогентизиновой кислоты в малеилацетоуксусную кислоту катализируется оксидазой гомогентизиновой кислоты. Малеилацетоуксус-ная кислота под действием специфической изомеразы в присутствии глу-татиона превращается в фумарилацетоуксусную кислоту, подвергающуюся гидролизу с образованием фумаровой и ацетоуксусной кислот. Фенилаланин и тирозин являются также предшественниками меланинов. В этом важном биологическом процессе, обеспечивающем пигментацию кожи, глаз, волос, активное участие принимает фермент тирозиназа.
Фенилкетонурия (фенилпировиноградная олигофрения, болезнь Феллин-га) — одно из наиболее частых наследственных заболеваний, чаще обусловлено недостаточностью фенилаланин гидроксилазы (261600, 12q24.1); при отсутствии своевременного лечения приводит к тяжёлой умственной отсталости. Тип наследования аутосомно-рецессивный. Больные гомозиготны по гену фенилкетонурии, а их родители гетерозиготны.
Вследствие дефекта гена фенилаланин гидроксилазы (ФАГ-ген) развивается недостаточность фермента, и как следствие наступает блок в нормальном превращении фенилаланина в аминокислоту тирозин . Фенилаланин накапливается в организме и его концентрация в крови повышается в 10-100 раз. Далее он превращается в фенилпировиноградную кислоту, оказывающую токсическое влияние на нервную систему. Накопление фенилаланина в организме происходит постепенно, поэтому клиническая картина развивается медленно. В связи с этим очень важна ранняя диагностика фенилкетонурии
Алкаптонурия возникает вследствие мутации гена, кодирующего синтез оксидазы гомогентезиновой кислоты. Данная патология характеризуется аутосомно-рецессивным типом наследования. Алкаптонурией чаще болеют мужчины. Ген оксидазы гомогетинзиновой кислоты человека (HGD) локализован на длинном плече 3 хромосомы человека . В нормальных условиях гомогентезиновая кислота — промежуточный продукт распада тирозина и фенилаланина — переводится в малеилацетоуксусную кислоту, из которой в конечном счёте образуются фумаровая и ацетоуксусная кислоты, вступающие в другие биохимические циклы. Из-за дефекта фермента этот процесс тормозится, и остающаяся в избытке гомогентезиновая кислота превращается полифенолоксидазой в хиноновый полифенол (алкаптон или бензохинонацетат), который и выводится почками. Не полностью экскретируемый мочой алкаптон откладывается в хрящевой и другой соединительной ткани, обусловливая их потемнение и повышенную хрупкость. Чаще всего вперёд появляется пигментация склер и ушных хрящей.
.
