
- •Содержание
- •Билет №1
- •2. Определение катаболизма. Катаболизм и анаболизм. Стадии катаболизма биомолекул в организме.
- •Билет№2.
- •1.Ферменты. Специфичность ферментов. Активный центр фермента.
- •2.Экзергонические и эндергонические биохимические реакции. Роль атф и других макроэргических фосфатов в сопряжении экзергонических процессов и эндергонических процессов.
- •3.Пути внутриклеточного метаболизма глюкозы. Гликолиз и глюконеогенез. Обратимые и необратимые реакции.
- •Билет №3
- •1.Регуляция активности ферментов. Проферменты. Изоферменты. Ингибиторы ферментов.
- •2.Реакции биологичемкого окисления.Типы реакций( дегидрогеназные, оксидазные, оксигеназные. Их биологическое значение.
- •3 Цитохромы Катализируют окисление веществ путем отдачи электронов Гемовое железо в одном из цитохромов имеется так же атом меди.
- •Билет№4
- •1.Ферментативный катализ
- •2.Митохондриальный транспорт
- •3.Аэробное окисление пирувата (окислительное декарбоксилирование пировиноградной кты).
- •Билет№5
- •1.Кинетика ферментативного катализа. Уравнение Михаэлиса-Ментен. Уравнение Лайнуивера-Берка.
- •2.Окислительное фосфорилирование. Пункты сопряжения окисления и фосфорилирования. Атф-синтетаза митохондрий.
- •3 Субъединицы (γ,δ,ε) способствуют целостности атф-синтазы
- •3.Полное окисление глюкозы. Энергетический баланс
- •Билет№6
- •1.Аллостерические ферменты. Ингибиторы и активаторы аллостерических ферментов. Аллостерические центры.
- •Деградация жирных кислот: β-окисление
- •Билет№7
- •1.Опять ферменты
- •2. Ингибиторы и разъединители транспорта электронов окислительного фосфорилирования
- •3.Глюконеогенез
- •Билет №8
- •1. Витамины
- •2. Микросомальная цепь транспорта электронов
- •3. Глюкозолактонный цикл
- •1. Витамин в2
- •3.Гипергликемия
- •Билет 10
- •Билет 11
- •1. Витамин в6(пиридоксин, пиридоксаль, пиридоксамин)
- •3 Существуют три источника аминокислот в клетке – поступление из крови, распад собственных внутриклеточных белков и синтез заменимых аминокислот.
- •Билет 12
- •1.Биотин
- •2. Нарушение обмена гликогена
- •3. Существуют три источника аминокислот в клетке – поступление из крови, распад собственных внутриклеточных белков и синтез заменимых аминокислот.
- •Билет 13. Фолиевая кислота. Биологическая роль. Пути поступления в организм. Коферментная функция.
- •2.Катаболизм триацилглицеролов. Реакции, механизм регуляции активности триглицеридлипазы. Нейрогуморальная регуляция липолиза (адреналин, глюкагон, инсулин).
- •3.Трансаминирование амк. Аминотрансферазы. Отдельные аминотрансферазы. Реакции. Биохимическое значение трансаминирования амк.
- •Билет 14
- •1.Витамин в12. Биологическая роль. Пути попадания в организм. Коферментная функция.
- •3.Пути превращения аммиака в организме человека. Механизмы обезвреживания аммиака.
- •Билет №15
- •1.Витамин с.
- •2.Окисление пальмитиновой кослоты.
- •3.Биосинтез мочевины.
- •Билет №16
- •1.Витамин а.
- •2.Окисление ненасыщенных жирных кислот.
- •3.Превращение безазотистого скелета ак
- •Билет №17
- •1.Витамин д
- •2. Биосинтез высших жирных кислот.
- •3. Метаболизм ак с разветвленной цепью.
- •Билет №25 Репликация днк
- •Свойства процесса репликации:
- •Желчные кислоты
- •Стероидные гормоны
- •2.Специализированные пути метаболизма цикл. А,к- фенилаланина и тирозина.. Заболевания, связанные с нарушением обмена фенилаланина и тирозина.
- •3.Биосинтез гема
- •Билет 19
- •2.Биосинтез пуриновых нуклеотидов
- •3.Основные закономерности генетического кода. Адапторная гипотеза ф. Крика и её развитие в wobble-гипотезе.
- •Билет №20
- •2. Кинетика ферменативного катализа. График зависимости скорости ферментативной реакции от концентрации субстрата при постоянной концентрации фермента.
- •Билет №21
- •Транскрипционные факторы: Механизмы действия тф , связавающиеся с днк, могут влиять на транскрипцию генов через несколько механизмов:
- •Билет№22
- •Билет 23
- •2. Полное окисление глюкозы. Энергетический баланс полного окисления глюкозы.
- •Билет№24
- •1.Антибиотические вещества, подавляющие синтез белка
- •24.2 Функционирование малат-аспартатного и глицерофосфатного шунта.
- •Билет №26
- •3. Окисление капроновой кислоты
- •Билет №27
- •Репликация
- •Билет 28
- •Билет29
- •29.2.Метаболизм аминокислот
- •Билет №30
- •1.Особенности молекулярной организации и экспрессии генома эукариот (экзоны, интроны, сплайсинг)
- •2.Образование кетоновых тел и их утилизация.
- •3.Цикл трикарбоновых кислот. Реакции
Билет 14
1.Витамин в12. Биологическая роль. Пути попадания в организм. Коферментная функция.
Витаминами B12 называют группу кобальтсодержащих биологически активных веществ, называемых кобаламинами. К ним относят собственно цианокобаламин — продукт, получаемый при химической очистке витамина цианидами, гидроксикобаламин и две коферментные формы витамина B12: метилкобаламин и 5-дезоксиаденозилкобаламин. B12 имеет самую сложную по сравнению с другими витаминами структуру, основой которой является корриновое кольцо. Коррин во многом аналогичен порфирину (сложной структуре, входящей в состав гема, хлорофилла и цитохромов), но отличается от порфирина тем, что два пиррольных цикла в составе коррина соединены между собой непосредственно, а не метиленовым мостиком. В центре корриновой структуры располагается ион кобальта. Четыре координационных связи кобальт образует с атомами азота. Ещё одна координационная связь соединяет кобальт с диметилбензимидазольным нуклеотидом. Последняя, шестая координационная связь кобальта остаётся свободной: именно по этой связи и присоединяется цианогруппа, гидроксильная группа, метильный или 5'-дезоксиаденозильный остаток с образованием четырёх вариантов витамина B12, соответственно. Ковалентная связь углерод-кобальт в структуре цианокобаламина — единственный в живой природе пример ковалентной связи металл-углерод. В природе продуцентами этого витамина являются бактерии и археи. Ковалентная связь C-Co кофермента B12 участвует в двух типах ферментативных реакций:
- Реакции переноса атомов, при которых атом водорода переносится непосредственно с одной группы на другую, при этом замещение происходит по алкильной группе, спиртовому атому кислорода или аминогруппе.
- Реакции переноса метильной группы (-CH3) между двумя молекулами.
В организме человека есть только два фермента с коферментом B12:
- Метилмалонил-КоА-мутаза, фермент, использующий в качестве кофактора аденозилкобаламин и при помощи реакции, упомянутой выше в п.1, катализирует перестановку атомов в углеродном скелете. В результате реакции из L-метилмалонил-КоА получается сукцинил-КоА. Эта реакция является важным звеном в цепи реакций биологического окисления белков и жиров.
- 5-метилтетрагидрофолат-гомоцистеин-метилтрансфераза, фермент из группы метилтрансфераз, использующий в качестве кофактора метилкобаламин и при помощи реакции, упомянутой выше в п.2, катализирует превращение аминокислоты гомоцистеина в аминокислоту метионин.
Ни животные, ни растения не способны синтезировать витамин В12. Это единственный витамин, синтезируемый почти исключительно микроорганизмами: бактериями, актиномицетами и сине-зелёными водорослями. Из животных тканей наиболее богаты витамином В12 печень и почки. Хотя этот витамин вырабатывается микроорганизмами в пищеварительном тракте любого животного, включая человека, как продукт деятельности микрофлоры, однако он не может усваиваться, так как образуется в толстой кишке и не может попасть в тонкую кишку. Поэтому витамин B12 человек получает в основном с животной пищей, в том числе с мясом, рыбой, яйцами и молочными продуктами. Источником кобаламинов также могут быть обогащённые ими продукты: например, для вегетарианцев и веганов, таким источником являются сухие завтраки, пивные дрожжи и пищевые дрожжи, искусственно обогащённые витамином B12; витаминизированные хлопья и изделия из дроблёного зерна, а также специальные добавки. В пищевой промышленности многих стран витамин добавляют в такие продукты, как сухие завтраки, шоколадные батончики, энергетические напитки.
Витамин В12 выполняет коферментные функции. В организме человека есть две коферментные формы витамина В12 (кобаламина): метилкобаламин — в цитоплазме и дезоксиаденозилкобаламин — в митохондриях. В метилкобаламине вместо аденозильной группы, связанной с атомом кобальта (см. рис. 6.1), имеется метальная группа. В развитии анемии основная роль принадлежит дефициту ме-тилкобаламина, который служит коферментом в реакциях трансметилирования (подробнее об этих реакциях см. в гл. 11). Реакции траснметилирования происходят, в частности, при синтезе нуклеотидов и нуклеиновых кислот. Поэтому при недостатке метилкобаламина синтез нуклеиновых кислот нарушается. Это проявляется прежде всего в тканях с интенсивной клеточной пролиферацией. К их числу относится и кроветворная ткань. Деление и созревание клеток эритроци-тарного ряда нарушаются, размеры клеток превышают нормальные, значительная часть клеток — предшественников эритроцитов разрушается еще в костном мозге. В циркулирующей крови количество эритроцитов резко уменьшено, размеры их увеличены. При отсутствии лечения наступают изменения и в других тканях, и болезнь заканчивается гибелью больного. Введение 100-200 мкг витамина В12 ежедневно в течение примерно двух недель излечивает болезнь.
Другая коферментная форма витамина В12 — дезоксиаденозилкобаламин, участвует в метаболизме метилмалоновой кислоты, которая получается в организме из жирных кислот с нечетным числом углеродных атомов, а также из аминокислот с разветвленной углеродной цепью (подробнее об этом см. в гл. 10). При дефиците витамина В12 метилмалоновая кислота накапливается в организме и в больших количествах выводится с мочой; ее определение в моче используется для диагностики злокачественной анемии.
2.Β-Окисление жирных кислот. Роль карнитина в транспорте жирных кислот в митохондрии.
Для преобразования энергии, заключенной в жирных кислотах, в энергию связей АТФ существует метаболический путь окисления жирных кислот до СО2 и воды, тесно связанный с циклом трикарбоновых кислот и дыхательной цепью. Этот путь называется β-окисление, т.к. происходит окисление 3-го углеродного атома жирной кислоты (β-положение) в карбоксильную группу, одновременно от кислоты отщепляется ацетильная группа, включающая С1 и С2 исходной жирной кислоты.
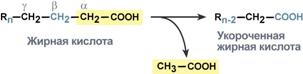
Элементарная схема β-окисления
Реакции β-окисления происходят в митохондриях большинства клеток организма (кроме нервных клеток). Для окисления используются жирные кислоты, поступающие в цитозоль из крови или появляющиеся при липолизе собственных внутриклеточных ТАГ. Суммарное уравнение окисления пальмитиновой кислоты выглядит следующим образом:
Пальмитоил-SКоА + 7ФАД + 7НАД+ + 7Н2O + 7HS-KoA → 8Ацетил-SКоА + 7ФАДН2 + 7НАДН
Этапы окисления жирных кислот:
Прежде, чем проникнуть в матрикс митохондрий и окислиться, жирная кислота должна активироваться в цитозоле. Это осуществляется присоединением к ней коэнзима А с образованием ацил-S-КоА. Ацил-S-КоА является высокоэнергетическим соединением. Необратимость реакции достигается гидролизом дифосфата на две молекулы фосфорной кислоты.
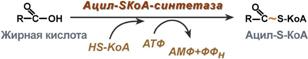
Реакция активации жирной кислоты
2. Ацил-S-КоА не способен проходить через митохондриальную мембрану, поэтому существует способ его переноса в комплексе с витаминоподобным веществом карнитином. На наружной мембране митохондрий имеется фермент карнитин-ацилтрансфераза I.
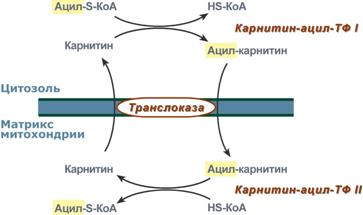
Карнитин-зависимый транспорт жирных кислот в митохондрию
Карнитин синтезируется в печени и почках и затем транспортируется в остальные органы. Во внутриутробном периоде и в первые годы жизни значение карнитина для организма чрезвычайно важно. Энергообеспечение нервной системы детского организма и, в частности, головного мозга осуществляется за счет двух параллельных процессов: карнитин-зависимого окисления жирных кислот и аэробного окисления глюкозы. Карнитин необходим для роста головного и спинного мозга, для взаимодействия всех отделов нервной системы, ответственных за движение и взаимодействие мышц. Существуют исследования, связывающие с недостатком карнитина детский церебральный паралич и феномен "смерти в колыбели".
3. После связывания с карнитином жирная кислота переносится через мембрану транслоказой. Здесь на внутренней стороне мембраны фермент карнитин-ацилтрансфераза II вновь образует ацил-S-КоА который вступает на путь β-окисления.
4. Процесс собственно β-окисления состоит из 4-х реакций, повторяющихся циклически. В них последовательно происходит окисление (ацил-SКоА-дегидрогеназа), гидратирование (еноил-SКоА-гидратаза) и вновь окисление 3-го атома углерода (гидроксиацил-SКоА-дегидрогеназа). В последней, трансферазной, реакции от жирной кислоты отщепляется ацетил-SКоА. К оставшейся (укороченной на два углерода) жирной кислоте присоединяется HS-КоА, и она возвращается к первой реакции. Все повторяется до тех пор, пока в последнем цикле не образуются два ацетил-SКоА.
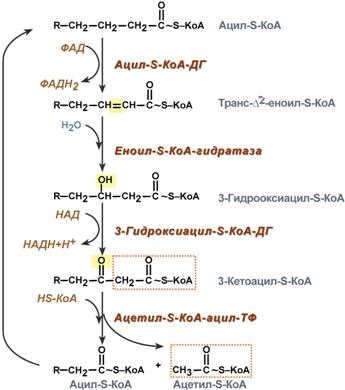
Последовательность реакций β-окисления жирных кислот
