
- •Содержание
- •Билет №1
- •2. Определение катаболизма. Катаболизм и анаболизм. Стадии катаболизма биомолекул в организме.
- •Билет№2.
- •1.Ферменты. Специфичность ферментов. Активный центр фермента.
- •2.Экзергонические и эндергонические биохимические реакции. Роль атф и других макроэргических фосфатов в сопряжении экзергонических процессов и эндергонических процессов.
- •3.Пути внутриклеточного метаболизма глюкозы. Гликолиз и глюконеогенез. Обратимые и необратимые реакции.
- •Билет №3
- •1.Регуляция активности ферментов. Проферменты. Изоферменты. Ингибиторы ферментов.
- •2.Реакции биологичемкого окисления.Типы реакций( дегидрогеназные, оксидазные, оксигеназные. Их биологическое значение.
- •3 Цитохромы Катализируют окисление веществ путем отдачи электронов Гемовое железо в одном из цитохромов имеется так же атом меди.
- •Билет№4
- •1.Ферментативный катализ
- •2.Митохондриальный транспорт
- •3.Аэробное окисление пирувата (окислительное декарбоксилирование пировиноградной кты).
- •Билет№5
- •1.Кинетика ферментативного катализа. Уравнение Михаэлиса-Ментен. Уравнение Лайнуивера-Берка.
- •2.Окислительное фосфорилирование. Пункты сопряжения окисления и фосфорилирования. Атф-синтетаза митохондрий.
- •3 Субъединицы (γ,δ,ε) способствуют целостности атф-синтазы
- •3.Полное окисление глюкозы. Энергетический баланс
- •Билет№6
- •1.Аллостерические ферменты. Ингибиторы и активаторы аллостерических ферментов. Аллостерические центры.
- •Деградация жирных кислот: β-окисление
- •Билет№7
- •1.Опять ферменты
- •2. Ингибиторы и разъединители транспорта электронов окислительного фосфорилирования
- •3.Глюконеогенез
- •Билет №8
- •1. Витамины
- •2. Микросомальная цепь транспорта электронов
- •3. Глюкозолактонный цикл
- •1. Витамин в2
- •3.Гипергликемия
- •Билет 10
- •Билет 11
- •1. Витамин в6(пиридоксин, пиридоксаль, пиридоксамин)
- •3 Существуют три источника аминокислот в клетке – поступление из крови, распад собственных внутриклеточных белков и синтез заменимых аминокислот.
- •Билет 12
- •1.Биотин
- •2. Нарушение обмена гликогена
- •3. Существуют три источника аминокислот в клетке – поступление из крови, распад собственных внутриклеточных белков и синтез заменимых аминокислот.
- •Билет 13. Фолиевая кислота. Биологическая роль. Пути поступления в организм. Коферментная функция.
- •2.Катаболизм триацилглицеролов. Реакции, механизм регуляции активности триглицеридлипазы. Нейрогуморальная регуляция липолиза (адреналин, глюкагон, инсулин).
- •3.Трансаминирование амк. Аминотрансферазы. Отдельные аминотрансферазы. Реакции. Биохимическое значение трансаминирования амк.
- •Билет 14
- •1.Витамин в12. Биологическая роль. Пути попадания в организм. Коферментная функция.
- •3.Пути превращения аммиака в организме человека. Механизмы обезвреживания аммиака.
- •Билет №15
- •1.Витамин с.
- •2.Окисление пальмитиновой кослоты.
- •3.Биосинтез мочевины.
- •Билет №16
- •1.Витамин а.
- •2.Окисление ненасыщенных жирных кислот.
- •3.Превращение безазотистого скелета ак
- •Билет №17
- •1.Витамин д
- •2. Биосинтез высших жирных кислот.
- •3. Метаболизм ак с разветвленной цепью.
- •Билет №25 Репликация днк
- •Свойства процесса репликации:
- •Желчные кислоты
- •Стероидные гормоны
- •2.Специализированные пути метаболизма цикл. А,к- фенилаланина и тирозина.. Заболевания, связанные с нарушением обмена фенилаланина и тирозина.
- •3.Биосинтез гема
- •Билет 19
- •2.Биосинтез пуриновых нуклеотидов
- •3.Основные закономерности генетического кода. Адапторная гипотеза ф. Крика и её развитие в wobble-гипотезе.
- •Билет №20
- •2. Кинетика ферменативного катализа. График зависимости скорости ферментативной реакции от концентрации субстрата при постоянной концентрации фермента.
- •Билет №21
- •Транскрипционные факторы: Механизмы действия тф , связавающиеся с днк, могут влиять на транскрипцию генов через несколько механизмов:
- •Билет№22
- •Билет 23
- •2. Полное окисление глюкозы. Энергетический баланс полного окисления глюкозы.
- •Билет№24
- •1.Антибиотические вещества, подавляющие синтез белка
- •24.2 Функционирование малат-аспартатного и глицерофосфатного шунта.
- •Билет №26
- •3. Окисление капроновой кислоты
- •Билет №27
- •Репликация
- •Билет 28
- •Билет29
- •29.2.Метаболизм аминокислот
- •Билет №30
- •1.Особенности молекулярной организации и экспрессии генома эукариот (экзоны, интроны, сплайсинг)
- •2.Образование кетоновых тел и их утилизация.
- •3.Цикл трикарбоновых кислот. Реакции
Билет29
29.1Транскрипция - первая стадия реализации генетической информации в клетке. В ходе процесса образуются молекулы мРНК, служащие матрицей для синтеза белков, а также транспортные, рибосомальные и другие виды молекул РНК, выполняющие структурные, адапторные и каталитические функции
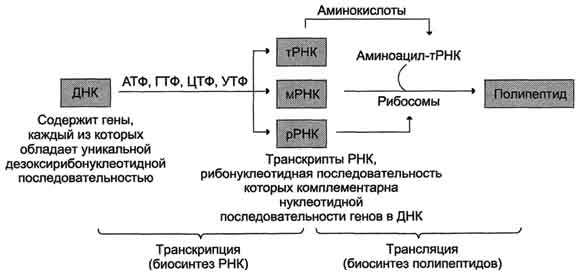
Синтез иРНК
Главный фермент синтеза иРНК - это РНК-полимераза (транскриптаза, ДНК-зависимая РНК-полимераза).
Этот фермент отличается от ДНК-полимеразы:
-РНК-полимеразы в клетке значительно больше, чем ДНК-полимеразы;
-РНК-полимераза работает с меньшей скоростью (50-100 нуклеотидов/сек, а ДНК-полимераза - 1000 нуклеотидов/сек)
-ДНК-полимераза обеспечивает большую верность, чем РНК-полимераза.
Наиболее изучена РНК-полимераза E.coli. Она состоит из пяти субъединиц - две альфа, две бетта и одна гамма. Считается, что функция гамма-субъединицы - это узнавание определённого участка на матрице ДНК, который называется промотор, куда присоединяется РНК-полимераза. Другим субъединицам фермента (core - ядро) приписывается функция инициации биосинтеза РНК (альфа), связывание субстратов и элонгация синтеза (бетта).
Сначала РНК-полимераза связывается с одной цепью нативной ДНК в определённой точке, вызывая расплетение биспиральной структуры на ограниченном участке, где и происходит ситез РНК. Потом синтез идёт в направлении 5` - 3`. К свободной 3`-ОН группе присоединяется 5`-фосфатная группа другого нуклеотидтрифосфата (НТФ) с последующим освобождением пирофосфата. Терминация идёт за счёт ро-фактора. Этот фактор обладает способностью обратимо связываться с терминирующим участком ДНК, выключая действие РНК-полимеразы. Таким образом происходит синтез пре-иРНК.
После синтез пре-иРНК у эукариот происходит процессинг, который включает:
-сплайсинг (нуклеотические и лигазные реакции)
-кепирование (образование шапочки)
-терминальные реакции полиаденилирования и метилирования.
Последовательность нуклеотидов в иРНК начинается с пары ГУ (5`-конец) и заканчивается парой АГ (3`-конец). Эти последовательности служат местами узнавания для ферментов сплайсинга.
Химический смысл кепирование сводится к присоединению 7-метилгуанозина посредством трифосфорной связи к 5`-концу молекулы иРНК.
Полиаденилирование заключается в последовательном ферментативном присоединении от 100 до 200 остатков АМФ и фрагментов ААУАА к 3`-концу иРНК. Также происходит метилирование 2`-ОН групп рибозы и N6-атомов АМФ.
29.2.Метаболизм аминокислот
Метаболизм аминокислот
Источниками аминокислот в клетке являются:
1. белки пищи после их гидролиза в органах пищеварения;
2. синтез заменимых аминокислот;
3. распад тканевых белков.
Тканевые белки подвергаются гидролитическому расщеплению при участии тканевых ПРОТЕАЗ - КАТЕПСИНОВ, которые в основном находятся в ЛИЗОСОМАХ. Выделяют разные КАТЕПСИНЫ, которые отличаются оптимумом рН и специфичностью действия. Распад тканевых белков необходим для обновления белков, а также для устранения дефектных молекул белка.
Несмотря на то, что почти для каждой аминокислоты выяснены индивидуальные пути обмена, известен ряд превращений, общих для многих аминокислот:
· ТРАНСАМИНИРОВАНИЕ;
· ДЕКАРБОКСИЛИРОВАНИЕ;
· ДЕЗАМИНИРОВАНИЕ.
ТРАНСАМИНИРОВАНИЕ – реакции межмолекулярного переноса аминогруппы от аминокислоты на кетокислоту без промежуточного образования аммиака.
Особенности реакций трансаминирования:
· протекают при участии ферментов - аминотрансфераз;
· для реакций необходим кофермент – пиридоксальфосфат (ПФ);
· реакции обратимы;
· могут подвергаться все аминокислоты кроме лиз, тре;
· в результате реакции образуются новая аминокислота и новая кетокислота.

Роль реакций ТРАНСАМИНИРОВАНИЯ:
1. Синтез заменимых аминокислот. При этом происходит перераспределение азота в органах и тканях;
2. Являются начальным этапом катаболизма аминокислот.
Реакции ДЕКАРБОКСИЛИРОВАНИЯ – отщепление альфа – карбоксильной группы аминокислот в виде углекислого газа.
При этом аминокислоты в тканях образуют биогенные амины, которые являются биологически активными веществами (БАВ). Среди них могут быть соединения, которые выполняют функции:
1. НЕЙРОМЕДИАТОРОВ (СЕРОТОНИН, ДОФАМИН, ГАМК),
2. Гормоны (АДРЕНАЛИН, НОРАДРЕНАЛИН),
3. Регуляторы местного действия (ГИСТАМИН).
ГАМК является НЕЙРОМЕДИАТОРОМ тормозного действия, поэтому препараты на основе ГАМК используются в клинике для лечения некоторых заболеваний ЦНС. Эта реакция используется в педиатрической практике: детям при сильном возбуждении используют раствор витамина В6, который стимулирует процесс образования ГАМК.
ДОФАМИН является НЕЙРОМЕДИАТОРОМ возбуждающего действия. Он является основой для синтеза АДРЕНАЛИНА и НОРАДРЕНАЛИНА.
Реакции ДЕЗАМИНИРОВАНИЯ - отщепление NН2-группы в виде аммиака.
ОКИСЛИТЕЛЬНОЕ ДЕЗАМИНИРОВАНИЕ.Непосредственно, ОКИСЛИТЕЛЬНОМУ ДЕЗАМИНИРОВАНИЮ подвергается только ГЛУ.
НЕПРЯМОЕ ДЕЗАМИНИРОВАНИЕ Этому виду дезаминирования подвергаются остальные аминокислоты, но через стадию трансаминирования с альфа-кетоглутаровой кислотой. Затем глутаминовая кислота (продукт этой реакции) подвергается окислительному дезаминированию.
Незаменимые аминокислоты — необходимые аминокислоты, которые не могут быть синтезированы в том или ином организме, в частности, в организме человека. Поэтому их поступление в организм с пищей необходимо.
Незаменимыми для взрослого здорового человека являются 8 аминокислот: валин, изолейцин, лейцин, лизин, метионин, треони́н, триптофан и фенилалани́н;
Для детей незаменимыми также являются аргинин и гистидин.
Заменимые аминокислоты –аминокислоты, которые могут поступать в наш организм с белковой пищей либо же образовываться в организме из других аминокислот. К заменимым аминокислотам относятся: аргинин, глютаминовая кислота, глицин, аспарагиновая кислота, гистидин, серин, цистеин, тирозин, аланин, пролин.
29.3.Триацилглицерины — сложные эфиры глицерина и высших жирных кислот. В их составе в наибольшем количестве содержатся стеариновая, пальмитиновая, пальмитоолеиновая кислоты. В плазме крови триацилглицерины транспортируются исключительно в составе липопротеинов, главным образом хиломикронов и липопротеинов очень низкой плотности ЛПОНП), осуществляющих транспорт триацилглицеринов из мест синтеза к местам утилизации. Циркулирующие в крови ЛПОНП и хиломикроны атакуются гепарин‑зависимым ферментом липопротеидлипазой, локализованной на поверхности эндотелия капилляров. Освобождающиеся жирные кислоты поступают в клетки, где используются для получения энергии.
Биосинтез триглицеридов.Триглицериды синтезируются а клетках практически всех органах и тканей в качестве резервных питательных веществ, однако необходимо подчеркнуть, что синтез интенсивный с наибольшей интенсивностью идет в клетках печени и клетках жировой ткани
Что необходимо для синтеза триглицеридов? Для синтеза необходимы ВЖК (высщие жирные кислоты)и глицерол ВЖК поступают в клетки или из плазмы крови или же синтезируются на месте, т е. в клетках непосредственно, из ацетилКоА.
Глицерол может поступать так же из плазмы крови, однако основным источником глицерина для синтеза триглицеридов и даже фосфолипидов в клетках служит промежуточный продукт распада углеводов –фосфодиоксиацетон.ВЖК участвуют в синтезе триглицеридов в виде своих активированных производных - ацилКоА. Необходимый для синтеза фосфоглицерин образуется или путем восстановления фосфодиоксиацетона, или же за счет фосфорилирования свободного глицерола Эта реакция катализируется АТФ зависимой глицеролкиназой
После образования фосфоглицерина за счет двух последовательных реакции ацилирования образуется фосфотидная кислота, затем от нее отщепляется остаток фосфорной кислоты и ооразуется диглицерид
И наконец в ходе последней реакции ацилирования образуется триглицерид.
Синтез фосфолипидов Все необходимые организму фосфолипиды могут синтезироваться в его клетках, причем в клетках могут функционировать несколько различных метаболических путей биосинтеза глицерофосфолипидов. Синтез лицитина А) при реакции ацилирования образуется фосфотидная кислота далее за счет фермента фосфотазы фосфотиднойкислоты образуется диглнцерид Б) Параллельно идет активация аминоспиртов (при наличии свободных аминоспиртов в клетке) далее идетактивация холина с образованием его производного - ЦДФхоли (активированный) он может включаться всинтезх.в) Диглицерид+ЦДФхолин - трансферазная реакция обеспечивает образование фосфотидилхолина и отщепляется ЦМФ, который затем за счет энергии АТФ может превращаться в ЦДФ. Алътернатнвным вариантоу синтеза может быть синтез с промежуточным образованием фосфотидной кислоты, но уже активированной. Сама фосфотидная кислота образуется при помощи ацилирования фосфоглицерина. Далее она взаимодействует с цитидин-3-фосфатом с образованием активной фосфотиднои кислоты (ЦДФ-фосфотидная кислота). Далее идет превращение в фосфотидилсерин или в инозитолфосфатид В том и другом случае происходит отщепление ЦМФ
Фосфолипиды (фосфоглицериды) - это сложные липиды, производные фосфатидной кислоты.
Фосфатидная кислота образуется в организме в процессе биосинтеза три-ацилглицеролов и глицерофосфолипидов как общий промежуточный метаболит; в тканях она присутствует в незначительных количествах. Следует отметить, что все природные глицерофосфолипиды относятся к L-ряду. Различные глицерофосфолипиды отличаются друг от друга дополнительными группировками, присоединенными фосфоэфирной связью к фосфатидной кислоте.
Фосфатидные кислоты являются промежуточными соединениями при биосинтезе всех глицеролипи - Дов за исключением липидов с простой эфирной связью; эти два типа соединений легко превращаются друг в друга путем фосфо - Рилирования и дефосфорилирования.
Глицеролипиды
В первом положении фосфо- и нейтральных глицеролипидов могут быть остатки не ЖК, а жирных спиртов (алкильная связь) или альдегидов (алкенильная). Во втором положении связь всегда сложноэфирная. Следовательно, могут быть три формы липидов: диацильная (А), алкилацильная (Б ) и алкенилацильная (В ).
Все глицерофосфолипиды можно рассматривать как производные фосфатидной кислоты, в которой атом водорода в одном из гмдроксилов фосфорной кислоты замещен на остатки или аминоспиртов, или серина, или фосфоинозитола или других соединений. В соответствии с характером замещения мы получаем различные классы глицерофосфолипидов.
