
- •Содержание
- •Билет №1
- •2. Определение катаболизма. Катаболизм и анаболизм. Стадии катаболизма биомолекул в организме.
- •Билет№2.
- •1.Ферменты. Специфичность ферментов. Активный центр фермента.
- •2.Экзергонические и эндергонические биохимические реакции. Роль атф и других макроэргических фосфатов в сопряжении экзергонических процессов и эндергонических процессов.
- •3.Пути внутриклеточного метаболизма глюкозы. Гликолиз и глюконеогенез. Обратимые и необратимые реакции.
- •Билет №3
- •1.Регуляция активности ферментов. Проферменты. Изоферменты. Ингибиторы ферментов.
- •2.Реакции биологичемкого окисления.Типы реакций( дегидрогеназные, оксидазные, оксигеназные. Их биологическое значение.
- •3 Цитохромы Катализируют окисление веществ путем отдачи электронов Гемовое железо в одном из цитохромов имеется так же атом меди.
- •Билет№4
- •1.Ферментативный катализ
- •2.Митохондриальный транспорт
- •3.Аэробное окисление пирувата (окислительное декарбоксилирование пировиноградной кты).
- •Билет№5
- •1.Кинетика ферментативного катализа. Уравнение Михаэлиса-Ментен. Уравнение Лайнуивера-Берка.
- •2.Окислительное фосфорилирование. Пункты сопряжения окисления и фосфорилирования. Атф-синтетаза митохондрий.
- •3 Субъединицы (γ,δ,ε) способствуют целостности атф-синтазы
- •3.Полное окисление глюкозы. Энергетический баланс
- •Билет№6
- •1.Аллостерические ферменты. Ингибиторы и активаторы аллостерических ферментов. Аллостерические центры.
- •Деградация жирных кислот: β-окисление
- •Билет№7
- •1.Опять ферменты
- •2. Ингибиторы и разъединители транспорта электронов окислительного фосфорилирования
- •3.Глюконеогенез
- •Билет №8
- •1. Витамины
- •2. Микросомальная цепь транспорта электронов
- •3. Глюкозолактонный цикл
- •1. Витамин в2
- •3.Гипергликемия
- •Билет 10
- •Билет 11
- •1. Витамин в6(пиридоксин, пиридоксаль, пиридоксамин)
- •3 Существуют три источника аминокислот в клетке – поступление из крови, распад собственных внутриклеточных белков и синтез заменимых аминокислот.
- •Билет 12
- •1.Биотин
- •2. Нарушение обмена гликогена
- •3. Существуют три источника аминокислот в клетке – поступление из крови, распад собственных внутриклеточных белков и синтез заменимых аминокислот.
- •Билет 13. Фолиевая кислота. Биологическая роль. Пути поступления в организм. Коферментная функция.
- •2.Катаболизм триацилглицеролов. Реакции, механизм регуляции активности триглицеридлипазы. Нейрогуморальная регуляция липолиза (адреналин, глюкагон, инсулин).
- •3.Трансаминирование амк. Аминотрансферазы. Отдельные аминотрансферазы. Реакции. Биохимическое значение трансаминирования амк.
- •Билет 14
- •1.Витамин в12. Биологическая роль. Пути попадания в организм. Коферментная функция.
- •3.Пути превращения аммиака в организме человека. Механизмы обезвреживания аммиака.
- •Билет №15
- •1.Витамин с.
- •2.Окисление пальмитиновой кослоты.
- •3.Биосинтез мочевины.
- •Билет №16
- •1.Витамин а.
- •2.Окисление ненасыщенных жирных кислот.
- •3.Превращение безазотистого скелета ак
- •Билет №17
- •1.Витамин д
- •2. Биосинтез высших жирных кислот.
- •3. Метаболизм ак с разветвленной цепью.
- •Билет №25 Репликация днк
- •Свойства процесса репликации:
- •Желчные кислоты
- •Стероидные гормоны
- •2.Специализированные пути метаболизма цикл. А,к- фенилаланина и тирозина.. Заболевания, связанные с нарушением обмена фенилаланина и тирозина.
- •3.Биосинтез гема
- •Билет 19
- •2.Биосинтез пуриновых нуклеотидов
- •3.Основные закономерности генетического кода. Адапторная гипотеза ф. Крика и её развитие в wobble-гипотезе.
- •Билет №20
- •2. Кинетика ферменативного катализа. График зависимости скорости ферментативной реакции от концентрации субстрата при постоянной концентрации фермента.
- •Билет №21
- •Транскрипционные факторы: Механизмы действия тф , связавающиеся с днк, могут влиять на транскрипцию генов через несколько механизмов:
- •Билет№22
- •Билет 23
- •2. Полное окисление глюкозы. Энергетический баланс полного окисления глюкозы.
- •Билет№24
- •1.Антибиотические вещества, подавляющие синтез белка
- •24.2 Функционирование малат-аспартатного и глицерофосфатного шунта.
- •Билет №26
- •3. Окисление капроновой кислоты
- •Билет №27
- •Репликация
- •Билет 28
- •Билет29
- •29.2.Метаболизм аминокислот
- •Билет №30
- •1.Особенности молекулярной организации и экспрессии генома эукариот (экзоны, интроны, сплайсинг)
- •2.Образование кетоновых тел и их утилизация.
- •3.Цикл трикарбоновых кислот. Реакции
Билет 19
1.БИОСИНТЕЗ ТРИАЦИЛГЛИЦЕРОЛОВ И ФОСФОГЛИЦЕРИДОВ. Биосинтез триацилглицеролов и глицеролфосфатидов начинается с общих предшественников. В животных тканях биосинтез триацилглицеролов и главных фосфолипидов - фосфатидилэтаноламина и фосфатидилхолина начинается с двух общих предшественников и имеет несколько общих этапов. Общими предшественниками служат СоА-эфиры жирных кислот и глицерол-3-фосфат. Глицеролфосфат может образовываться двумя путями. В ходе гликолиза он возникает из дигидроксиацетонфосфата под действием цитоплазматического NAD-зависимого фермента глицеролфосфатдегидрогеназы: Дигидроксиацетонфосфат + NADH + Н+ ↔ L-глицерол-З-фосфат + NAD + .
Кроме того, глицеролфосфат может образоваться из глицерола под действием глицеролкиназы: АТР + Глицерол → Глицерол-3-фосфат + ADP. Другими предшественниками триацил-глицеролов служат СоА-производные жирных кислот, образующиеся при помощи ацил-СоА—синтетаз. Жирная кислота + АТР + СоА—SH — Ацил—S—СоА + AMP + РРi На первом этапе биосинтеза триацил-глицеролов происходит ацилирование двух свободных гидроксильных групп глицеролфосфата двумя молекулами Со-А-производных жирных кислот с образованием диацилглицерол-3-фосфата: Ацил—S—СоА + Глицерол → Моноацилглицерол-3-фосфат + СоА—SH Моноацилглицерол-3-фосфат + + Ацил—S—СоА → Диацилглицерол-3-фосфат + СоА—SH
Д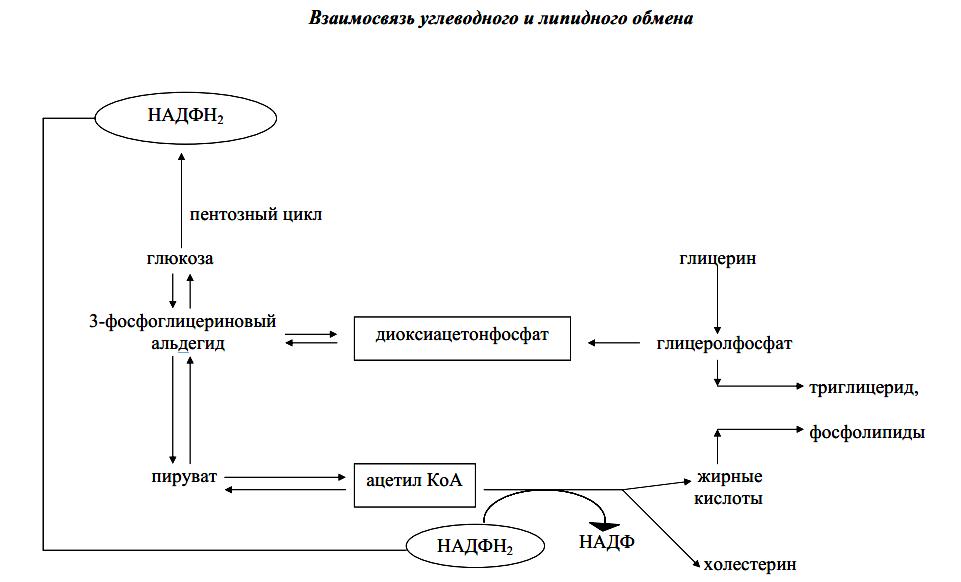 иацилглицерол-3-фосфат
(чаще его называют фосфатидной
кислотой) встречается в клетках
лишь в следовых количествах, однако он
является важным промежуточным продуктом
в биосинтезе липидов. В ходе синтеза
триацилглицеролов фосфатидат
гидролизуется фосфатидат-фосфатазой с
образованием 1,2-диа-цилглицерола:
Фосфатидат
+ Н20 → 1,2-диацилглицерол + Рi.
Диацилглицерол,
взаимодействуя с третьей молекулой
СоА-производного жирной кислоты,
превращается затем в
триацилглицерол:
СоА-производное
жирной кислоты +1,2-диацилглицерол →
Триацилглиперол + СоА—SH.
Формирование
каждой эфирной связи триацилглицеролов
требует значительного количества
свободной энергии. Для того чтобы
возникла эфирная связь, жирная кислота
сначала должна активироваться путем
образования эфира с СоА; для этой реакции
необходима энергия двух высокоэнергетических
фосфатных связей, так как она протекает
благодаря пирофосфатному расщеплению
АТР и последующему гидролизу образовавшегося
пирофосфата.
иацилглицерол-3-фосфат
(чаще его называют фосфатидной
кислотой) встречается в клетках
лишь в следовых количествах, однако он
является важным промежуточным продуктом
в биосинтезе липидов. В ходе синтеза
триацилглицеролов фосфатидат
гидролизуется фосфатидат-фосфатазой с
образованием 1,2-диа-цилглицерола:
Фосфатидат
+ Н20 → 1,2-диацилглицерол + Рi.
Диацилглицерол,
взаимодействуя с третьей молекулой
СоА-производного жирной кислоты,
превращается затем в
триацилглицерол:
СоА-производное
жирной кислоты +1,2-диацилглицерол →
Триацилглиперол + СоА—SH.
Формирование
каждой эфирной связи триацилглицеролов
требует значительного количества
свободной энергии. Для того чтобы
возникла эфирная связь, жирная кислота
сначала должна активироваться путем
образования эфира с СоА; для этой реакции
необходима энергия двух высокоэнергетических
фосфатных связей, так как она протекает
благодаря пирофосфатному расщеплению
АТР и последующему гидролизу образовавшегося
пирофосфата.
2.Биосинтез пуриновых нуклеотидов
Первая специфическая реакция образования пуриновых нуклеотидов - перенос амидной группы Глн на ФРДФ с образованием 5-фосфорибозил-1 -амина. Эту реакцию катализирует фермент амидофосфорибозилтрансфераза. При этом формируется β-N-гликозидная связь. Затем к аминогруппе 5-фосфорибозил-1-амина присоединяются остаток глицина, N5,N10-метенил-Н4-фолата ещё одна амидная группа глутамина, диоксид углерода, аминогруппа аспартата и формильный остаток N10-формил Н4-фолата. Результатом этой десятистадийной серии реакций является образование первого пуринового нуклеотида - инозин-5'-монофосфата (ИМФ), на синтез которого затрачивается не менее шести молекул АТФ.
ИМФ(иозиновая кислота) в основном используется на синтез АМФ или ГМФ. Небольшое количество этого продукта обнаруживается также в тРНК в качестве одного из минорных нуклеотидов.
Превращение ИМФ в АМФ и ГМФ в обоих случаях включает 2 стадии и идёт с затратой энергии. Аденилосукцинатсинтетаза, используя энергию ГТФ, присоединяет аспартат к ИМФ с образованием аденилосукцината, который в реакции, катализируемой аденилосукциназой, отщепляет фумарат и превращается в АМФ.
Второй пуриновый нуклеотид (ГМФ) образуется также в 2 стадии. Сначала ИМФ окисляется NAD+-зависимой ИМФ-дегидрогеназой с образованием ксантозин-5'-монофосфата (КМФ). Последующее трансамидирование гидроксильной группы при С2-пуринового кольца КМФ катализирует ГМФ-синтетаза с использованием амидной группы Глн и энергии АТФ.
При образовании пуриновых нуклеотидов ГТФ расходуется на синтез АМФ, а АТФ - на синтез ГМФ. Перекрёстное использование пуриновых нуклеозидтрифосфатов на образование конечных продуктов синтеза помогает поддерживать в клетках баланс адениловых и гуаниловых нуклеотидов.
Огромные затраты энергии для синтеза пуриновых нуклеотидов de novo не способны полностью обеспечить субстратами синтез нуклеиновых кислот в период гаструляции и раннего роста ребёнка. Потребность в большом количестве нуклеотидов привела к развитию "запасных" путей синтеза этих молекул. Наибольшее значение в этом процессе имеют ферменты, осуществляющие превращение пуринов в мононуклеотиды с использованием ФРДФ как донора остатка фосфорибозы.
Основным показателем, от которого зависит синтез пуриновых нуклеотидов, служит концентрация ФРДФ, которая, в свою очередь, зависит от скорости его синтеза, утилизации и разрушения. Количество ФРДФ определяется доступностью рибозо-5-фосфата и активностью ФРДФ синтетазы - фермента, чувствительного к концентрации фосфата и пуриновых нуклеотидов. Внутриклеточная концентрация ФРДФ строго регулируется и обычно низкая. ФРДФ синтетаза - аллостерический фермент. Он активируется неорганическим фосфатом (Рi) и ингибируется пуриновыми нуклеозид- моно-, ди- и трифосфатами. ФРДФ служит не только субстратом, но и аллостерическим активатором второй реакции синтеза пуринонуклеотидов de novo, которую катализирует амидофосфорибозилтрансфераза.
Пуриновые нуклеотиды, особенно АМФ и ГМФ по механизму отрицательной обратной связи ингибируют амидофосфорибозилтрансферазу, которая катализирует первую специфическую реакцию синтеза пуриновых нуклеотидов de novo.
Метаболическая цепь образования АМФ и ГМФ de novo регулируется также в месте её разветвления: АМФ ингибирует аденилосукцинатсинтетазу, а ГМФ - реакцию образования ксантиловой кислоты, которую катализирует ИМФ дегидрогеназа. Перекрёстная регуляция путей использования ИМФ служит для того, чтобы снизить синтез одного пуринового нуклеотида при дефиците другого.
Помимо ферментов основного пути синтеза пуриновых нуклеотидов de novo, регулируется также активность ферментов "запасных" путей: аденинфосфорибозилтрансфераза ингибируется АМФ, а гипоксантин-гуанинфосфорибозилтрансфераза - ИМФ и ГМФ.

