- •Теории химического строения
- •Основные положения теории бутлерова:
- •2. Положение о зависимости свойств от химического строения.
- •3. Положение о взаимном влиянии атомов.
- •6. Классификация органических реакций по механизму
- •Пространственное строение предельных углеводородов
- •Способы получения предельных углеводородов
- •Лабораторные способы получения алканов
- •Физические свойства предельных углеводородов
- •I. Замещение
- •II. Окисление
- •IV. Изомеризация предельных углеводородов
- •Номенклатура
- •Способы получения
- •Химические свойства олефинов
- •1. Реакции присоединения
- •2. Реакции окисления
- •3. Реакции полимеризации
- •4. Реакции аллильного замещения
- •Физические свойства
- •Особенности электронного строения диенов с сопряженными связями
- •1. Реакции присоединения
- •Классификация
- •Способы получения
- •Физические свойства
- •Химические свойства
- •I.Реакции нуклеофильного замещения
- •Реакции отщепления галогена
- •III. Реакции отщепления галогеноводорода
- •Карбонильные соединения
- •Способы получения
- •Отличие химических свойств альдегидов и кетонов
- •Химические свойства
- •III. Реакции окисления и восстановления
- •Реакции восстановления
- •Карбоновые кислоты
- •Номенклатура
- •Способы получения
- •4) Дегидратация кислот
- •Определение
- •Классификация
- •Изомерия
- •Получение
- •Физические свойства
- •Химические свойства
- •Основные признаки ароматичности
- •Ароматические соединения
- •Гомологический ряд, изомерия и номенклатура ароматических углеводородов
- •Названия ароматических радикалов
- •Способы получения ароматических углеводородов
- •Б. Синтетические способы получения ароматических углеводородов
- •Химические свойства
- •Механизм электрофильного замещения
- •Нитрование гомологов бензола
- •Реакции присоединения (нетипичны)
- •Галоидпроизводные ароматических углеводородов Классификация, изомерия, номенклатура
- •Получение
- •Физические свойства галогенопроизводных ароматических углеводородов
- •Химические свойства
- •Нитросоединения ароматического ряда
- •1.Нитросоединения с нитрогруппой в ядре
- •Физические свойства
- •Химические свойства
- •II. Реакции в ядре
- •II. Нитросоединения с группой no2 в боковой цепи
- •Способы получения
- •Химические свойства ароматических нитросоединений с группой no2 в боковой цепи
- •Ароматические сульфокислоты
- •Физические свойства
- •Химические свойства
- •I тип реакций. Реакции, характерные для органических кислот.
- •II тип реакции. Восстановление сульфогруппы
- •III тип реакций. Реакции нуклеофильного замещения сульфогруппы
- •IV тип реакций. Реакции электрофильного замещения в ядре идут в соответствии с правилами замещения
- •27. Ариламины. Ароматические амины Классификация
- •I. По положению аминогруппы относительно ароматического ядра.
- •II. По количеству радикалов, связанных с азотом
- •III. По количеству аминогрупп
- •Получение
- •Физические свойства
- •Химические свойства
- •II. Реакции замещения водорода в аминогруппе
- •IV. Окисление
- •V. Реакции замещения в ароматическом ядре
- •VI. Реакции конденсации ароматических аминов с другими органическими и неорганическими соединениями
- •Диазо- и азосоединения
- •Ароматические диазосоединения
- •1. Реакция диазотирования - -получение солей диазония.
- •Химические свойства солей диазония
- •I. Реакции с выделением азота
- •II. Реакции диазосоединений без выделения азота
- •Азокрасители
- •Связь строения с цветностью
- •Ароматические оксисоединения
- •Классификация
- •Физические свойства фенолов
- •Химически свойства фенолов
- •I. Реакции подвижного водорода в группе он
- •II. Реакции электрофильного замещения в ядре
- •III. Окислительно-восстановительные реакции
- •IV. Конденсация фенолов с другими органическими соединениями
- •Ароматические альдегиды и кетоны
- •Способы получения
- •II. Частные способы получения альдегидов и кетонов
- •Физические свойства
- •Химические свойства
- •Ароматические кислоты
- •Способы получения
- •Физические свойства
- •Химические свойства
- •Полициклические ароматические углеводороды и их производные
- •Ароматические углеводороды с изолированными ядрами
- •Способы получения
- •Физические свойства
- •Химические свойства
- •Наиболее важные группы многоядерных соединений. Группа дифенила
- •Группа трифеиилметана
- •Полициклические ароматические углеводороды с конденсированными ядрами
- •Получение
- •Физические свойства
- •Особенности химических свойств
- •Ароматические моноциклические пятичленные гетероциклы
- •Номенклатура гетероциклических соединений
- •Способы получения
- •Физические свойства
- •34. Шестичленные гетероциклы с одним гетероатомом
- •Получение
Полициклические ароматические углеводороды и их производные
Делятся на два типа.
Соединения с изолированными ядрами (многоядерные).
Соединения с конденсированными ядрами.
Ароматические углеводороды с изолированными ядрами
Имеют два или несколько бензольных колец, соединенных между собой посредством простых связей или посредством других углеродных атомов. Например,
|
Дифенил |
|
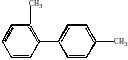
2,4/-диметилдифенил |
|
Дифенилметан |
|
П,п/-диоксидифенилметан; бис(2-оксифенил)метан; 4,4?-метиленбисфенол |
|
Трифенилметан |
C6H5-CH2-CH2-C6H5 |
Sim-1,2-дифенилэтан |
|
Asim-дифенилэтан |
|
Гексафенилэтан |
Способы получения
Основаны, главным образом, на использовании реакций вюрца-Фиттига и Фриделя-Крафтса. Эти реакции имеют здесь определенное ограничение:
Реакция Вюрца идет только с иодарилами.
2 C6H5I + 2 Na C6H5-C6H5 + 2 NaI
2) Для получения многоядерных углеводородов с помощью реакции Фриделя-Крафтса необходимо использовать полигалогенопроизводные углеводородов.
3 |
|
AlCl3 + CHCl3 (C6H5)3CH -3 HCl |
|
хлороформ |
трифенилметан |
Физические свойства
Бесцветные вязкие жидкости или кристаллические термостойкие вещества, нерастворимые в воде.
Химические свойства
Проявляют типичные свойства ароматических углеводородов.
Особенности:
1) Реакции электрофильного замещения в ядре идут труднее, чем у одноядерных (при более жестких условиях). Заместители становятся в основном в положение пар- или орто- (если пара-положение заняты).
Реакции связующего звена.
Атомы водорода, расположенные в -положении к нескольким ядрам, обладают большей подвижностью и очень легко подвергаются замещению по различным механизмам.
С6H5-СH2-C6H5 + 2 Cl2 C6H5-CCl2-C6H5 + 2 HCl
дифенилметан дихлордифенилметан
С6H5-СH2-C6H5 + O2 |
|
+ H2O |
|
дифенилкетон (ацетофенон) |
|
Наиболее важные группы многоядерных соединений. Группа дифенила
Дифенил может быть получен пиролизом бензола.
|
+ |
|
7000
-H2 |
|
AlCl3 + 3 Cl2 |
|
|
|
|
||
Благодаря такой высокой термостойкости используется в качестве высокотемпературного теплоносителя в реакторах (Тпл=700С, Ткип=2540С). Производные дифенила с заместителями в орто-положениях, могут иметь оптическую изомерию. Известно, что оптическая изомерия наблюдается у соединений, имеющих асимметричный атом углерода. В дифениле два плоских бензольных кольца соединены простой связью и могут свободно вращаться вокруг этой простой связи,
не имея закрепленного положения в пространстве.
Если в орто-положениях к простой связи имеется несколько заместителей, занимающих значительный объем в пространстве, то они делают свободное вращение невозможным, и кольца приобретают закрепленное положение друг относительно друга. Если сумма радиусов двух о-заместителей превышает 3,0 А0, то расположение ядер в одной плоскости становится невозможным: они поворачиваются друг к другу, под определенным углом, чаще всего под углом 900С. такие молекулы не имеют центра симметрии, и поэтому, хотя у них нет асимметрических атомов, у них наблюдается явление оптической изомерии.
Так, 2,2/-динитродифенил-6,6/-дикарбоновая кислота имеет два изомера:
|
|
Эти две формы отличаются друг от друга как предмет от зеркального изображения – они являются оптическими антиподами.
Такое явление – наличие пространственных оптических изомеров вследствие торможения свободного вращения – получило название поворотной оптической изомерии.