
- •Российской федерации
- •Тема 1. Роль отечественных ученых в развитии науки
- •Тема 11. Физико-химические, органолептические и техноло-
- •Тема 12. Физико-химические изменения молока при его
- •Тема 13. Физико-химические и биохимические изменения
- •Тема 1. Роль отечественных ученых в развитии науки «химия и физика молока»
- •Контрольные вопросы
- •Тема 2. Современное состояние молочной промышленности, основные направления развития технологии молочных продуктов и задачи исследований в области химии и физики молока
- •Тема 3. Роль молока и молочных продуктов в питании человека. Экономические аспекты рационального использования молока в производстве молочных продуктов
- •Тема 4. Общая характеристика химического состава молока
- •Компоненты молока
- •10.Как изменяются состав и свойства молока при заболеваниях коров маститом?
- •Тема 5. Белки молока
- •ИrG1 (1,2-3,3%) b-лактоглобулин Электрофо- мочевина
- •5.2. Структура белков
- •5.3. Состав белков: элементарный и аминокислотный
- •5.4. Физико-химические свойства белков
- •5.5. Химические свойства белков
- •5.6. Биосинтез белков в молочной железе
- •Контрольные вопросы
- •Тема 6. Липиды молока
- •6.1. Значение липидов. Классификация
- •6.2. Глицеридный состав молочного жира
- •6.3. Жирнокислотный состав молочного жира
- •6.4. Физико-химические свойства молочного жира
- •6.5. Химические свойства молочного жира
- •6.6. Фосфолипиды, стерины и другие липиды
- •6.7. Биосинтез липидов
- •Контрольные вопросы
- •Тема 7. Углеводы молока
- •7.1. Общая характеристика углеводов молока. Значение лактозы
- •7.2. Структура лактозы, ее изомерные формы и физические свойства
- •7.3. Химические свойства лактозы
- •7.4. Биосинтез лактозы
- •Контрольные вопросы
- •Тема 8. Минеральные вещества молока
- •8.1. Общая характеристика минеральных веществ. Солевой состав молока
- •Ионы Макроэлементы Микроэлементы
- •8.2. Солевое равновесие молока. Факторы, влияющие на солевое равновесие
- •8.3. Роль макро- и микроэлементов в молоке и молочных продуктах
- •Контрольные вопросы
- •Тема 9. Биологически активные и другие вещества молока
- •Витамины молока и их биологическая роль
- •Гормоны и газы
- •Контрольные вопросы
- •Тема 10. Молоко как полидисперсная система
- •10.1. Общая характеристика дисперсных систем
- •10.2. Молоко как коллоидная система
- •10.2.1. Структура мицелл казеина, обусловливающая коллоидное состояние золя
- •10.2.2. Условия дестабилизации коллоидного состояния золя и формирование геля при различных способах коагуляции
- •10.3. Молоко как эмульсия жира в плазме
- •10.3.1. Факторы агрегативной устойчивости жировой эмульсии
- •10.3.2. Факторы нарушения устойчивости жировой эмульсии
- •10.4. Молоко как истинный раствор
- •Контрольные вопросы
- •Тема 11. Физико-химические, органолептические и технологические свойства молока
- •Плотность
- •Титруемая кислотность
- •11.3. Активная кислотность и буферные свойства
- •Окислительно-восстановительный потенциал
- •Вязкость и поверхностное натяжение
- •Осмотическое давление и температура замерзания молока
- •Электропроводность и теплофизические свойства
- •Органолептические свойства
- •Технологические свойства
- •Контрольные вопросы
- •Тема 12. Физико-химические изменения молока при его хранении и обработке
- •10.Какие изменения происходят в солевой системе при тепловой обработке молока?
- •11.Какие изменения происходят в жировой фазе при тепловой обработке молока?
- •12.Как изменяется активность ферментов при тепловой обработке молока?
- •Тема 13. Физико-химические и биохимические изменения составных частей молока
- •3 Надф`
- •2Адф Ацетат Ацетальдегид
- •2Атф надф·н2
- •2 Пентозо-5-фосфат атф
- •13.2.4. Изменения липидных компонентов
- •Контрольные вопросы
- •Библиографический список
10.Какие изменения происходят в солевой системе при тепловой обработке молока?
11.Какие изменения происходят в жировой фазе при тепловой обработке молока?
12.Как изменяется активность ферментов при тепловой обработке молока?
Тема 13. Физико-химические и биохимические изменения составных частей молока
В ПРОЦЕССАХ ЕГО ПЕРЕРАБОТКИ И ПРИ ХРАНЕНИИ МОЛОЧНЫХ ПРОДУКТОВ
Изменения белковой и жировой фаз, углеводных компонентов, солевого и витаминного состава, которые происходят в молоке при его хранении и обработке (тепловой, механической) продолжаются при последующих технологических операциях выработки молочных продуктов. Характер этих изменений зависит от вида вырабатываемых продуктов и, соответственно, от направленности и режимов физических воздействий, например, нагревания и концентрирования в производстве сгущенных, сгущенных стерилизованных и сухих продуктов, или биологических воздействий: использования бактериальных заквасок и ферментных препаратов в производстве кисломолочных продуктов, сыров.
13.1. Изменения составных компонентов молока
при сгущении и сушке
При сгущении молока происходит концентрирование всех составных компонентов за счет удаления части свободной воды. Следствием концентрирования являются увеличение концентрации всех дисперсных фаз молока и активной межфазной поверхности; рост свободной поверхностной энергии на границе раздела фаз и усиление роли сил молекулярного взаимодействия (сил Ван-дер-Ваальса-Лондона). Каковы последствия этих изменений для различных фаз молока имеет смысл рассмотреть более подробно.
Белки и соли. При концентрировании (сгущении) происходит увеличение молекулярной массы частиц казеинаткальцийфосфатного комплекса в силу следующих причин:
повышения концентрации ионов водорода в среде и, как следствие, снижение отрицательного заряда на его поверхности;
изменения соотношения электростатических сил отталкивания и молекулярного притяжения в сторону увеличения последних;
увеличения концентрации солей кальция в истинном растворе, а следовательно, и ионизированного кальция, способствующего агрегированию мицелл.
Сближение агрегатов ККФК при концентрировании за счет усиления молекулярного взаимодействия приводит к образованию структурированной системы, характеризующейся повышенной вязкостью. Это явление усиливается предшествующей гомогенизацией и тепловой обработкой молока, при которой происходит денатурация сывороточных белков, как следствие, образование комплексов β-лактоглобулин – α-лактальбумин и их взаимодействие с мицеллами казеина. Интенсивность этих изменений возрастает при последующей тепловой обработке (стерилизации или сушке), что может привести к дестабилизации белковой фазы (коагуляции).
С целью предотвращения дестабилизации белковой фазы при сгущении, последующей стерилизации сгущенного молока или сушке используют следующие приемы. Путем внесения солей-стабилизаторов в виде цитратов или фосфатов калия (натрия) снижают концентрацию ионизированного кальция в исходном молоке. Анионы лимонной или фосфорной кислот связывают ионизированный кальций, переводя его в нерастворимое состояние. При таких условиях дисперсность и гидрофильность белковых частиц повышается. Другим способом повышения тепловой устойчивости белковой фазы является удаление центрифугированием образовавшихся при предварительном нагревании молока до (75оС) неустойчивых белковых агрегатов и коллоидного фосфата кальция, а также высокотемпературная пастеризация смеси перед сгущением с целью образования устойчивых комплексов между ККФК и основными сывороточными белками.
Лактоза. В процессе сгущения концентрация лактозы, как и других компонентов возрастает, однако, она остается в растворенном состоянии и существенно не влияет на свойства сгущенного продукта. При длительном воздействии высоких температур в процессе сгущения создаются условия для альдольно-аминной полимеризации ее с белками. Реакция протекает при взаимодействии аминогрупп лизина, входящего в состав белков, и альдегидных групп глюкозы и лактозы с образованием меланоидинов - коричневоокрашенных соединений, обусловливающих изменение цвета продукта от светло-кремового до темно-бурого. Начавшаяся в процессе сгущения реакция может протекать и при последующем хранении продуктов с нарушением температурных режимов.
Вследствие меланоидинообразования изменяются не только цвет продуктов, но и его вкусовые характеристики, за счет образования побочных продуктов реакций, консистенция (загустевание продукта при полимеризации казеинового комплекса), а также снижается их биологическая ценность из-за потери незаменимой аминокислоты лизина, аминогруппы которой вступают в реакцию полимеризации. Потери лизина могут составлять до 20% в производстве сгущенного молока и до 15% при выработке сухого молока.
Как уже отмечалось, при сгущении повышается концентрация лактозы, ее раствор переходит в состояние, близкое к насыщенному. При последующем охлаждении концентрата часть лактозы выкристаллизовывается. С учетом физико-химических свойств изомерных форм лактозы (см. тему 7, раздел 7.2. «Структура лактозы, ее изомерные формы и физические свойства») в первую очередь кристаллизуется α-форма, имеющая более низкую растворимость по сравнению с β-формой. Из-за выделения из раствора α-гидратной формы лактозы нарушается равновесие между изомерными формами и часть β-формы переходит в α-форму. Вследствие недостаточного пресыщения лактозой скорость образования зародышей кристаллов будет замедленной. При последующем охлаждении сгущенного молока скорость роста кристаллов на базе уже образовавшихся зародышей кристаллов будет превышать образование центров кристаллизации. Это может привести к увеличению размеров кристаллов до 20…25 мкм и появлению мучнистой и песчанистой консистенции продукта.
С целью предотвращения возможности появления такого порока в ходе технологических процессов создают условия для преобладания скорости образования зародышей кристаллов над скоростью их роста. В качестве зародышей будущих кристаллов вносят мелкокристаллическую лактозу (затравку) и регулируют режим охлаждения продукта.
В процессе сушки частично кристаллизуется β-форма лактозы, а большая часть ее переходит в аморфное состояние. Аморфное состояние лактозы обусловливает высокую гигроскопичность сухих молочных продуктов. В процессе их хранения может происходить кристаллизация и переход β-лактозы в α-гидратную форму, что ухудшает свойства сухих молочных продуктов.
Молочный жир. В процессах сгущения, гомогенизации сгущенной смеси, распыления сгущенного молока и сушки происходит повышение степени дисперсности жировой фазы: увеличение количества жировых шариков и их общей поверхности. При таких условиях не исключена возможность частичной дестабилизации жировой фазы и появления свободного жира, который в значительной степени подвержен окислительным воздействиям, что снижает стойкость продуктов при хранении.
При сгущении и сушке происходит частичный гидролиз триацилглицеринов молочного жира с накоплением летучих жирных кислот, образованием лактонов, карбонильных соединений, участвующих в формировании свойственных пастеризованному молоку вкуса и аромата продуктов. При такой обработке снижается содержание в молочном жире ненасыщенных жирных кислот.
С целью сохранения стабильности жировой фазы обеспечивают строгий контроль всех режимов и параметров сгущения и сушки, а для предупреждения окислительных процессов допускается вносить антиоксиданты.
Витамины. В производстве сгущенных и сухих продуктов происходят потери витамина А до 20%, а витамин Е достаточно стойкий к технологическим воздействиям. Некоторое снижение его по сравнению с содержанием в исходном молоке обусловлено в основном пастеризацией.
В процессе сгущения и сушки не происходит значительных изменений в содержании большинства водорастворимых витаминов: тиамина (В1), биотина (Н), пантотеновой кислоты (В3), рибофлавина (В2), а содержание фолиевой кислоты в сгущенном и сухом молоке повышается. Объясняется это высвобождением связанных форм витамина под влиянием температурной обработки.
Менее стоек при сгущении и сушке кобаламин (В12), потери которого могут достигать более 40%, пиридоксин (В6) – от 30 до 40%, по некоторым данным до 90% при сушке. Потери аскорбиновой кислоты при сгущении составляют от 17 до 26%, а при последующем высушивании достигают 60%.
13.2. Биохимические изменения составных компонентов
молока при его переработке
Направленное регулирование биохимических превращений составных компонентов молока: углеводов, белков, липидов за счет использования бактериальных ферментов заквасочных культур микроорганизмов, а также промышленных ферментных препаратов положено в основу производства различных молочных продуктов и сыров. Молоко представляет собой идеальную питательную среду для микроорганизмов, обмен веществ которых обусловливает ферментативный гидролиз углеводов – гликолиз, белков – протеолиз и липидов – липолиз, а также последующие ферментативные превращения продуктов их гидролиза. В результате ферментативных превращений составных компонентов молока образуются вкусовые и ароматические вещества, формирующие специфические органолептические характеристики продуктов. Следует иметь ввиду, что ферментативные превращения начинаются в процессе хранения сырого молока и их направленность зависит от качественного состава микрофлоры сырого молока.
13.2.1. Брожение молочного сахара. Виды брожения
В основе производства большой группы кисломолочных продуктов, сыров лежат процессы глубокого распада молочного сахара под действием ферментных систем микроорганизмов, называемые брожением. В некоторых случаях процессы брожения лактозы являются причиной порчи молочных продуктов: излишняя кислотность, избыточное газообразование и др. В зависимости от накопления конечных продуктов распада, обусловленного видом микроорганизмов и их ферментными системами, различают несколько типов брожения молочнокислое гомоферментативное и гетероферментативное, спиртовое, уксуснокислое, пропионовокислое. На начальном этапе все виды брожения протекают по одинаковой схеме до промежуточной стадии – образование пирувата. Исключение составляет гетероферментативное молочнокислое брожение.
На первом этапе под действием фермента β-галактозидазы (лактазы) происходит гидролиз лактозы на глюкозу и галактозу.
Лактоза
+ Н2О
![]()
Продукты гидролиза глюкоза и галактоза далее подвергаются брожению под действием ферментных систем микроорганизмов. Распад глюкозы и галактозы начинается с их фосфорилирования посредством АТФ и при участии ферментов гексокиназы и галактокиназы.
Глюкоза + АТФ ![]()
Галактоза +АТФ ![]()
Под действием ферментов и при участии уридиндифосфатглюкозы (УДФГ) галактозо-1-фосфат переходит в глюкозо-1-фосфат, а затем в глюкозо-6-фосфат.
Галактозо-1-фосфат+УДФГ![]()
Таким образом, галактоза непосредственно не сбраживается, она переходит последовательно в глюкозо-1-фосфат, затем после изомеризации в глюкозо-6-фосфат, который включается в схему ферментативных превращений глюкозы.
Процесс молочнокислого брожений каждой гексозы молочного сахара выражается суммарным уравнением
С6Н12О6 + 2Фн + 2 АДФ → 2С3Н6О3 + 2 АТФ + Н2О
Наряду с молочной кислотой могут образовываться и побочные продукты брожения.
Молочнокислые бактерии по характеру продуктов сбраживания глюкозы относят к гомоферментативным или гетероферментативным. Гомоферментативные бактерии образуют главным образом молочную кислоту (более 90% всех продуктов брожения), а гетероферментативные бактерии около 50% глюкозы превращают в молочную кислоту, а остальное количество – в этиловый спирт, уксусную кислоту и углекислый газ. Однако провести строгую границу между гомо- и гетероферментативными молочнокислыми бактериями по образующимся продуктам брожения иногда бывает трудно. Так, отмечены факты образования отдельными штаммами гомоферментативных молочнокислых бактерий от 8 до 30% побочных продуктов, а гетероферментативные бактерии под воздействием ряда факторов могут вести себя как гомоферментативные.
Более характерным признаком при делении молочнокислых бактерий на группы является путь сбраживания глюкозы. Гомоферментативные бактерии: молочнокислые стрептококки Lac.lactis, Lac.cremoris, Lac.diacetylactis и др., термофильные и мезофильные молочнокислые палочки Lbm.acidophilum, Lbm.bulgariсum, Lbm.casei и др. сбраживают глюкозу по гликолитическому пути Эмбдена-Мейергофа.
Гомоферментативное молочнокислое брожение. Механизм гомоферментативного молочнокислого брожения глюкозы изучен достаточно подробно. Превращение глюкозы в пировиноградную кислоту в результате ряда последовательных реакций происходит при участии десяти ферментов по схеме, представленной на рис.13.1. На заключительной стадии пировиноградная кислота восстанавливается до молочной кислоты под действием фермента лактатдегидрогеназы. Роль восстановительного агента при этом выполняет НАД·Н2, образовавшийся в результате окисления глицеральдегид-3-фосфата (рис.13.1).
СН3СОСООН + НАД·Н2 ↔ СН3СНОНСООН + НАД`
Следовательно, при гомоферментативном молочнокислом брожении из 1 моля глюкозы образуются 2 моля молочной кислоты (с одновременным синтезом 2 молей АТФ). Молочная кислота может быть не единственным конечным продуктом гомоферментативного молочнокислого брожения. Ход брожения может изменяться в зависимости от конкретных условий процесса: наличия углекислого газа и кислорода, рН и температуры среды и др. При этом в качестве побочных продуктов могут образовываться летучие и нелетучие органические кислоты, глицерин, спирты, ацетон, ацетоин, диацетил и др. Однако содержание побочных продуктов при гомоферментативном молочнокислом брожении невелико.
Гетероферментативное молочнокислое брожение. Бактерии группы лейконостоков (Leuc.citrovorus, Leuc.dextranicum), а также гетероферментативные молочнокислые палочки (Lbm.brevis, Lbm.plantarum и др.) не могут сбраживать глюкозу по гликолитичес-
Глюкоза
 1 АТФ
1 АТФ
АДФ
Г люкозо-6-фосфат
люкозо-6-фосфат
2
Фруктозо-6-фосфат
 3 АТФ
3 АТФ
АДФ
Фруктозо-1,6-дифосфат

 4
4
5


 Глицеральдегид-3-фосфат Диоксиацетонфосфат
Глицеральдегид-3-фосфат Диоксиацетонфосфат
НАД` (2) 6 +Фн (2)
НАД·Н2 (2)
1 ,3-Дифосфоглицерат
(2)
,3-Дифосфоглицерат
(2)
 7 АДФ (2)
7 АДФ (2)
АТФ (2)
3-Фосфоглицерат (2)
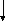 8
8
2-Фосфоглицерат (2)
 9 -Н2О
9 -Н2О
Фосфоенолпируват (2)
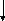 10 АДФ
(2)
10 АДФ
(2)
АТФ (2)
Пируват (2)
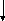 11
11

L(D)-лактат (2)
Рис. 13.1. Схема расщепления глюкозы молочнокислыми бактериями по гликолитическому пути
Примечание. Цифры на схеме обозначают ферменты, катализирующие реакции: 1-гексокиназа; 2-глюкозофосфатизомераза; 3-фосфофруктокина-за; 4-альдолаза; 5-триозофосфатизомераза; 6-глицеральдегид-фосфатдегидрогеназа; 7-фосфоглицераткиназа; 8-фосфоглицеро-мутаза; 9-енолаза; 10-пируваткиназа; 11-лактатдегидрогеназа.
кому пути вследствие отсутствия у них ключевого фермента альдолазы, необходимого для расщепления фруктозо-1,6-дифосфата на две молекулы триозофосфата. Расщепление глюкозы под действием ферментных систем гетероферментных бактерий происходит пентозофосфатным путем по схеме, представленной на рисунке 13.2.
Глюкоза

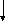 1 АТФ
1 АТФ
АДФ
Г люкозо-6-фосфат
люкозо-6-фосфат
НАДФ`
Н
 АДФ·Н2
АДФ·Н2
6-Фосфоглюканат
