
- •Часть I. Механизмы хранения и реализации генетической информации 17
- •Предисловие автора
- •Часть I. Механизмы хранения и реализации генетической информации введение
- •Средний размер гаплоидного генома у некоторых групп организмов
- •Гены и хромосомы
- •Геном прокариот
- •Геном вирусов
- •Нуклеоид бактериальной клетки
- •Геном архебактерий
- •Минимальный размер генома одноклеточных организмов
- •Геном эукариот
- •Последовательности нуклеотидов эукариотического генома
- •Хроматин
- •Свойства гистонов животных
- •Роль днк-топоизомераз в обеспечении структуры и функционирования хроматина
- •Реализация генетической информации при экспрессии генов
- •Транскрипция
- •Днк-зависимые рнк-полимеразы
- •Характеристики белковых компонентов холофермента рнк-полимеразы II дрожжей
- •Единицы транскрипции (транскриптоны)
- •Этапы транскрипции
- •Субъединичный состав и характеристика основных факторов транскрипции (gtf) рнк-полимеразы II человека
- •Основные факторы элонгации рнк-полимеразы II
- •Хроматин во время транскрипции
- •Субъединичный состав и свойства белковых комплексов Swi/Snf и nurf
- •Котранскрипционные и посттранскрипционные модификации рнк
- •Процессинг рнк у бактерий
- •Редактирование пре-мРнк
- •Различные способы редактирования мРнк
- •Редактирование рнк у животных и их вирусов
- •Другие модификации эукариотических мРнк
- •Сравнение полиаденилирования мРнк у эукариот и прокариот
- •5’-Концевой сайт Точка 3’-Концевой сайт
- •5’–Экзон 1guaugu__...__uacuaac__...__(Py)nAgэкзон 2–3’
- •Механизм прямой и обратной реакций аутосплайсинга интронов группы I
- •Кэп-связывающий комплекс в роли фактора, сопрягающего основные реакции метаболизма транскриптов рнк-полимеразы II
- •Функциональная компартментализация ядра
- •Интерфазные хромосомы в ядре
- •Ядрышко
- •Пространственная организация синтеза мРнк
- •Ядерные тельца и домены
- •Компартментализованное ядро
- •Биосинтез белка рибосомами бактерий
- •Рибосомы
- •Этапы биосинтеза белка
- •Антибиотики, действующие на уровне трансляции
- •Трансляция у эукариот
- •Особенности первичной структуры эукариотических мРнк
- •Инициация биосинтеза белка эукариотическими рибосомами
- •Элонгация полипептидных цепей
- •Терминация трансляции
- •Трансляция в митохондриях
- •Трансляция в хлоропластах.
- •Основные пути регуляции экспрессии генов
- •Регуляция экспрессии генов на уровне транскрипции у прокариот
- •Регуляция на уровне инициации транскрипции
- •Регуляция синтеза рнк на уровне элонгации и терминации
- •Регуляция экспрессии генов на уровне транскрипции у эукариот
- •Передача сигнала и вторичные мессенджеры
- •Рецепторы мембран, осуществляющие трансмембранный перенос сигнала
- •Механизмы позитивной регуляции транскрипции
- •Классификация факторов транскрипции
- •Функциональные домены факторов транскрипции
- •Механизмы негативной регуляции транскрипции
- •Структура хроматина как специфический регулятор экспрессии генов
- •Импринтинг
- •Метилирование днк в регуляции транскрипции
- •Факторы транскрипции позвоночных, на активность которых оказывает влияние метилирование остатков цитозина в узнаваемых ими регуляторных последовательностях нуклеотидов
- •Посттранскрипционная регуляция экспрессии генов
- •Направленный транспорт, внутриклеточная локализация и депонирование мРнк
- •Сплайсинг рнк в регуляции экспрессии генов
- •Избирательная деградация мРнк
- •Регуляция экспрессии генов на уровне трансляции
- •Регуляция инициации трансляции
- •Регуляция элонгации синтеза полипептидных цепей
- •Регуляция терминации трансляции
- •Синтез белков, содержащих остатки селеноцистеина
- •Посттрансляционная регуляция экспрессии генов
- •Последствия фолдинга вновь синтезированных полипептидных цепей
- •Специфические протеиназы в посттрансляционном процессинге белков
- •Убиквитин-зависимая система протеолиза в регулируемой деградации белков
- •Сплайсинг белков
- •Другие посттрансляционные модификации белков
- •Воспроизведение генетической информации
- •Репликация днк
- •Белки, участвующие в репликации днк
- •Белки, входящие в состав репликативных комплексов прокариотических и эукариотических организмов
- •Репликативная вилка e. Coli и бактериофага t4
- •Особенности функционирования репликативной вилки эукариот
- •Эукариотические днк-полимеразы и их функциональные гомологи у прокариот
- •Регуляция репликации днк
- •Инициация репликации днк у e. Coli и ее регуляция
- •Регуляция репликации плазмиды ColE1
- •Особенности репликации линейных геномов
- •Линейные хромосомы бактерий
- •Репликаторы эукариот
- •Репликация теломерных участков эукариотических хромосом
- •Пространственная организация синтеза днк у эукариот
- •Защита генетической информации
- •Мутации
- •Основные источники мутаций и методы определения мутагенной активности
- •Основные классы алкилирующих агентов
- •Метаболиты нормальной микрофлоры человека, обладающие мутагенной и канцерогенной активностями
- •Sos-мутагенез у бактерий
- •Мутаторный фенотип
- •Экспансия днк
- •Адаптивные мутации
- •Механизмы защиты генома от мутаций
- •Репарация днк
- •Основные механизмы репарации поврежденной днк
- •Эксцизионная репарация в клетках животных
- •Днк-гликозилазы и эндонуклеазы клеток микроорганизмов и человека, участвующие в ber
- •Белки животных, участвующие в ner
- •Гомологичная рекомбинация в репарации днк
- •Репарация ошибочно спаренных нуклеотидов
- •Полимераза поли(adp-рибозы) в репарации днк у эукариот
- •Альтруистичная днк
- •Парадокс возможности существования многоклеточных организмов
- •Повышение информационной стабильности генома избыточными последовательностями
- •Селективная защита генов от мутаций
- •Высокоупорядоченное расположение летальных генов на хромосомах
- •Возможный смысл парадокса с
- •Современная концепция гена
- •Часть II основные направления развития прикладной молекулярной генетики Введение
- •Часть II. Искусственные генетические системы
- •Принципы генной инженерии
- •Основные ферменты, используемые в генной инженерии
- •Рестриктазы и днк-метилазы
- •Эффективность расщепления коротких последовательностей днк некоторыми распространенными рестриктазами
- •Днк- и рнк-лигазы
- •Ферменты матричного синтеза днк и рнк
- •Частота ошибок при синтезе днк, осуществляемом термостабильными днк-полимеразами in vitro при проведении пцр в оптимальных условиях
- •Другие ферменты
- •Векторы
- •Плазмидные векторы
- •Векторы на основе фага
- •Космиды и фазмиды
- •Сверхъемкие векторы yac, bac и pac
- •Интегрирующие и челночные (бинарные) векторы
- •Конструирование экспрессирующих векторов и их функционирование
- •Векторы для переноса днк в клетки животных и растений
- •Клонотеки генов
- •Получение клонотек генов
- •Введение рекомбинантных днк в клетки
- •Методы скрининга клонотек генов
- •Эукариотические системы экспрессии рекомбинантных генов, основанные на культурах клеток
- •Клетки яичников китайских хомячков (линия cho)
- •Клетки мышиной миеломы (линия Sp2/0)
- •Клетки селезенки мышей (линия mel)
- •Клетки африканской зеленой мартышки (линия cos)
- •Клетки насекомых, зараженные бакуловирусами
- •Сравнение эффективности рассмотренных систем экспрессии
- •Бесклеточные белоксинтезирующие системы
- •Прокариотические системы
- •Эукариотические системы
- •Проточные системы
- •Другие современные методы исследования генов
- •Рестрикционное картирование генов
- •"Прогулки и прыжки по хромосомам"
- •S1-картирование рнк и днк
- •Футпринтинг
- •Стратегия выделения нового гена
- •Направленный мутагенез и белковая инженерия
- •Методы направленного получения мутаций
- •Получение делеций и вставок
- •Химический мутагенез
- •Сайт-специфический мутагенез с использованием олигонуклеотидов
- •Полимеразная цепная реакция в направленном мутагенезе
- •Белковая инженерия
- •Библиотеки пептидов и эпитопов
- •Белки-репортеры в гибридных белках
- •Гибридные токсины
- •Подходы к созданию новых ферментов
- •Субтилигаза в лигировании пептидов
- •Концепция ксенобиоза
- •Антисмысловые рнк, рибозимы и дезоксирибозимы
- •Антисмысловые рнк и олигонуклеотиды
- •Механизм действия антисмысловых рнк
- •Использование антисмысловых рнк
- •Влияние экспрессии антисмысловых рнк на фенотип трансгенных мышей
- •Природные антисмысловые рнк
- •Антисмысловые рнк и патология: возможный механизм возникновения доминантных мутаций
- •Рибозимы и дезоксирибозимы
- •Типы рибозимов
- •Свойства рибозимов
- •Рибозимы как лекарственные средства
- •Репарация мутантных рнк с помощью рибозимов, осуществляющих транс-сплайсинг
- •Дезоксирибозимы
- •Аптамеры
- •Молекулы рнк у истоков жизни
- •Молекулы рнк в качестве рнк-репликаз
- •Возможность синтеза полипептидных цепей молекулами рнк
- •Трансгенные животные и растения
- •Способы получения трансгенных многоклеточных организмов
- •Экспрессия трансгенов
- •Использование трансгенов у животных
- •Исследование механизмов экспрессии генов
- •Токсигены в исследовании дифференцировки соматических клеток в онтогенезе
- •Изменение физиологического статуса лабораторных и сельскохозяйственных животных
- •Моделирование наследственных и приобретенных заболеваний человека
- •Трансгенные растения
- •Генотерапия наследственных и приобретенных заболеваний
- •Способы доставки новых генов в геном человека
- •Управление экспрессией трансгенов в клетках-мишенях
- •Современные достижения генотерапии онкологических заболеваний
- •Ближайшие перспективы использования генотерапии
- •Успехи генотерапии в модельных экспериментах
- •Проблемы, возникающие в связи с практическим применением генотерапии
- •Днк-диагностика и днк-типирование
- •Днк-диагностика наследственных и приобретенных заболеваний
- •Получение клинического генетического материала
- •Диагностика заболеваний
- •Днк-типирование
- •Днк-типирование микроорганизмов
- •Идентификация личности на основе минисателлитной днк: определение отцовства
- •Микроматрицы и микрочипы днк
- •Методы создания микроматриц днк
- •Ограничения в использовании микроматриц днк
- •Использование микроматриц днк в фундаментальных и прикладных исследованиях
- •Картирование и определение первичной структуры генома человека
- •Основные подходы к картированию генома человека
- •Генетические карты сцепления
- •Современные методы построения генетических карт сцепления
- •Пцр в исследованиях генома человека
- •Физические карты низкого разрешения
- •Физические карты высокого разрешения
- •Определение полной первичной структуры днк генома человека
- •Базы данных получаемой информации
- •Заключение
- •Рекомендуемая литература
Рестрикционное картирование генов
Полную, но, к сожалению, пока трудно интерпретируемую информацию о строении гена может дать только определение его первичной структуры, т.е. последовательности составляющих ген нуклеотидов. На практике при исследовании протяженных (до 40 т.п.о.) клонированных последовательностей нуклеотидов, включающих исследуемые гены, прежде всего строят их рестрикционные карты. Рестрикционные карты представляют собой схемы, изображающие взаимное расположение сайтов рестрикции для разных рестриктаз и расстояния между ними. Поскольку каждый сайт рестрикции является не чем иным, как строго определенной последовательностью нуклеотидов ДНК, рестрикционные карты наглядно заключают в себе информацию об особенностях первичной структуры картируемых участков генома.
Для построения рестрикционной карты используют гибридизацию по методу Е. Саузерна. Клонированный фрагмент ДНК отдельно или в составе вектора получают в препаративном количестве, затем его обрабатывают соответствующими рестриктазами и продукты рестрикции разделяют электрофорезом в агарозном геле. Количество образовавшихся рестрикционных фрагментов ДНК, обнаруживаемых после окрашивания бромистым этидием в виде флуоресцирующих полос в ультрафиолетовом свете, соответствует количеству сайтов рестрикции в том случае, если различия в размерах образовавшихся фрагментов ДНК достаточны для их разделения при электрофорезе.
Размеры рестрикционных фрагментов оценивают путем сравнения их электрофоретической подвижности с таковой фрагментов ДНК известных размеров. Получив информацию о количестве сайтов рестрикции в гене, далее определяют их взаимное расположение. Для этого в качестве зондов выбирают короткие фрагменты ДНК и после введения в них радиоактивной метки их гибридизуют с рестрикционными фрагментами ДНК, которые после электрофоретического разделения в агарозном геле были перенесены на нитроцеллюлозные или нейлоновые фильтры. По завершении гибридизации положение фрагментов ДНК, связавших метку, на фильтрах обнаруживают с помощью авторадиографии. Получение такой информации о принадлежности конкретных фрагментов ДНК, образовавшихся под действием различных рестриктаз, к 5’- или 3’-концевым частям исследуемой последовательности нуклеотидов обычно бывает достаточным для определения взаимного расположения различных сайтов рестрикции на рестрикционных картах.
"Прогулки и прыжки по хромосомам"
Многие гены в геноме эукариот располагаются в виде кластеров, члены которых функционально или эволюционно связаны друг с другом. В связи с этим в молекулярной генетике часто возникает задача клонирования генов, расположенных по соседству с уже выделенными генами. Для ее решения был разработан метод "прогулки по хромосоме". Из клонотеки генов, полученной на основе фаговых или космидных векторов, выделяют ген и короткие 5’- и 3’-концевой фрагменты его последовательности используют в качестве зондов для поиска фрагментов ДНК, перекрывающихся с этим геном. Основным требованием, предъявляемым к зонду, является принадлежность его к уникальной последовательности нуклеотидов, т.е. встречающейся в геноме только один раз. С использованием такого простого подхода были исследованы многие кластеры эукариотических генов, в частности -глобинового локуса человека, структура которого представлена на рис. II.14.

Рис. II.14. Генетическая карта локуса -глобинового гена человека, полученная методом "прогулки по хромосоме"
Перекрывающиеся фрагменты геномной ДНК человека получены путем ее частичного расщепления рестриктазой EcoRI, сайты рестрикции для которой отмечены поперечными черточками. Указаны расстояния междуEcoRI-сайтами рестрикции в т.п.о., гены-глобинового локуса, а также названия рекомбинантных фагов
С помощью "прогулки по хромосоме" удается детально картировать участки ДНК длиной до 250 т.п.о. Недавно разработанный метод "прыжков по хромосоме" позволяет стыковать за один прием фрагменты ДНК общей длиной от 100 до 500–1000 т.п.о. В этом случае на первом этапе препарат высокомолекулярной ДНК расщепляют соответствующей рестриктазой и с помощью электрофореза в импульсном электрическом поле получают фракцию фрагментов ДНК одинакового размера (в данном примере ~100 т.п.о.) (см. рис. II.15). Затем фрагменты ДНК лигируют с маркерным геном, например геном устойчивости к антибиотикам, что приводит к образованию кольцевых молекул. Кольцевые молекулы ДНК расщепляют другой рестриктазой, для которой отсутствуют сайты рестрикции в маркерном гене, что сопровождается образованием коротких фрагментов ДНК, которые далее можно клонировать обычными способами. Полученную клонотеку фрагментов ДНК исследуют с использованием гибридизации с зондом, комплементарным точке начала "прыжка по хромосоме". Отобранные в результате гибридизации клоны содержат маркерный ген, фланкированный изучаемыми последовательностями нуклеотидов, удаленными друг от друга на 100 т.п.о. Таким образом, получают информацию о последовательностях нуклеотидов, удаленных от точки начала "прыжка по хромосоме" на 100 т.п.о., и эти последовательности далее используют в качестве зонда для выделения и исследования фланкирующих ее фрагментов ДНК.
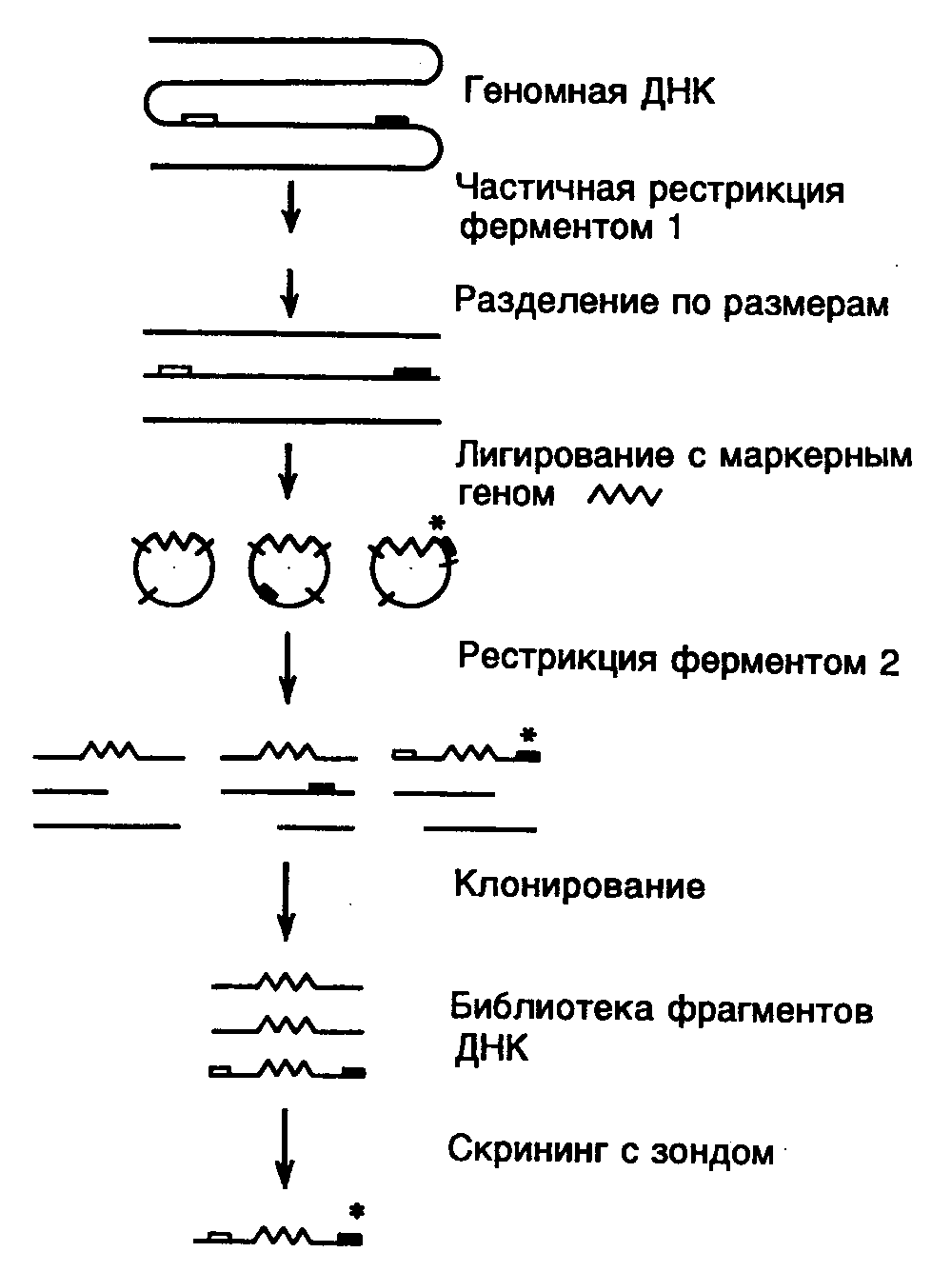
Рис. II.15. Схема метода "прыжков по хромосоме"
