
- •Вопрос 1.Основные понятия термодинамики.
- •Вопрос 2. Первое начало термодинамики.
- •Вопрос 3. Второе начало термодинамики.
- •Вопрос 4. Термодинамические условия равновесия.
- •Вопрос 6. Предмет и основные понятия химической кинетики.
- •Вопрос 7. Зависимость скорости реакции от концентрации.
- •Вопрос 8. Зависимость скорости химической реакции от температуры.
- •Вопрос 9. Катализ.
- •Вопрос 10. Кислоты и основания.
- •Вопрос 12. Коллигативные свойства разбавленных растворов неэлектролитов и электролитов.
- •Второй закон Рауля
- •Вопрос 13. Элементы теории растворов электролитов.
- •Вопрос 14. Электрическая проводимость растворов.
- •Вопрос 15. Кондуктометрия. Использование кондуктометрических измерений в медицине и биологии.
- •Вопрос 16. Осмос.
- •Вопрос 17. Растворимость газов в жидкостях и ее зависимость от различных факторов.
- •Вопрос 21. Буферные системы крови: гидрокарбонатная, фосфатная, гемоглобиновая, протеиновая.
- •Белковая буферная система. В сравнении с другими буферными системами имеет меньшее значение для поддержания кислотно-основного равновесия.
- •Гемоглобиновая буферная система.
- •Вопрос 22. Гетерогенные реакции в растворах электролитов.
- •Вопрос 23. Механизм функционирования кальций-фосфатного буфера.
- •Вопрос 24. Строение комплексных соединений.
- •Вопрос 25. Константа нестойкости комплексного иона.
- •Вопрос 26. Представление о строении металлферментов и других биокомплексных соединений.
- •Вопрос 27. Окислительно-восстановительные реакции.
- •Вопрос 28. Константа окислительно-восстановительного процесса.
- •Вопрос 29. Адсорбционные равновесия и процессы на подвижных границах раздела.
- •Вопрос 30. Адсорбционные равновесия на неподвижных границах раздела фаз.
- •Вопрос 31. Классификация дисперсных систем.
- •Вопрос 32. Лигандные, гетерогенные и протолитические равновесия с участием важнейших биогенных элементов (примеры).
- •Вопрос 33. Устойчивость дисперсных систем.
- •Вопрос 34. Свойства растворов вмс.
- •Вопрос 35. Осмотическое давление растворов биополимеров.
- •Вопрос 36. Устойчивость растворов биополимеров.
- •Вопрос 37. Титриметрический анализ.
- •Вопрос 38. Окислительно-восстановительное титрование.
- •Вопрос 39. Комплексонометрическое титрование: комплексонометрия.
- •Вопрос 40. Потенциометрия.
Вопрос 28. Константа окислительно-восстановительного процесса.
Формула есть: lgK = (E0окис-E0восст)*z/0,059 K - константа равновесия z - число электронов, равное наименьшему кратному из числа электронов, отданных восстановителем и принятых окислителем.
Константа
равновесия должна быть тем больше, чем
больше разность стандартных потенциалов
обеих пар. Если эта разность достаточно
велика, т. е. ![]() ,
реакция идет практически до конца.
Наоборот, при малой разности потенциалов
химическое превращение взаимодействующих
веществ до конца не пойдет, если не
создать условий, которые будут
способствовать смещению равновесия в
нужном направлении.
,
реакция идет практически до конца.
Наоборот, при малой разности потенциалов
химическое превращение взаимодействующих
веществ до конца не пойдет, если не
создать условий, которые будут
способствовать смещению равновесия в
нужном направлении.
Окислитель — вещество, в состав которого входят атомы, присоединяющие во время химической реакции электроны, иными словами, окислитель — это акцептор электронов.
Восстановитель - это вещество или химический элемент, отдающие электроны в окислительно-восстановительной реакции.
Токсическое действие нитратов заключается в том, что в пищеварительном тракте они частично восстанавливаются до нитритов(более токсичных), и последние при поступлении в кровь могут вызвать метгемоглобинемию, а также подавление активности ферментных систем, участвующих в процессах тканевого дыхания. Кроме того, установлено, что из нитритов в присутствии аминов могут образовываться N-нитрозамины, которые проявляют канцерогенной активностью.
Токсическое действие нитритов в человеческом организме проявляется в форме метгемоглобинемии. Нитрози-лионы окисляют двухвалентное железо гемоглобина в трехвалентное. В результате такого окисления гемоглобин, имеющий красную окраску, превращается в метгемоглобин, который уже имеет темно-коричневую окраску. Метгемоглобин блокирует центры переноса кислорода. В крови возрастает содержание молочной кислоты, холестерина, лейкоцитов, снижается количество белков.
В определенных условиях нитриты, взаимодействуя с вторичными и третичными аминами, образуют нитрозамины - вещества, являющиеся канцерогенами. При нормальном физиологическом со стоянии в организме образуется примерно 2% метгемоглобина, поскольку редуктазы красных кровяных телец (эритроцитов) взрослого человека обладают способностью превращать образовавшийся метгемоглобин снова в гемоглобин.
Детоксикация (мед.) — естественное и искусственное удаление токсинов из организма.
Вопрос 29. Адсорбционные равновесия и процессы на подвижных границах раздела.
Адсорбцией называется самопроизвольное изменение концентрации растворенного вещества на границе раздела фаз.
Поверхностная энергия Гиббса системы пропорциональна межфазной поверхности:
Gs=δs
Gs- поверхностная энергия Гиббса, Дж.
δ-коэффицент пропорциональности, называемый поверхностным натяжением, Дж/м2
s- межфазная поверхность, м2
Адсорбцию на границе раздела жидкость-газ непосредственно не измеряют, а вычисляют с помощью уравнения Гиббса, которое выведено на основании 2-го начала термодинамики:
Г = - dσ/dc*c/RT – уравнение Гиббса.
Где Г- количество адсорбированного вещества, моль/м^2, с – молярная концентрация растворенного вещества, моль/дм^3, R – газовая постоянная , равная 8,32 Дж/ (моль*К),
- dσ/dc – поверхностная активность.
Поверхностное натяжение δесть величина, измеряемая энергией Гиббса, приходящейся на единицу площади поверхностного слоя. Оно численно равно работе, которую необходимо совершить для образования единицы поверхностного раздела фаз при постоянной температуре.
Способность растворенных веществ изменять поверхностное натяжение растворителя называется поверхностной активностью.
Поверхностно-активные и поверхностно-неактивные вещества.
При растворении в данной жидкости какого-либо вещества наблюдают следующие случаи.
1.Растворенное вещество понижает поверхностное натяжение растворителя. Такие вещества называются поверхностно-активные(ПАВ), так как для них g>0. По отношению к воде ПАВ являются многие органические соединения ,например, спирты и кислоты алифатического ряда, сложные эфиры, белки и др.
2.Растворенное вещество незначительно повышает поверхностное натяжение растворителя.
Такие вещества называют поверхностно-инактивными (ПИВ). Для них g<0.К ним относят неорганические кислоты, основания, соли, также органические соединения, глицерин, альфа-аминокислоты.
3.Ратворенное вещество практически не изменяет поверхностного натяжения растворителя.
Такие вещества называют поверхностно-неактивными(ПНВ) .по отношению к воде веществами являются сахароза и др.
Поверхностная активность зависит от природы поверхностно-активного вещества. Согласно правилу Дюкло-Траубе: Поверхностная активность вещества одного и того же гомологического ряда возрастает приблизительно в 3 раза при увеличении углеводородной цепи на одну метиленовую группу -СН2-
Зависимость адсорбции от равновесной концентрации растворенного вещества при постоянной температуре называют изотермой адсорбции.
Ориентация молекул в поверхностном слое и структура биологических мембран.
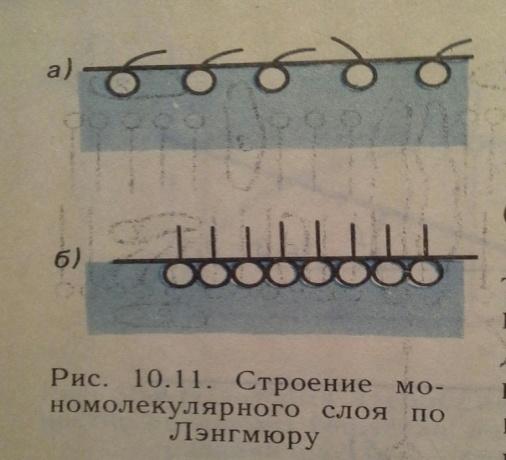
По теории Ленгмюра. Молекулы ПАВ состоят из двух частей: полярной (гидрофильной) и неполярной (гидрофобной). При адсорбции полярная группа, обладающая большим сродством к полярной фазе (например, к воде) втягивается в нее. Неполярная группа выталкивается в неполярную фазу.
При малых концентрациях ПАВ углеводородные радикалы «лежат» на поверхности полярной жидкости, а полярные группировки погружены в нее. 10.11 (а)
С увеличение концентрации ПАВ в растворе число молекул, находящихся в поверхностном слое, возрастает. Это приводит в пределе к образованию на граничной поверхности насыщенного мономолекулярного адсорбционного слоя 10.11 (б), в котором молекулы ПАВ предельно ориентированы. Этот слой образно называют молекулярным частоколом Лэнгмюра.
Основным компонентом мембранных структур клетки является биомолекулярный слой из молекул липидов, полярные группировки которых направлены наружу(они взаимодействуют с белками), а неполярные углеводородные радикалы внутрь. Среди мембранных белков имеются такие, которые способны взаимодействовать с гидрофобными радикалами и проникать внутрь мембран (интегральные белки). Макромолекулы интегральных белков, пронизывающих мембрану могут образовывать поры - ионные каналы, которые обладают избирательной проницаемостью для различных ионов.
