
- •Contents
- •1.1. Радиус-вектор материальной точки
- •1.2.Кинематические уравнения движения материальной точки
- •1.3. Траектория материальной точки
- •1.4.Вектор перемещения
- •1.5. Скорость
- •1.6. Ускорение
- •1.7. Криволинейное движение. Тангенциальное и нормальное ускорения
- •1.8. Методические указания к решению задач по кинематике
- •2. Кинематика вращательного движения. Введение
- •2.1. Угол поворота твердого тела
- •2.2. Угловая скорость
- •2.3. Период и частота обращения
- •2.4. Угловое ускорение
- •2.5. Связь угловых и линейных величин
- •3. Динамика материальной точки и поступательного движения твердого тела
- •3.1. Первый закон Ньютона
- •3.2. Понятие о силе
- •3.3. Масса. Второй закон Ньютона
- •3.4. Принцип независимости действия сил
- •3.5.Третий закон Ньютона
- •3.6 Преобразование координат Галилея и механический принцип относительности
- •3.7.Основное уравнение динамики поступательного движения материальной точки. Импульс материальной точки
- •3.8. Центр инерции системы
- •3.9. Универсальная форма второго закона Ньютона, выраженная через импульс системы
- •3.10. Основное уравнение динамики поступательного движения твердого тела
- •3.11.Изолированная (замкнутая) система. Закон сохранения импульса
- •3.12. Методические указания к решению задач по динамике
- •4. Энергия и работа
- •4.1. Основные понятия об энергии механической системы
- •4.2. Работа
- •4.3. Консервативные силы. Условие потенциальности силового поля
- •4.4. Мощность
- •4.5 Кинетическая энергия
- •4.6.Потенциальная энергия
- •4.7. Закон сохранения и превращения энергии
- •4.8. Связь между потенциальной энергией и силой
- •5.6. Момент импульса материальной точки и твердого тела
- •7.2. Колебания под действием упругой силы (пружинный маятник)
- •7.3. Энергия колеблющегося тела
- •7.4. Основное уравнение гармонических свободных колебаний. (Дифференциальное уравнение гармонических колебаний)
- •7.5. Математический и физический маятники
- •7.6. Сложение механических колебаний
- •7.7.Затухающие колебания
- •7.8. Вынужденные колебания
- •8.1. Распространение волн в упругой среде
- •8.2. Уравнение плоской одномерной волны
- •8.3. Фазовая скорость
- •8.4.Волновая поверхность, фронт волны
- •8.5. Уравнение плоской волны распространяющейся в произвольном направлении
- •8.6. Волновое уравнение
- •8.7. Энергия волны
- •8.8. Объемная плотность энергии волны
- •8.9. Плотность потока энергии. Вектор Умова
- •8.10. Стоячие волны
- •9. Основы термодинамики.Термодинамический и молекулярно – кинетический метод исследования явлений природы
- •9.1. Термодинамическое состояние тела
- •9.2 Внутренняя энергия
- •9.3 Работа газа
- •9.4 Первый закон (начало) термодинамики
- •9.5. Основные понятия о теплоемкости вещества
- •9.7 Изобарический процесс
- •9.8 Изотермический процесс
- •9.9 Адиабатический процесс
- •9.10. Обратимые и необратимые процессы. Круговой процесс
- •9.11 Цикл Карно
- •9.12. Второе начало термодинамики
- •9.13 Приведенная теплота. Равенство (неравенство) Клаузиуса
- •9.14 Теорема Клаузиуса
- •9.15 Энтропия
- •9.16 Свойства энтропии
- •9.17 Физический смысл энтропии
- •10. Основы молекулярно-кинетической теории газов. Введение
- •10.1 Основное уравнение м.К.Т. Идеальных газов. Температура
- •10.2 Распределение энергии по степеням свободы молекулы
- •10.3 Внутренняя энергия идеального газа
- •11. Статистические распределения
- •11.1 Распределение молекул по скоростям
- •11.2 Закон распределения молекул идеального газа во внешнем силовом поле
- •11.3. Распределение давления по высоте
- •11.4. Среднее число столкновений и средняя длина свободного пробега молекул
- •12. Явления переноса. Введение
- •12.1 Диффузия
- •12.2 Теплопроводность
- •12.3. Внутреннее трение
- •13. Основы электростатики
- •13.1. Взаимодействие зарядов Закон Кулона
- •13.2. Электрический диполь
- •13.3. Электростатическое поле. Напряженность поля
- •13.4. Силовые линии электрического поля
- •13.5. Принцип суперпозиции электрических полей
- •13.6. Поток вектора напряженности электростатического поля
- •13.7. Теорема Остроградского - Гаусса
- •13.8. Примеры применения теоремы Гаусса
- •13.9. Работа сил электростатического поля при перемещении заряда
- •13.10. Потенциальная энергия электростатического поля
- •13.11. Циркуляция вектора напряженности
- •13.12. Потенциал электростатического поля
- •13.13. Эквипотенциальные поверхности
- •13.14. Связь между напряженностью и потенциалом
- •13.15.Вычисление потенциала простейших электрических полей
- •14. Электрическое поле в диэлектриках. Введение
- •14.1. Поляризация диэлектриков
- •14.2. Напряженность электрического поля в диэлектрике
- •14.3. Электрическое смещение
- •14.4. Поле на границах раздела диэлектрика
- •15. Проводники в электрическом поле
- •15.1. Равновесие зарядов на проводнике
- •15.2. Напряженность электростатического поля вблизи заряженной поверхности проводника
- •15.3. Проводники во внешнем электрическом поле
- •15.4. Электроемкость проводников
- •15.5. Конденсаторы
- •16. Энергия электрического поля
- •16.1. Энергия системы зарядов
- •16.2. Энергия заряженного уединенного проводника и конденсатора
- •16.3. Объемная плотность энергии электростатического поля
- •17. Электропроводность металлов
- •17.1. Электрический ток
- •17.2. Электродвижущая сила
- •17.3. Закон Ома для участка цепи. Сопротивление проводников
- •17.4. Закон Ома в интегральной форме
- •17.5 Закон Джоуля-Ленца в интегральной и дифференциальной формах
- •17.6. Разветвленные цепи. Правила Кирхгофа
- •18. Классическая теория электропроводности
- •6.4.1. Закон Ома. Закон Джоуля-Ленца.
- •6.4.2. Эффект Холла.
- •6.4.3. Высокочастотная электропроводность металлов.
- •6.4.4. Высокочастотная диэлектрическая проницаемость металлов.
- •18.1. Основы классической электронной теории электропроводности металлов
- •18.2. Вывод закона Ома в дифференциальной форме в классической электронной теории
- •18.3. Вывод закона Джоуля-Ленца в дифференциальной форме в классической теории электропроводности
- •18.4. Связь между теплопроводностью и электропроводностью металлов (закон Видемана-Франца)
- •18.5. Недостатки классической электронной теории проводимости металлов
- •18.6. Работа выхода из металла. Термоэлектронная эмиссия
- •19. Электрический ток в газах
- •19.2. Несамостоятельный газовый разряд
- •19.3. Самостоятельный газовый разряд
9.1. Термодинамическое состояние тела
Термодинамическое
состояние тела (например, газа)
характеризуется его массой ![]() ,
молярной массой μ, давлением
,
молярной массой μ, давлением ![]() ,
объемом
,
объемом ![]() ,
температурой
,
температурой ![]() (а
возможно, и другими величинами, например,
определяющими его химический состав).
Все эти величины называются
термодинамическими параметрами тела.
Однако, как будет видно из дальнейшего,
такие параметры, как
(а
возможно, и другими величинами, например,
определяющими его химический состав).
Все эти величины называются
термодинамическими параметрами тела.
Однако, как будет видно из дальнейшего,
такие параметры, как ![]() ,имеют
смысл только тогда, когда тело находится,
хотя бы приближенно, в так называемом
состоянии термодинамического равновесия
(т.д.р.). Так называется состояние, в
котором все термодинамические параметры
остаются со временем постоянными (к
этому следует добавить еще условие
отсутствия стационарных потоков). Если,
например, быстро подогревать газ, как
это показано на рис. 9.1, температура
непосредственно подогреваемой части
сосуда А окажется выше температуры
части В. Не будут равны и давления в
частях А и В. В этом случае не имеет
смысла понятие температуры
,имеют
смысл только тогда, когда тело находится,
хотя бы приближенно, в так называемом
состоянии термодинамического равновесия
(т.д.р.). Так называется состояние, в
котором все термодинамические параметры
остаются со временем постоянными (к
этому следует добавить еще условие
отсутствия стационарных потоков). Если,
например, быстро подогревать газ, как
это показано на рис. 9.1, температура
непосредственно подогреваемой части
сосуда А окажется выше температуры
части В. Не будут равны и давления в
частях А и В. В этом случае не имеет
смысла понятие температуры ![]() или
давления
или
давления ![]() всего
газа. Другой пример – впустим в газ
пучок быстрых молекул. Ясно, что не имеет
смысла говорить о температуре газа до
тех пор, пока быстрые молекулы, вследствие
ряда столкновений с другими, не приобретут
скоростей порядка средней скорости
остальных молекул, иначе говоря, пока
система не придет в состояние т.д.р.
всего
газа. Другой пример – впустим в газ
пучок быстрых молекул. Ясно, что не имеет
смысла говорить о температуре газа до
тех пор, пока быстрые молекулы, вследствие
ряда столкновений с другими, не приобретут
скоростей порядка средней скорости
остальных молекул, иначе говоря, пока
система не придет в состояние т.д.р.
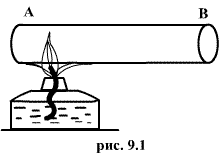
В состоянии т.д.р. для каждого вещества термодинамические параметры связаны между собой так называемым уравнением состояния:
|
|
(9.1) |
Таким уравнением состояния для идеального газа является уравнение Менделеева – Клапейрона:
|
|
(9.2) |
Здесь R=8,31 Дж/(мольК) – универсальная газовая постоянная, μ - молярная масса. Для углерода (С) величина μ составляет 12г, для водорода (H2) – 2г, для кислорода (О2) – 32г, для воды (Н2О) – 18г и т.д.
В моле любого вещества содержится одно и то же количество молекул N0, называемое числом Авогадро:
|
|
(9.3) |
Это объясняется тем, что значение моля любого вещества выбрано пропорциональным массе молекулы этого вещества. Масса молекулы может быть получена делением массы моля на число Авогадро:
|
|
(9.4) |
Отношение универсальной газовой постоянной R к числу Авогадро (т.е. универсальная газовая постоянная, приходящаяся на одну молекулу) называется постоянной Больцмана:
|
|
(9.5) |
В формулу (9.2) входят еще давление, объем, температура и масса газа. Давление Р в системе СИ измеряется в ньютонах на квадратный метр или паскалях (Н/м2=Па), объем V – в кубических метрах (м2), масса m – в килограммах (кг), температура T – в кельвинах (К). Абсолютная температура Т отсчитывается от абсолютного нуля (-273,15°С), т.е. Т=t+273,15, где t – температура по Цельсию.
Если количество вещества равно 1 молю, то (9.2) превращается в
|
|
(9.6) |
Идеальным газом называется газ, настолько разреженный, что он подчиняется уравнению (9.2) или(9.6). Смысл этого определения состоит, очевидно, в том, что для подчинения уравнению (9.6) газ должен быть достаточно разреженным. Если газ, напротив, сжат до достаточно больших плотностей (так называемый реальный газ), то вместо (9.6) имеем
|
|
(9.7) |
Это – уравнение состояния реального газа или уравнение Ван-дер-Ваальса. Здесь a и b – постоянные.
