
- •Федеральное агентство по образованию рф
- •Федеральное агентство по образованию рф
- •Часть I. Общие теоретические сведения курса «основы квантовой механики, атомной и ядерной физики».
- •§1.1. Тепловое излучение. Квантовая природа излучения
- •Формула Планка
- •§1.2. Фотоэффект. Давление света
- •Энергия, масса и импульс фотона. Давление света.
- •§1.3 Двойственная природа электромагнитного излучения вещества
- •Корпускулярно – волновая двойственность свойств света
- •Соотношение неопределенностей Гейзенберга
- •§1.4 Уравнения шредингера. Простейшие случаи движения микрочастиц
- •Условие нормировки вероятностей и самой ψ - функции
- •Уравнение Шредингера
- •В случае, когда -функция не зависит от времени , она удовлетворяетстационарному уравнению Шредингера
- •Одномерное уравнение Шредингера для стационарных состояний
- •Движение свободной частицы
- •Частица в одномерной потенциальной яме бесконечной глубины
- •§1.5 Квантово - механическое описание атома и молекул
- •Принцип Паули
- •Уровни энергии двухатомных молекул
- •§1.6 Физика твердого тела
- •Некоторые сведения о квантовой физике твердых тел
- •Распределение Ферми – Дирака имеет вид
- •Теплоемкость кристаллов по Дебаю
- •Понятие о фононах.
- •§1.7 Ядерная физика
- •Активностью а нуклида (общее название атомных ядер, отличающихся числом протонов z и нейтронов n) в радиоактивном источнике называется число распадов, происходящих с ядрами образца в 1с
- •Условие равновесия изотопов в радиоактивном семействе
- •Часть II. Примеры решения задач
- •§2.1. Тепловое излучение. Квантовая природа излучения
- •Решение
- •Решение Энергия с единицы площади поверхности в единицу времени
- •Решение
- •Решение Вычислим энергию фотона по формуле
- •§2.2. Фотоэффект. Давление света
- •Решение
- •Подстановка числовых значений даёт
- •Решение
- •Решение
- •При комптоновском рассеянии длина волны меняется на величину
- •Импульс выразим через длину волны де Бройля
- •1) Определим неопределенность скорости пылинки. Согласно принципу неопределенностей
- •Подставим в (2.51) числовые значения и найдем значение скорости пылинки
- •§2.4 Уравнения шредингера. Простейшие случаи движения микрочастиц
- •Ответ: .
- •Решение
- •Подставим в (2.55) числовые значения, получим
- •§2.5 Квантово - механическое описание атома и молекул
- •Решение
- •Решение
- •Кинетическая энергия вращения молекулы водорода определяется по формуле
- •Решение
- •§2.6 Физика твердого тела
- •Решение
- •Решение
- •Решение
- •Решение
- •§2.7 Ядерная физика
- •Решение
- •Решение
- •Решение
- •Решение
- •Часть III. Контрольные вопросы и задачи для самоподготовки
- •§3.1. Тепловое излучение. Квантовая природа излучения
- •§3.2. Фотоэффект. Давление света
- •§3.3 Двойственная природа электромагнитного излучения вещества
- •§3.4 Уравнения шредингера. Простейшие случаи движения микрочастиц
- •§3.5 Квантово - механическое описание атома и молекул
- •§3.6 Физика твердого тела
- •§3.7 Ядерная физика
- •Продолжение таблицы а.1
- •Приложение б
- •Приставки к единицам си
- •Некоторые основные физические постоянные
- •Продолжение таблицы б.2
- •Некоторые характеристики Солнца, Земли и Луны
- •Работа выхода (а) электронов из металлов
- •Длины волн некоторых спектральных линий
- •Шкала электромагнитных излучений
- •Изотопный состав элементов
§3.5 Квантово - механическое описание атома и молекул
Что описывает обобщенная формула Бальмера
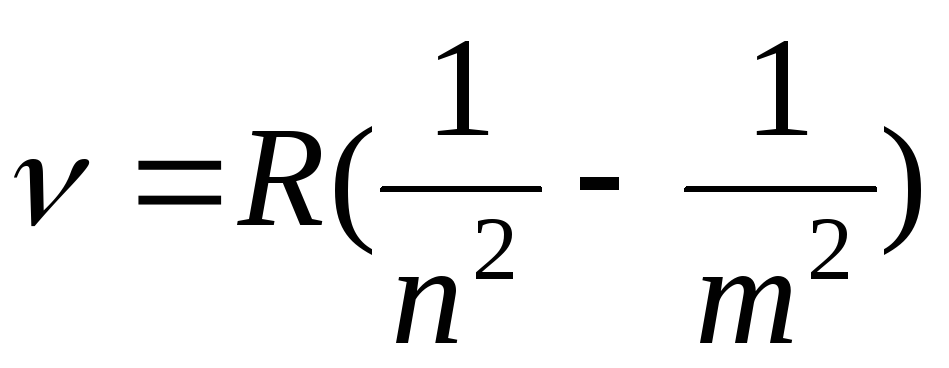 ?
?Получите из этой формулы выражения для видимой, ультрафиолетовой и инфракрасной областей спектра излучения атома водорода. Что означает понятие «серия линий»?
Сформулируйте постулаты Бора. Как осуществляется квантование атома водорода. Опишите с помощью квантовых чисел n, l и m спектр атома водорода. Сформулируйте правило отбора.
Что характеризуют квантовые числа: главное, орбитальное и магнитное? Какие значения они могут принимать? Каковы возможные значения l и m для главного квантового числа n= 5? Сколько различных состояний соответствует n= 4?
Дайте квантово - механическую формулировку принципа Паули. Покажите, что максимальное число электронов, находящихся в состояниях, определяемых главным квантовым числом n, равно 2 n2 .
Что называется гиромагнитным отношением? Чем спиновое гиромагнитное отношение отличается от орбитального? Чему равен магнетон Бора?
В каких случаях обнаруживается тонкая структура спектра? Дайте определение спина как квантового числа. Каков его смысл? Запишите закон квантования спина.
Почему атом водорода может иметь одну и ту же энергию, находясь в различных состояниях?
Какие принципы квантовой физики положены в основу объяснения Периодического закона Менделеева? Опишите заполнение электронных оболочек атомов Н, Не, Li, O, Ne, Si, Ar.
Каков механизм возникновения электронно-колебательных и колебательно-вращательных спектров?
Построить и объяснить диаграмму, иллюстрирующую расщепление энергетических уровней и спектральных линий (с учетом правил отбора) при переходах между состояниями с l = 2 и l = 1.
Электрон в атоме находится в f – состоянии. Определить: 1) момент импульса (орбитальный) Le электрона; 2) максимальное значение проекции момента импульса
 на
направление внешнего магнитного поля.
на
направление внешнего магнитного поля.
Заполненной электронной оболочке соответствует главное квантовое число n=3. Определить число электронов в этой оболочке, которые имеют одинаковые следующие квантовые числа: 1)
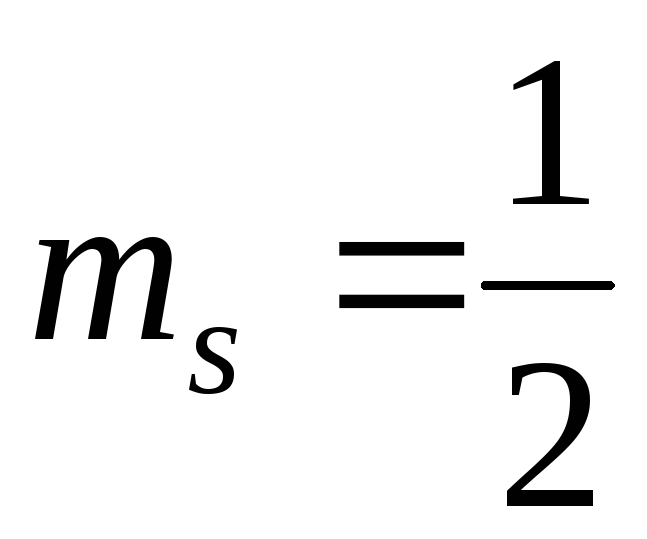 и
и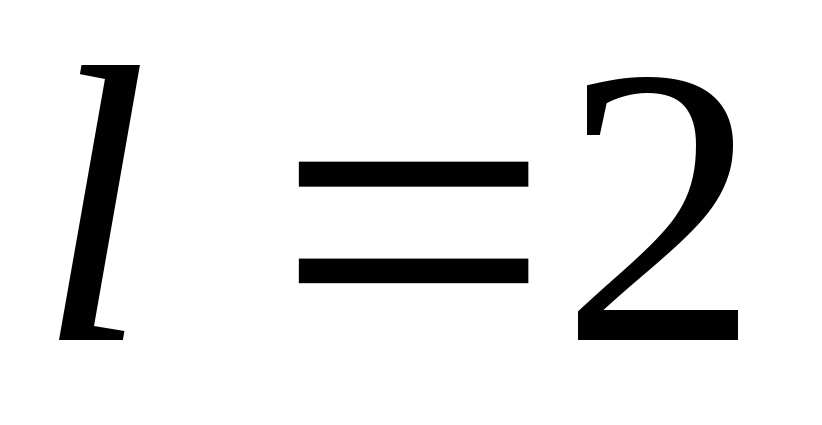 ;
2)
;
2)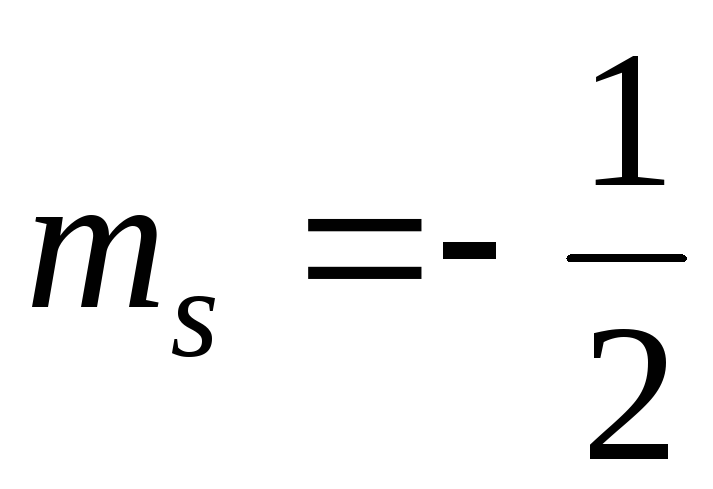 и
и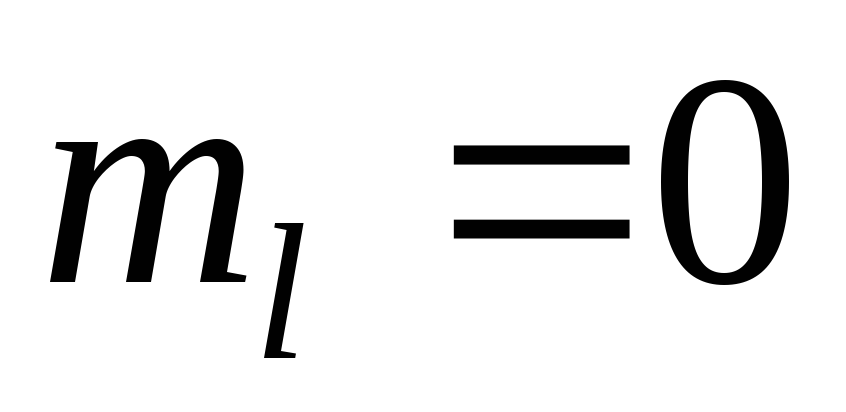 .
.
Пользуясь представлениями модели атома Резерфорда – Бора, вывести формулу скорости движения электрона по орбите. Вычислить ее скорость на двух первых электронных круговых орбитах в атоме водорода.
Электрон движется по второй орбите атома водорода. Найти длину волны де Бройля.
С помощью условий квантования вывести формулу центростремительного ускорения электрона на орбите. Найти их ускорения на двух первых орбитах в атоме водорода.
Во сколько раз увеличится радиус орбиты электрона у атома водорода, находящегося в основном состоянии, при возбуждении его фотоном энергией 12,09 эВ?
Определить границы серии водородных линий, расположенных в далекой ультрафиолетовой части спектра (серия Лаймана).
Наибольшая длина волны спектральной водородной линии серии Лаймана 121,6 нм. Вычислить наибольшую длину волны в серии Бальмера.
Какую работу нужно совершить, чтобы удалить электрон со второй орбиты атома водорода за пределы притяжения его ядром?
Какие спектральные линии появятся в видимой области спектра при возбуждении атомов водорода электронами энергией 13,0 эВ?
