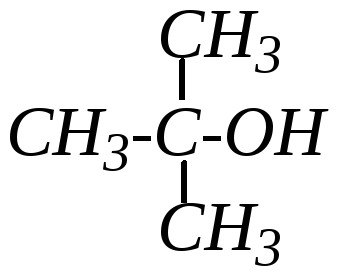- •Глава 3. Функциональные производные алканов
- •3.1. ОбщноСть Химических свойств
- •3.1.1. Реакции нуклеофильного замещения
- •3.1.2. Реакции отщепления (элиминирования)
- •3.2. Галогеналканы
- •3.2.1. Классификация, номенклатура, изомерия
- •3.2.2. Строение и свойства
- •3.2.3. Способы получения
- •3.2.4. Полигалогеналканы
- •3.2.5. Физиологическая роль и Важнейшие представители
- •3.3. Насыщенные спирты
- •3.3.1. Классификация, номенклатура, изомерия
- •3.3.2. Строение и физические свойства
- •3.3.3. Химические свойства
- •3.3.4. Способы получения
- •3.3.5. Многоатомные спирты
- •3.3.6. Физиологическое действие
- •3.3.7. Важнейшие представители
- •3.4. Простые насыщенные эфиры
- •3.4.1. Номенклатура и изомерия
- •3.4.2. Физические и химические свойства
- •3.4.3. Способы получения
- •3.4.4. Циклические простые эфиры
- •3.4.5. Физиологическая роль и Важнейшие представители
- •3.5. Эфиры минеральных кислот
- •3.5.1. Эфиры серной кислоты
- •3.5.2. Эфиры фосфорной кислоты
- •3.6. Тиоспирты и тиоэфиры
- •3.7. Насыщенные амины
- •3.7.1. Классификация, номенклатура, изомерия
- •3.7.2. Физические свойства
- •3.7.3. Строение и химические свойства
- •3.7.4. Способы получения
- •3.7.5. Физиологическая роль и Важнейшие представители
- •3.8. Нитроалканы
- •3.8.1. Строение
- •3.8.2. Свойства
- •3.8.3. Способы получения
- •3.8.4. Физиологическое действие и Важнейшие представители
- •3.9. Кремний-, фосфор- и мышьякорганические соединения
- •3.9.1. Кремнийорганические соединения
- •3.9.2. Фосфорорганические соединения
- •3.9.3. Мышьякорганические соединения
- •Вопросы и упражнения
3.2.5. Физиологическая роль и Важнейшие представители
Метиленхлорид (хлористый метилен, дихлорметан) — бесцветная жидкость со сладковатым запахом, малорастворим в воде. Обладает наркотическими свойствами. В промышленности получают хлорированием метана.
Метиленхлорид применяют в качестве растворителя для полимерных материалов (поливинилхлорида, полистирола, хлоркаучуков и др.).
Хлороформ (трихлорметан) — бесцветная жидкость со сладковатым запахом, малорастворим в воде. Обладает наркотическими и анестезирующими свойствами, применяется в медицине. В промышленности получают хлорированием этанола хлорной известью или гипохлорита кальция. Схема превращения с использованием гипохлорита выглядит следующим образом:

![]() .
.
Хлороформ хорошо растворяет жиры, смолы, каучук. Его используют также в промышленном органическом синтезе для получения фреонов. При контакте с воздухом, особенно на свету, хлороформ постепенно окисляется с образованием фосгена COCl2.
Йодоформ — антисептическое средство.
Тетрахлорметан (тетрахлорид углерода, четырёххлористый углерод) CCl4 — бесцветная тяжёлая негорючая жидкость со сладковатым запахом. Малорастворим в воде. С водой образует азеотропную смесь, кипящую при 339 К и содержащую 96% CCl4 и 4% H2O.
В промышленности тетрахлорметан получают хлорированием метана или сероуглерода. Используют его в качестве растворителя, особенно для растворения жиров, масел, смол. Тетрахлорметан является исходным сырьём для промышленного синтеза фреонов. Ядовит, вызывает повреждение печени и почек.
Дихлорэтан (1,2-дихлорэтан) — бесцветная жидкость со сладковатым запахом. Малорастворим в воде. С водой образует азеотропную смесь, кипящую при 344.6 К и содержащую 83% дихлорэтана.
В промышленности дихлорэтан получают хлорированием этилена. Он широко используется в качестве растворителя и исходного сырья в органическом синтезе (винилхлорид, этилендиамин и др.). Дихлорэтан обладает наркотическими свойствами, но ядовит, вызывает тяжёлые поражения печени.
Фреоны (хладоны) — фторохлороалканы представляют собой бесцветные газы или низкокипящие жидкости и вследствие своих специфических термодинамических свойств применяются в качестве хладагентов в холодильных машинах. Фреоны получают из соответствующих хлороалканов.
Перфторуглеводороды — продукты исчерпывающего фторирования углеводородов — обладают способностью растворять и переносить кислород по кровеносным сосудам. Являются химической основой для создания кровезаменителей.
3.3. Насыщенные спирты
Насыщенные (или предельные) спирты — это гидроксильные производные алканов, то есть это продукты замещения одного или нескольких атомов водорода в молекуле алкана гидроксогруппой или гидроксогруппами (-ОН).
3.3.1. Классификация, номенклатура, изомерия
Классификация предельных спиртов возможна по следующим признакам.
1. в зависимости от числа гидроксильных групп в молекуле спирты разделяют на одноатомные и многоатомные. Под атомностью понимают количество гидроксогрупп в молекуле спирта, например:
|
CH3-CH2ОН одноатомный |
CH2ОН-CH2ОН многоатомный (двухатомный) |
По взаимному расположению гидроксогрупп в двухатомных спиртах иногда выделяют геминальные диолы (или гем-диолы) и вицинальные диолы (или виц-диолы), но гем-диолы неустойчивы и существуют только в водном растворе в равновесии с соответствующим карбонильным соединением (гл. 3.3.5).
В зависимости от природы атома углерода, с которым связана гидроксогруппа, различают первичные, вторичные и третичные спирты.
Среди используемых номенклатур для названия низших спиртов преобладает радикало-функциональная, по которой название соединения состоит из прилагательного, образованного от названия углеводородного радикала, и существительного «спирт». Например:
|
CH3-ОН
|
— |
метиловый спирт |
|
C2H5-ОН
|
— |
этиловый спирт |
|
|
— |
третичнобутиловый спирт (трет-бутиловый спирт) |
Реже применяется рациональная номенклатура (применительно к спиртам она ещё называется «карбинольная»). По этой номенклатуре все спирты рассматриваются как производные родоначального соединения — CH3-ОН, называемого карбинолом. Для этого перечисляются все заместители у атома углерода, связанного с гидроксогруппой, и добавляется слово «карбинол». Например:
|
СН3-CH2-ОН
|
— |
метилкарбинол |
|
СН3CH2-CH2-ОН
|
— |
этилкарбинол |
|
|
— |
триметилкарбинол |
Но радикало-функциональная и рациональная номенклатуры малопригодны для названия соединений, имеющих длинный и разветвлённый углеводородный радикал, и конечно же для названия многоатомных спиртов. Значительно более универсальной является заместительная номенклатура ИЮПАК. В отсутствие более старших функциональных групп ОН-группа называется суффиксом -ол, добавляемым к названию углеводорода, а в присутствии старших групп — приставкой гидрокси-. Например:
|
СН3CH2CH2ОН
|
— |
пропанол-1 |
|
НОСН2CH2CH2ОН
|
— |
пропандиол-1,3 |
|
НОСН2CH2CООН |
— |
3-гидроксипропановая кислота |
Применяются также и тривиальные названия некоторых широкоупотребительных соединений: древесный спирт, винный спирт и др.
В названиях металлических производных спиртов (алкоголятов) ROMe в радикало-функциональной номенклатуре суффикс -ат добавляется к названию радикала, а в заместительной номенклатуре тот же суффикс -ат(ят) добавляется к полному названию спирта. Например: СН3ONa — метилат натрия, метанолят натрия; (С2Н5O)3Al — этилат алюминия, этанолят алюминия.
Изомерия предельных спиртов, аналогично галогеналканам, — структурная, оптическая, конформационная. Среди конформационных изомеров полифункциональных соединений, например галогеноспиртов, заслуживают внимания молекулы, в которых атом галогена и водородный атом гидроксогруппы пространственно сближены, так что между ними возможно образование водородной связи. Это, например, наблюдается в 2-хлорэтаноле-1. Поэтому для этой молекулы наиболее устойчивой будет скошенная конформация (гош-конформация):
|
|
|
|
2-хлорэтанол-1 | |