
- •Міністерство освіти і науки, молоді та спорту україни
- •Лекція № 3. Другий закон термодинаміки. . . . . . . . . . . . . 11
- •Передмова
- •Фізичну хімію підрозділяють на декілька основних розділів, які характеризують напрямок розвитку цієї науки та її предмет.
- •1.2 Теоретичні методи дослідження фізичної хімії
- •1.3 Експериментальні методи дослідження будови речовин
- •2.1 Основні поняття хімічної термодинаміки
- •2.2 Перший закон термодинаміки
- •2.4 Калориметрія
- •Лекція № 3. Другий закон термодинаміки
- •Лекція № 4. Термодинаміка хімічної рівноваги
- •4.1 Хімічна рівновага
- •Лекція № 5. Термодинаміка фазових переходів
- •5.1 Фазові рівноваги
- •5.2 Хімічний потенціал речовин
- •5.3 Фізико-хімічний аналіз
- •5.4Діаграма стану води
- •Лекція № 6. Термічний аналіз
- •6.1 Побудова діаграм стану систем за кривими охолодження
- •6.2 Діаграми стану систем, компоненти яких утворюють твердий розчин
- •Лекція № 7. 3агальна характеристика розчинів
- •7.1 Розчинність речовин
- •7.2 Способи вираження концентрації розчинів
- •7.3 Взаємна розчинність рідин
- •7.2 Екстракція
- •8.1 Розчини газів у рідинах
- •8.2 Закон Рауля
- •8.3 Осмос
- •9.1 Теорія електролітичної дисоціації
- •9.2 Водневий показник
- •9.3 Фізико-хімічні властивості розчинів електролітів
- •9.4 Теорія сильних електролітів
- •10.1 Механізм виникнення електродного потенціалу
- •10.2 Класифікація електродів
- •10.3 Потенціометричний метод дослідження
- •10.4 Кондуктометричний метод дослідження
- •11.1 Електрохімічні елементи
- •11.2 Класифікація електрохімічних елементів
- •11.3 Хімічні джерела електричної енергії
- •12.1 Швидкість хімічних реакцій
- •12.2 Кінетична класифікація хімічних реакцій
- •12.3 Кінетичні рівняння хімічних реакцій і-го і іі-го порядків
- •12.4 Методи визначення порядку хімічних реакцій
- •13.1 Паралельні і послідовні хімічні реакції
- •13.2 Ланцюгові хімічні реакції
- •13.3 Фотохімічні реакції
- •14.1 Загальні властивості каталізаторів
- •14.2 Гомогенний каталіз
- •14.3 Гетерогенний каталіз
- •14.4 Ферментативний каталіз
- •15.1 Поверхневий натяг
- •15.2 Поверхнево-активні речовини
- •15.3 Адсорбція пар на поверхні рідин
- •16.1 Теорія фізичної адсорбції Ленгмюра
- •Під час полімолекулярній адсорбції
- •16.3 Іонообмінна адсорбція
- •17.3 Флотація
- •17.4 Адсорбція в поруватих тілах
- •18.1 Класифікація дисперсних систем
- •18.2 Методи одержання дисперсних систем
- •18.3 Молекулярно-кінетичні властивості золів
- •18.4 Оптичні властивості дисперсних систем
- •19.2 Будова міцел ліофобних золів
- •19.3 Подвійний електричний шар на поверхні часточок
- •19.4 Електрокінетичний потенціал
- •20.1 Явище коагуляції золів
- •20.3 Захист золів від коагуляції
- •20.4 Пептизація
- •21.1 Колоїдні поверхнево-активні речовини
- •21.2 Міцелоутворення в ліофільних системах
- •21.3 Гідрофільно-ліпофільний баланс
- •21.4 Солюбілізація
- •22.1 Класифікація емульсій
- •22.2 Методи визначення типу емульсій
- •22.3 Емульгатори
- •22.4 Руйнування емульсій
- •22.5 Застосування емульсій в харчовій промисловості
- •23.2 Суспензії
- •23.3 Аерозолі
- •23.4 Порошки
- •24.1 Класифікація вмс
- •24.2 Фізичний стан полімерів
- •24.3 Фракціонування вмс
- •25.1 Механізм процесу набрякання вмс
- •25.2 Характеристики процесу набрякання
- •25.3 Термодинаміка процесів набрякання вмс
- •26.1 Класифікація поліелектролітів
- •26.2 Поліамфоліти
- •26.3 Властивості розчинів поліелектролітів
- •26.4 Висолювання і денатурація білків
- •27.1 Закон Ньютона
- •27.2 Віскозиметрія
- •27.3 В’язкість структурованих систем
- •27.4 Драглі
- •Рекомендована до дисципліни література
- •Навчальне видання
- •Для студентів напряму підготовки
- •6.051701 «Харчові технології та інженерія» піднапряму „Харчова інженерія”
20.3 Захист золів від коагуляції
 Стабільність
золів підвищують шляхом утворення
міцної захисної структури на поверхні
часточок або в дисперсійному середовищі.
На поверхні часточок адсорбуються
молекули ПАР або ВМС, які утворюють
механічну перепону, що не дозволяє
гранулам наближатися на “близьку”,
необхідну для їх злипання відстань. Під
час адсорбції молекул ВМС з довгими
ланцюгами більша частина цих ланцюгів
знаходиться в дисперсійному середовищі.
Стабілізація золів відбувається
внаслідок взаємного відштовхування
гнучких ланцюгів молекул. Під час
зближення часточок спостерігається
лише пружне зіткнення адсорбованих
молекул, а безпосередній контакт гранул
при цьому неможливий (рис. 20.2).
Стабільність
золів підвищують шляхом утворення
міцної захисної структури на поверхні
часточок або в дисперсійному середовищі.
На поверхні часточок адсорбуються
молекули ПАР або ВМС, які утворюють
механічну перепону, що не дозволяє
гранулам наближатися на “близьку”,
необхідну для їх злипання відстань. Під
час адсорбції молекул ВМС з довгими
ланцюгами більша частина цих ланцюгів
знаходиться в дисперсійному середовищі.
Стабілізація золів відбувається
внаслідок взаємного відштовхування
гнучких ланцюгів молекул. Під час
зближення часточок спостерігається
лише пружне зіткнення адсорбованих
молекул, а безпосередній контакт гранул
при цьому неможливий (рис. 20.2).
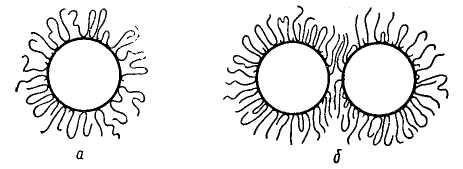
Рисунок 20.2 – Адсорбція макромолекул ланцюгових ВМС на:
а – окремій колоїдній часточці; б – на часточках, що зблизилися
Під час додання до золів певної кількості ВМС у дисперсійному середовищі утворюються просторові структури, які призводять до застигання золів. Рух часточок у таких системах суттєво обмежується і може навіть припинитися. Контакт колоїдних часточок при цьому стає маловірогідним – дисперсна система стабілізується.
Мірою захисної дії ВМС є захисне число, яке визначається масою сухого полімеру в мг, яка достатня для захисту від коагуляції 10 мл золю. Назва захисного числа походить від назви золю, який захищають. Так, «залізне» захисне число визначає кількість ВМС, яку необхідно додати до 10 мл золю Fе(ОН)3. Найбільш ефективними стабілізаторами золів є білки і полісахариди. Для желатину «залізне» число дорівнює 3...5 мг, для декстрину – 20...25 мг. Значення захисних чисел певною мірою є умовними, оскільки на захисну дію ВМС впливає ряд факторів: дисперсність золю, значеннярНсередовища, молярна маса ВМС і т.д.
Необхідність захисту золів від коагуляції пов’язана з тим, що значне число харчових продуктів виготовляється в подрібненому (диспергованому) стані. Цінні речовини у таких виробах повинні рівномірно розподілятися в об’ємі системи, щоб поступово розчиняючись, справляти необхідну дію.
Якщо кількість полімеру, що додають до золю, недостатня, то можливий зворотний ефект – зниження стійкості золю під час додання ВМС. Таке явище називається сенсибілізацією.Сенсибілізація пояснюється тим, що макромолекул ВМС не вистачає для утворення суцільного захисного адсорбційного шару. Гнучкі ланцюги макромолекул адсорбуються на часточках тільки окремими ділянками. Найдовші ланцюги ВМС при цьому утворюють так звані «містки», які зв’язують колоїдні часточки між собою, притягуючи їх одна до одної і, таким чином, сприяють коагуляції.
20.4 Пептизація
Пептизацією називається перехід у колоїдний розчин осадів, що утворилися під час коагуляції. Розщеплення продуктів коагуляції золів і повторне утворення золю можливе, якщо не змінилася структура часточок у коагуляті, і вони не зрослися одна з одною. Для пептизації коагулят необхідно ретельно промити водою, щоб позбавитись від електроліту, який викликав коагуляцію, і додати речовину-стабілізатор, яка містить потенціалвизначаючі іони. При цьому на поверхні часточок знову виникає подвійний електричний шар, а навколо них – сольватні оболонки. Все це призводить до подолання сил зчеплення між колоїдними часточками. Часточки, що стали вільними, під дією броунівського руху рівномірно розподіляються по об’єму рідини. Таким чином, пептизація є процесом, зворотним коагуляції. Перемішування і підвищення температури сприяє пептизації.
Пептизація широко застосовується у техніці, коли необхідно розчиняти осади і переводити їх у колоїдний стан.
Лекція № 21. Властивості ліофільних колоїдних систем
План лекції
1. Колоїдні поверхнево-активні речовини.
2. Міцелоутворення в ліофільних системах.
3. Гідрофільно-ліпофільний баланс.
4. Солюбілізація.
Рекомендована література:[2]С.128-132.
