
- •Биоорганическая химия
- •Теория строения органических соединений а.М.Бутлерова.
- •Классификация и номенклатура органических соединений.
- •Основные классы органических соединений
- •Образование и типы химических связей в органических соединениях.
- •Классификация органических реакций.
- •По характеру изменений связей в субстрате и реагенте.
- •Э электрофил лектрофильная реакция:
- •Н Нуклеофил уклеофильная реакция:
- •В соответствии с конечным результатом.
- •Электрофильное замещение se
- •Электрофильное присоединение аe
- •По числу частиц, принимающих участие в элементарной стадии.
- •Взаимное влияние атомов в молекулах органических соединений и способы его передачи.
- •Сопряжение.
- •Кислотность и основность органических соединений
- •Кислотность и основность по Бренстеду.
- •Кислоты и основания Льюиса.
- •Жесткие и мягкие кислоты и основания.
- •План описания органических соединений:
- •Алканы (предельные, насыщенные углеводороды, парафины)
- •Физические свойства.
- •Способы получения.
- •Промышленные
- •Лабораторные
- •Химические свойства.
- •Реакции галогенирования
- •Нитрование (реакция Коновалова)
- •3. Сульфирование и сульфохлорирование.
- •4. Окисление.
- •5. Изомеризация.
- •6. Дегидрирование.
- •7. Крекинг.
- •I. Промышленные.
- •Лабораторные.
- •Дегидратация спиртов:
- •Химические свойства.
- •Реакции присоединения.
- •3) Присоединение галогеноводородов (гидрогалогенирование):
- •4) Присоединение воды (гидратация):
- •2. Реакции окисления.
- •4) Озонолиз (окисление озоном):
- •3. Реакции полимеризации.
- •I. Промышленные.
- •II. Лабораторные.
- •Дегалогенирование тетрагалогенпроизводных:
- •Химические свойства.
- •Реакции электрофильного присоединения.
- •Присоединение галогенов (галогенирование):
- •Присоединение галогеноводородов:
- •Присоединение воды (реакция Кучерова):
- •Реакции нуклеофильного присоединения.
- •Реакции окисления-восстановления.
- •Реакции полимеризации.
- •Реакции замещения.
- •Алкадиены (диеновые углеводороды)
- •Способы получения.
- •Дегидратация двухатомных спиртов:
- •Химические свойства.
- •Электронное строение бутадиена-1,3.
- •Реакции присоединения.
- •Гидрирование:
- •Галогенирование:
- •Гидрогалогенирование:
- •Реакции полимеризации.
- •Галогенпроизводные алифатического ряда.
- •Физические свойства.
- •Способы получения.
- •Электронное строение и химические свойства.
- •Реакции нуклеофильного замещения.
- •Реакции элиминирования.
- •Ароматические углеводороды (арены)
- •Изомерия.
- •Способы получения.
- •Переработка угля и нефти:
- •Электронное строение бензола.
- •Химические свойства.
- •Реакции присоединения.
- •Реакции окисления.
- •Реакции замещения.
- •Галогенирование:
- •Сульфирование:
- •Алкилирование (реакция Фриделя-Крафтса):
- •Ацилирование:
- •Правила ориентации заместителей.
- •Спирты (алкоголи)
- •Физические свойства.
- •Способы получения.
- •Гидратация алкенов:
- •2. Гидролиз галогенпроизводных:
- •3. Спиртовое брожение сахаров:
- •Электронное строение и химические свойства.
- •1. Кислотные и основные свойства.
- •Реакции с участием нуклеофильного центра.
- •Образование простых эфиров (межмолекулярная дегидратация):
- •Образование сложных эфиров:
- •Реакции с участием электрофильного центра.
- •Реакции с участием сн-кислотного центра (реакции элиминирования).
- •5. Реакции окисления.
- •4. Восстановление:
- •Классификация.
- •Способы получения.
- •Химические свойства.
- •1. Кислотные и основные свойства.
- •2. Реакции с участием нуклеофильного центра.
- •3. Реакции с участием электрофильного центра.
- •4. Реакции электрофильного замещения в ароматическом ядре.
- •5. Реакции окисления-восстановления.
- •Карбонильные соединения (альдегиды и кетоны).
- •Бутаналь бутанон-2 Физические свойства.
- •Способы получения.
- •Электронное строение и химические свойства.
- •Реакции присоединения.
- •Гидратация:
- •Присоединение спиртов:
- •Присоединение тиолов:
- •2. Реакции конденсации.
- •3. Реакции окисления.
- •1. Окисление кислородом воздуха:
- •2. Окисление аммиачным раствором оксида серебра (реакция «серебряного зеркала»):
- •4. Реакции полимеризации.
- •Карбоновые кислоты.
- •Предельные одноосновные карбоновые кислоты. Номенклатура.
- •Способы получения.
- •Электронное строение и химические свойства.
- •Кислотные свойства.
- •Реакции нуклеофильного замещения.
- •Реакция этерификации:
- •Образование ангидридов:
- •Образование галогенангидридов:
- •Образование амидов:
- •Реакции по углеродному атому.
- •Реакции декарбоксилирования.
- •Функциональные производные карбоновых кислот
- •Галогенангидриды.
- •Ангидриды.
- •Сложные эфиры.
- •Тиоэфиры.
- •Классификация.
- •Номенклатура.
- •Способы получения.
- •Восстановление нитросоединений:
- •Аммонолиз и аминолиз галогенпроизводных:
- •Химические свойства.
- •Основные свойства.
- •Кислотные свойства.
- •3. Нуклеофильные свойства.
- •Ацилирование аминов:
- •4. Реакции с азотистой кислотой.
- •1 . Первичные алифатические амины
- •2. Первичные ароматические амины:
- •3. Вторичные алифатические и ароматические амины:
- •Электрофильное замещение в ароматических аминах.
-
По характеру изменений связей в субстрате и реагенте.
По этому признаку реакции подразделяют на радикальные, ионные и согласованные.
Радикальные, или гомолитические реакции (символ R). В них действуют радикальные реагенты и происходит гомолитический разрыв связи в субстрате:
Cl + Н СН3 НСl + СН3
Ионные, или гетеролитические реакции. Эти реакции сопровождаются гетеролитическим разрывом связи в субстрате. В зависимости от природы атакующего реагента могут быть электрофильными (символ Е) и нуклеофильными (символ N).
Э электрофил лектрофильная реакция:


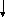
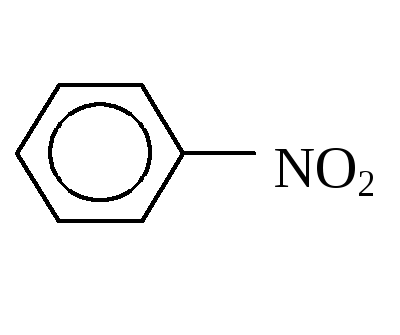
Субстрат Реагент Продукты реакции
Н Нуклеофил уклеофильная реакция:
С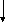 Н3Br
+ Na+OH
CH3OH
+ Na+Br
Н3Br
+ Na+OH
CH3OH
+ Na+Br
Субстрат Реагент Продукты реакции
Согласованные, или синхронные реакции. В данных реакциях разрыв старых и образование новых связей происходит одновременно без участия радикальных или ионных частиц. Для них теряют смысл понятия реагента и субстрата. Эти реакции протекают через циклическое переходное состояние:
Н2С=СНСН=СН2 + Н2С=СН2
Бутадиен-1,3 Этилен Переходное состояние Циклогексен
-
В соответствии с конечным результатом.
По этому признаку реакции делят на несколько основных типов:
Реакции замещения (символ S). В зависимости от природы атакующего реагента замещение может быть радикальное, электрофильное или нуклеофильное.
Радикальное
замещение SR
C X + У С У + Х
Электрофильное замещение se
C X + Е+ С Е + Х+
Нуклеофильное
замещение SN
C X + У С У + Х
Замещаемая часть субстрата Х называется уходящей группой. Група, уходящая без пары электронов, называется электрофугом; уходящая с парой электронов – нуклеофуг. При радикальном замещении уходящий свободный радикал тут же вступает в дальнейшую реакцию.
Р
Радикальное
присоединение АR
+Х
C=С + ХУ СС СС
У
Х У
Электрофильное присоединение аe
C=С + ЕУ С+С СС
Нуклеофильное
присоединение AN
C=С + ЕУ СС СС
У Е У
В зависимости от природы присоединяемого вещества реакции присоединения имеют частные названия:
-
Гидрирование (присоединение водорода);
-
Галогенирование (присоединение галогенов);
-
Гидрогалогенирование (присоединение галогеноводородов);
-
Гидратация (присоединение воды).
Реакции отщепления (элиминирования) (символ Е). Это реакции обратные реакциям присоединения:
СС С=С + Х+ + У
-
Х У Группы Х и У могут уходить последовательно или одновременно.
В зависимости от природы отщепляющихся фрагментов реакции элиминирования имеют частные названия:
-
Дегидратация (отщепление воды);
-
Дегидрирование (отщепление водорода);
-
Дегидрогалогенирование (отщепление галогеноводородов);
-
Дегалогенирование (отщепление галогенов);
-
Декарбоксилирование (отщепление СО2).
Перегруппировки. В ходе перегруппировки происходит переход (миграция) атомов или групп от одного участка молекулы к другому.
AlCl3
СН3СН2СН2СН3 СН3СНСН3
Бутан CH3 Изобутан
Окислительно-восстановительные реакции. В ходе этих реакций меняется степень окисления атома углерода, являющегося реакционным центром.
Окислительно-восстановительный ряд показан на примере последовательного окисления метана в СО2:
[O] [O] [O] [O]
С






 Н4
CH3OH
HC=О
HC=О
СО2
Н4
CH3OH
HC=О
HC=О
СО2
[H] [H] [H] [H]
H ОH
метан метанол формальдегид муравьиная к-та оксид углерода
