
- •1. Броуновское движение
- •2. Законы идеального газа
- •3. Барометрическая формула.
- •4. Основное уравнение молекулярно-кинетической
- •5. Распределение Максвелла
- •6. Средняя длина свободного пробега
- •Vмол30 1030 м3, м.
- •7. Явления переноса
- •Диффузия в газах
- •8. Внутреннее трение
- •Теплопроводность
- •9. Первое начало термодинамики
- •10. Классическая теория теплоемкости
- •11. Адиабатический процесс
- •12. Политропический процесс
- •13. Энтропия. Второе и третье начала термодинамики
- •14. Расчет изменения энтропии в процессах
- •15. Цикл Карно. Второе начало термодинамики
- •16. Реальные газы. Критическое состояние
- •17. Уравнение Ван-дер-Ваальса
- •18. Особенности жидкого состояния вещества
- •19. Свободная энергия как функция состояния
- •Поверхностное натяжение
- •20. Условия равновесия на границах различных сред
- •21. Формула Лапласа
- •22. Фаза. Фазовое равновесие. Общая характеристика фазовых переходов 1-го и 2-го рода
- •23. Уравнение Клапейрона Клаузиуса.
- •24. Эффект Джоуля-Томсона
- •25. Методы получения низких температур
- •26. Термодинамическая шкала температур.
- •27. Симметрия кристаллов. Дефекты в кристаллах
- •Классическая теория теплоемкости твердых тел
- •28. Понятие о квантовой статистике. Распределения
- •29. Понятие о квантовой теории теплоемкости.
- •Рекомендуемая литература*
3. Барометрическая формула.
Распределение Больцмана. Опыт Перрена
Атмосфера планеты находится в ее гравитационном поле. Если бы этого поля не было, воздух рассеялся бы по космосу. С другой стороны, если бы не было теплового движения молекул газа, то молекулы атмосферного воздуха упали бы на Землю. Тяготение и тепловое движение приводят к такому стационарному состоянию атмосферы, при котором происходит убыль концентрации и давления газа с высотой.
Найдем, как изменяется давление с высотой. Для этого необходимо сделать ряд упрощений: 1) Земля – идеальный шар; 2) атмосфера – идеальный газ; 3) температура на всех высотах одна и та же; 4) ускорение свободного падения не зависит от высоты; 5) молярная масса воздуха постоянна.
 Пусть
на поверхности Земли давление равно
р0,
а на высоте h
давление равно р
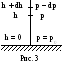
(рис. 3). Воспользуемся формулой для
давления p
= gh.
При переходе от высоты h
к высоте h
+ dh
давление
изменяется на величину
Пусть
на поверхности Земли давление равно
р0,
а на высоте h
давление равно р
(рис. 3). Воспользуемся формулой для
давления p
= gh.
При переходе от высоты h
к высоте h
+ dh
давление
изменяется на величину
– dp = g dh. Знак "минус" говорит о том, что давление убывает с высотой. Плотность воздуха найдем из уравнения Клапейрона-Менделеева:
![]()
![]() .
.
Получаем
для изменения давления:
![]() .
.
Разделяем
переменные:
![]() .
.
Интегрируем,
взяв постоянную интегрирования в
удобном для дальнейших расчетов виде):![]()
Умножим
дробь на единицу (1
= ln
e):
![]() .
.
Постоянную
интегрирования С
находим из начальных условий:
при
h
= 0, C
= p0.
Таким
образом, окончательно получаем
барометрическую формулу:![]()
![]() .
(8)
.
(8)
Формула (8), несмотря на сделанные упрощения, позволяет достаточно точно определять высоту (в пределах десятков километров) при измерении давления. Предназначенные для этой цели специальные барометры, шкала которых проградуирована непосредственно в метрах, называются альтиметрами (высотомерами). Такие приборы устанавливаются, в частности, на самолетах.
Если при выводе барометрической формулы учесть зависимость ускорения свободного падения от высоты, то можно получить формулу, из которой следует, что даже на бесконечном удалении от Земли атмосферное давление не равно нулю. Так как это невозможно, то следует предположить, что атмосфера Земли не находится в равновесном состоянии, а постепенно рассеивается в космическое пространство. Однако это рассеяние относительно мало, так как Земля и ее атмосфера существуют несколько миллиардов лет.
Возьмем барометрическую формулу (8) и сделаем в ней следующие замены: p = nkT, M/R = M/(kNA) = m/k, где m – масса одной молекулы, k – постоянная Больцмана. Кроме того, пусть температура на всех высотах одинакова (Т = Т0). Тогда
![]() .
.
После
сокращений получаем распределение
Больцмана:![]()
Из формулы (9) следует, что процентное содержание (концентрация) легких газов в смеси возрастает с высотой (т.е. изменяется молярная масса воздуха).
Распределение Больцмана можно записать и в другом виде:
![]() ,
или
,
или
![]() .
(10)
.
(10)
Формула (10) позволяет определить долю частиц от общего числа, которые в условиях теплового равновесия обладают потенциальной энергией p = mgh.
Французский физик Перрен в 1909 г., используя формулу распределения Больцмана, определил опытным путем постоянную Больцмана (число Авогадро). Перрен использовал эмульсию из практически одинаковых шариков диаметром 0,1 мкм (шарики из гуммигута – сгущенного млечного сока некоторых деревьев из Южной Азии). Применялся вертикально расположенный микроскоп с очень малой глубиной резкости. Непосредственно подсчитывалось число частиц в поле зрения микроскопа в слое глубиной 1 мкм. При вычислениях учитывалась поправка на уменьшение веса за счет Архимедовой силы. Найденное значение числа Авогадро находилось в хорошем соответствии с результатами, полученными другими исследователями, что доказывает применимость распределения Больцмана к броуновским частицам.
