
- •Часть I
- •§ I. А) Оборудование рабочего места.
- •§ 7. Метод люминесцентной микроскопии.
- •§ I. Устройство электронного микроскопа.
- •§2. Методы электронно-микроскопического препарирования.
- •§3. Методы получения ультратонких срезов
- •§ 4. Демонстрация ультратонких срезов бактериальных клеток в электронном микроскопе.
- •§ 5. Описание метода микроскопии в темном поле см. В методических указаниях к 4 практическому занятию.
- •§ 2. Посмотреть под микроскопом препарат-мазок из культуры бактерий, имеющих жгутики, и зарисовать. Препарат окрашен по методу Бениньетти.
- •§ 3. Окраска по Граму (в модификации Синева) производят следующим образом. Из исследуемого материала готовят тонкий препарат-мазок, высушивают его на воздухе и фиксируют на пламени спиртовки.
- •§ 4. Окраска зерен волютина по Нейссеру.
- •§ 5. Окраска капсул по методу Бурри-Гинса.
- •§ 3. Метод микроскопии в темном поле.
- •§ 6. В препарате-мазке, окрашенном метиленовым синим, обратить внимание на форму дрожжевых клеток, наличие почковидных выпячиваний, а также на внутреннее строение клеток.
- •3Анятие 5
- •§ 9. Сделать посев отпечатков пальцев руки на пластинки мпа и среды Эндо.
- •§ 4. Результаты посева на среды пестрого ряда зарегистрировать в таблице.
- •§ 5. Приготовить взвесь почвы в Физиологическом растворе. С помощью пастеровской пипетки засеять 1-2 капли взвеси на среду Тароцци.
- •§ 4. А) Определение дифтерийного экзотоксина реакцией преципитации в агаре.
- •§ 7. Демонстрация различных методов заражения экспериментальных животных:
- •§ I. Макроскопическое изучение культур стафилококков на кровяном мпа. Зарисовать картину гемолиза.
- •§ 2. Демонстрация инструментария, посуды, разбор правил пересылки материала для исследования в бактериологические лаборатории.
- •§ 5. Опыт действия лизоцима на Micrococcus lysodeikticus.
- •§ I. Определение ld50 по методу Рида и Менча. Ld50 - количество микроорганизмов (бактерий, вирусов), вызывающих гибель 50 % зараженных животных.
- •§ 3. Приготовить корпускулярные антигены из культур водного вибриона и кишечной палочки. Для этого:
- •§ 4. Методы иммунизации животных и получения иммунных сывороток:
- •§ 5. Реакция агглютинации:
- •§ I. Разбор методов приготовления 0- и н-антигенов.
- •§ 5. Определение титра агглютинирующей сыворотки. Для опыта необходимо иметь:
- •§ I. Учесть окончательный результат реакции агглютинации и определить титр испытуемой агглютинирующей сыворотки. Результаты опыта отметить в таблице, схема которой дана ниже.
- •§ 5. Для постановки реакции преципитации необходимо иметь:
- •§ 6.Реакция преципитации в агаре.
- •§2. Реакция лизиса.
- •§ 4. Реакция фагоцитоза. Постановка опсоно-фагоцитарной реакции.
- •§5. А)Прямой иммунофлуоресцентный метод.
- •§ I. А). Опыт трансдукции.
- •Часть II. Вирусология
- •§ I. Зарисовать феномен бактериофагии на плотной питательной среде.
- •§ 2. Для титрования бактериофага используются различные методы. Наиболее точным является метод агаровых слоев, предложенный Графа. Сущность этого метода состоит в следующем.
- •§ 3. А). Элементарные тельца (вирионы) вируса оспы (тельца Пашена) в препаратах, окрашенных по Морозову, выглядят в виде мелких точек круглой или удлиненной формы, темно-коричневого цвета.
- •§ 4. Методы заражения животных разнообразны: внутрибрюшинный, внутривенный, внутримышечный, интраназальный, заражение в мозг и другие.
- •§ 6. С помощью камеры Горяева подсчитают количество клеток в 1 мл. Клетки считают по всей камере под малым увеличением микроскопа . Количество клеток в 1 мл вычисляют по формуле:
- •3. Методы микробиологической диагностики вирусных заболеваний
- •3Анятие 3
- •1. Вирусологические:
- •2. Эпидемиологические:
- •§ 3. Для диагностики вирусных гепатитов могут быть использованы методы:
- •Часть III
- •§1.Зарегистрировать в таблице результаты реакции Райта. Сформулировать и записать вывод: указывают ли результаты реакции на наличие заболевания бруцеллезом у данного больного?
- •§5.Рассмотреть невооруженным глазом и под малым увеличением микроскопа колонии сибиреязвенных палочек (вакцинный штамм сти).
- •§ 2,3. Поставить реакцию агглютинации с монорецепторными 0- и н-сыворотками, принимая во внимание биохимические свойства выделенной культуры. Результаты зарегистрировать в тетрадь.
- •§ 1. Произвести макро- и микроскопическое исследование подозрительных колоний (бесцветные, прозрачные). Посеять подозрительную колонию на скошенный мпа и среды "пестрого ряда".
- •§ 1. Поставить реакцию агглютинации на стекле выделенной культуры кишечной палочки с поливалентными ок-сыворотками:
- •§1. Демонстрация роста анаэробов на средах Виллиса-Хоббс, Тароцци, Вильсон-Блера, Цейсслера, на молоке.
- •§1. Промикроскопировать готовые препараты-мазки из культуры коклюшной палочки с окраской по Граму и зарисовать.
- •§2. Разбор методов микробиологической диагностики коклюша: бактериологического и серологического. Дифференциация коклюшной и паракоклюшной палочек.
- •§2. Промикроскопировать готовые препараты-мазки туберкулезных бактерий, окрашенных по Цилю-Нильсену. Препараты зарисовать.
- •§3. Демонстрация роста туберкулезных бактерий на глицериновом бульоне, яичной среде Петраньяни и других средах.
- •§7. Ознакомление с составом и назначением следующих иммунопрепаратов: туберкулин Коха, очищенный туберкулин ррd-l, вакцина бжп.
- •§1. Произвести учет результатов определения биохимической активности коринебактерий и пробы на токсигенность.
- •§1. Промикроскопировать и зарисовать готовые препараты-мазки риккетсий. По Романовскому-Гимза риккетсии окрашены в красный цвет.
- •§2. Разбор и демонстрация реакции агглютинации с риккетсиозным антигеном (взвесь убитых формалином риккетсий). Результаты реакции зарегистрировать.
Часть I
ОБЩАЯ МИКРОБИОЛОГИЯ И ИММУНОЛОГИЯ
ЗАНЯТИЕ 1
Дата________________
Тема: ВВЕДЕНИЕ В МИКРОБИОЛОГИЧЕСКУЮ ЛАБОРАТОРИЮ. МИКРОСКОПИЧЕСКИЕ МЕТОДЫ ИССЛЕДОВАНИЯ
План занятия
1.Знакомство с рабочим местом и режимом работы в микробиологической лаборатории.
2.Знакомство с иммерсионным микроскопом и правилами работы с ним.
3.Упражнение в микроскопии на готовых препаратах с применением сухих и иммерсионной систем.
4.Правила обращения с культурами микробов.
5.Приготовление препарата "раздавленная капля".
6.Приготовление и окраска препарата тушью по Бурри (негативный способ окраски).
7.Знакомство со специальными методами микроскопии (люминесцентная микроскопия).
Методические указания
§ I. А) Оборудование рабочего места.
На рабочем столе должно быть все необходимое для работы: микроскоп, иммерсионное масло, бактериологическая петля, спиртовка, набор красок, промывалка и ванна для промывки препаратов, предметные стекла и салфетки для протирания их, штатив для пробирок с культурами, пинцет, фильтровальная бумага для высушивания препаратов и банка для отработанных стекол.
Из личных вещей студента на рабочем месте допускается иметь только рабочую тетрадь, в которой делают записи и зарисовки. Ничего лишнего (в том числе учебников и других книг) на рабочем столе не должно быть.
б) Режим работы в бактериологической лаборатории.
Работа с болезнетворными микробами требует обязательного соблюдения ряда правил личной и общественной профилактики. Каждый студент обязан работать в халате, на голову надевать шапочку или косынку, не курить и не принимать пищу в лаборатории, избегать суеты. По окончании работы необходимо вымыть руки с мылом.
§ 2. Важнейшей характеристикой каждого объектива микроскопа является его разрешающаяся способность. Разрешающей способностью называется расстояние между двумя точками, при котором они еще видны раздельно (т.е. не сливаются в одну). Разрешающая способность объектива ограничивается такими недостатками оптической системы, как сферическая и хроматическая аберрации ,дифракция и т.д. Если первые два явления устранимы, то явление дифракции имеет место в любой оптической системе. Оно ограничивает разрешающую способность оптических систем. Разрешающая способность объектива с учетом явлений дифракции описывается следующей формулой:
А
= 0,61
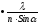 ,
,
где А - минимальное расстояние между двумя точками объекта (разрешающая способность);
n - показатель преломления среды между препаратом и фронтальной линзой объектива (в случае масляной иммерсии n=1,51);
α- угол между оптической осью объектива и наиболее крайним лучом, попадающим в объектив из центра препарата;
λ- длина световой волны;
0,61 - коэффициент, который учитывает геометрические факторы при вычислении освещенности первого дифракционного максимума от круглого отверстия.
Величина n·Sinα постоянна для каждого объектива и называется числовой, или нумерической, апертурой. Она выгравирована на оправе объектива. В монобромнафталиновых иммерсионных объективах нумерическая апертура может варьировать в пределах от 1,25 до 1,60. При наличии воздуха между фронтальной линзой и покровным стеклом нумерическая апертура не превышает 0,95.
Из приведенной выше формулы видно, что разрешающая способность объектива прямо пропорциональная его числовой апертуре и обратно пропорциональна длине волны света, используемого при микроскопии. При микроскопии в видимом свете с длиной волны порядка 0,55 микрона и иммерсионным объективом с максимальной нумерической апертурой 1,60 разрешающая способность равна:
А
= 0,61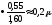
Величина угла, при котором глаз способен различать раздельно две точки, называется углом резкого зрения. Для получения на сетчатке раздельного изображения двух точек световые лучи должны попасть в глаз под углом зрения, который стягивает дугу от 2 до 4 минут.
Изображение структур, разрешенных объективом, может быть увеличено окуляром лишь настолько, чтобы оно просматривалось под углом, стягивающим дугу величиной от 2 до 4 минут. Это - полезное увеличение микроскопа. Полезное увеличение микроскопа не может превышать числовую апертуру более чем в 1000 раз. Поэтому максимальное полезное увеличение для микроскопов, имеющих иммерсионные объективы с апертурой 1,4-1,6, составляет 1400-1600. Применение в таких микроскопах более сильных окуляров никаких дополнительных деталей к структуре препарата, разрешаемой объективом, не выявляет.
Для полного использования разрешающей способности иммерсионного объектива необходимо выполнять следующие основные правила:
1)Конденсор осветительного аппарата должен быть поднят до отказа (до уровня предметного столика).
2)Диафрагма конденсора должна быть полностью открыта.
3)Во всех без исключения случаях работа ведется с плоским зеркалом, так как конденсор рассчитан на работу с параллельными пучками света.
Наряду с увеличением и нумерической апертурой одной из важных характеристик объектива является его свободное рабочее расстояние, т.е. расстояние между верхней поверхностью препарата и нижней поверхностью фронтальной линзы объектива при наведенном на фокус объективе. Эти расстояния следующие:
для объектива с увеличением х8 - 8,5 мм;
для объектива с увеличением 40х - 0,4 мм;
для объектива с увеличением 90х - 0,2 мм.
Знание этих расстояний необходимо для того, чтобы быстро сфокусировать микроскоп на препарате. Кроме того, чтобы правильно и быстро установить освещение, необходимо, чтобы объектив находился от препарата на свободном рабочем расстоянии.
Порядок работы с микроскопом
1.Проверить состояние осветительного аппарата (поднять конденсор, открыть его диафрагму, поставить плоское зеркало).
2.Положить на столик микроскопа исследуемый препарат и поставить слабый сухой объектив (8x) на расстояние несколько меньше свободного рабочего расстояния (для данного объектива 5-7 мм).
Рис.1 Дрожжевые клетки объектив 8x
Рис.2 Дрожжевые клетки объектив 40x
Рис.3 Дрожжевые клетки объектив 90x
3. Глядя в окуляр и вращая зеркалом, произвести предварительную установку освещения,
4. Медленно поднимая тубус макровинтом, добиться резкого изображения препарата. При использовании слабого сухого объектива в поле зрения, кроме препарата, может быть видно изображение источника света, т.е. оконной рамы и других предметов, находящихся за окном.
5.Движением зеркала поставить в центре поля зрения наиболее светлый участок оконной рамы (например, участок неба с облаками), после чего можно переходить на микроскопию с сильным сухим или иммерсионным объективами. При этом мешающие детали исчезают из поля зрения, Если этого не происходит, то следует осторожно приподнять или опустить конденсор на 1-1,5 мм.
6.Поставив сильный сухой или иммерсионный объектив, ни в коем случае нельзя опускать тубус микроскопа, глядя в окуляр. Необходимо под контролем глаза, глядя сбоку, опустить объектив на расстояние меньше свободного рабочего, а затем, глядя в окуляр, макровинтом медленно поднимать тубус до тех пор, пока появится мелькание препарата. После этого точная установка достигается с помощью микровинта. Не следует делать микровинтом более половины оборота в одну или другую сторону. При фокусировке микроскопа полезно левой рукой слегка двигать препарат по поверхности предметного столика.
§ 3. Пользуясь изложенными сведениями, необходимо научиться быстро и правильно устанавливать препарат в Фокусе при всех трех объективах. Рассматривая препарат, следует обратить внимание на резкое увеличение числа разрешаемых подробностей при работе с иммерсионным объективом по сравнению с сухими объективами.
Зарегистрировать рабочий номер своего микроскопа и указать в таблице его основные параметры.
Рис.4. Микроскоп Обозначения: 1 - окуляр; 2 - тубус; 3 -штатив(колонка и ножка);4- макрометрический винт; 5- микрометрический винт;6- зеркало; 7 - конденсор;8- предметный столик;9- объектив; 10 – револьвер.
Параметры рабочего микроскопа.
Тип (марка)__________________________________________________
Заводской номер_____________________________________________
Увеличение окуляра__________________________________________
Номера объективов: 8x________________________________________
40x_______________________________________
90x_______________________________________
Нумерическая апертура
объективов: 8x________________________________________
40x_______________________________________
90x_______________________________________
Общее увеличение
с объективом 90x_______________________________________
Порядковый номер________________________________________
Роспись_________________________________________________
§ 4. Необходимо твердо усвоить основные приемы бактериологической техники: обращение с культурами микробов, использование бактериологической петли, спиртовок, способы обеззараживания использованного материала и отработанных стекол.
При работе с культурами микроорганизмов необходимо соблюдать следующие два основные принципа: 1 - не загрязнить микробами окружающей среды и не заразить самого себя и 2 - не загрязнить культуру посторонними микробами из окружающей среды, так как точная идентификация исследуемого возбудителя заболевания возможна лишь при условии выделения и сохранения его в чистой культуре.
Культуру бактерий сохраняют обычно на жидких и плотных питательных средах в пробирках, закрытых ватно-марлевыми пробками. При всех манипуляциях с культурой (приготовление мазка, пересев ее с одной среда на другую и т.д.) используют стерильную бактериологическую петлю из металлической проволоки. Правильно приготовленная петля диаметром от I до 5 мм должна быть полностью замкнута и не должна тлеть лишнего свободного конца. Петлю стерилизуют прокаливанием докрасна в пламени горелки, держа ее сначала вертикально, затем проводят 3-4 раза через пламя прилегающую к петле часть петледержателя.
Для соблюдения вышеуказанных принципов в случае приготовления бактериологическую петлю берут в правую руку как ручку или карандаш, а пробирку держат в левой руке между большим и указательным пальцами с тыльной стороны кисти почти в горизонтальном положении. При этом должна быть хорошо видна поверхность питательной среды с культурой бактерий.
Простерилизовав петлю, правой рукой захватывают пробку, прижимая ее мизинцем к ладони, освобождают ее небольшим поворотом, вынимают над пламенем горелки и, не выпуская пробку из руки (в таком положении она сохраняется в течение последующих манипуляций) обжигают края пробирки. Петлю вводят в пробирку, остужают прикосновением к внутренней стороне стекла и берут ею небольшое количество культуры, стараясь не захватить при этом питательной среды. Вынув петлю, опять обжигают края пробирки, слегка обжигают пробку и закрывают ею пробирку. Не выпуская петли из руки, ставят пробирку в штатив и приступают к приготовлению мазка. После этого петлю стерилизуют и ставят в штатив.
С соблюдением этих основных правил производят и все другие манипуляции с культурами бактерий - пересев из пробирки в пробирку» из пробирки в чашку, из чашки в чашку и т.п.
В случае попадания культуры микробов на руки, другие предметы и пол необходимо немедлено протереть руки и загрязненные предметы ватой, смоченной дезинфицирующим растворов, а пол залить этим же раствором. Через 30 минут руки можно вымать с мылом.
§ 5. На чистое сухое предметное стекло нанести с помощью бактериологической петли каплю воды. Прокаленной и остуженной петлёй внести в небольшое количество (одну петлю) микробной массы и равномерно перемешать с водой. Петлю прокалить и поставить в штатив. Накрыть каплю чистым покровным стеклом и придавить его слегка рукояткой петли. Полученную "раздавленную каплю" поместить на предметный столик микроскопа и промикроскопировать сначала со слабым сухим объективом, затем с сильным сухим объективом и, наконец, с иммерсионным. Для установки препарата в фокусе следует найти вначале при малом увеличении капли, вывести его в центр поля зрения и затем по нему ориентироваться.
При микроскопии необходимо помнить, что рассматривание неокрашенного препарата возможно только с ограниченным освещением, что достигается опусканием конденсора или уменьшением отверстия ирис-диафрагмы,
§ 6. На чистое предметное стекло наносят каплю воды и рядом с ней несколько больших размеров каплю туши. В каплю воды вносят небольшое количество исследуемой культуры (получается облачко помутнения). Прокалив и остудив петлю(чтобы сжечь оставшуюся массу бактерий), готовят равномерную взвесь бактерий. Затем соединяют эту каплю с каплей туши, тщательно перемешивают и размазывают по стеклу тонким слоем. Высушивают мазок на воздухе и микроскопируют с иммерсионным объективом.
При микроскопии препарата рекомендуется начинать с более светлых участков его, а затем переходить на более темные. Необходимо помнить, что при негативных способах окраски микробы остаются не убитыми.
