
Общие вопросы / Хосева 2014 Диссертация
.pdf
141
Таблица 4.3.2.
Мероприятия по купированию НПР у пациентов групп исследуемых
препаратов и сравнения (абс. числ.)
|
|
|
|
Кол-во |
|
|
Мероприятия по купированию НПР |
|
|
|
||||||||
|
|
|
|
пациентов с |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
КТГ |
|
|
НПР |
|
Отмена |
Уменьшение |
Без |
|
|
Коррек- |
|||||||
|
|
|
|
|
|
|
|
|
дозы |
|
коррекции |
|
ция |
|
||||
|
|
|
|
Гр |
Гр |
|
Гр |
Гр |
Гр |
|
Гр |
Гр |
|
Гр |
|
Гр |
|
Гр |
|
|
|
|
ИП |
Ср |
|
ИП |
Ср |
ИП |
|
Ср |
ИП |
|
Ср |
|
ИП |
|
Ср |
|
Кардиология |
|
72 |
43 |
|
29 |
27 |
5 |
|
0 |
38 |
|
16 |
|
0 |
|
0 |
|
|
Эндокринолог |
|
7 |
0 |
|
1 |
0 |
0 |
|
0 |
6 |
|
0 |
|
0 |
|
0 |
|
|
ия |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Неврология |
|
3 500 |
9 |
|
29 |
0 |
2 |
|
0 |
3 469 |
|
9 |
|
0 |
|
0 |
|
|
Гинекология |
|
129 |
16 |
|
0 |
0 |
0 |
|
0 |
129 |
|
0 |
|
0 |
|
16 |
|
Дерматология/ |
|
68 |
20 |
|
1 |
0 |
0 |
|
0 |
67 |
|
20 |
|
0 |
|
0 |
||
|
аллергология |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Педиатрия |
|
1 |
0 |
|
1 |
0 |
0 |
|
0 |
0 |
|
0 |
|
0 |
|
0 |
|
|
Фтизиатрия |
|
55 |
52 |
|
0 |
7 |
нд |
|
нд |
нд |
|
нд |
|
нд |
|
нд |
|
|
ИТОГО |
|
|
3 832 |
140 |
|
61 |
34 |
7 |
|
0 |
3 709 |
|
45 |
|
0 |
|
16 |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Таким образом, среди 20 859 пациентов, принимавших участие в анализируемых исследованиях, НПР были зарегистрированы у 3 972 (19,04%)
чел., в группах исследуемых препаратов - у 3 832 (20,2%), в группах терапии сравнения - у 140 (7,5%).
Втаблице 4.3.3. представлено соотношение числа пациентов, у которых были зарегистрированы НПР к общему числу пациентов по группам наблюдения.
Таблица 4.3.3.
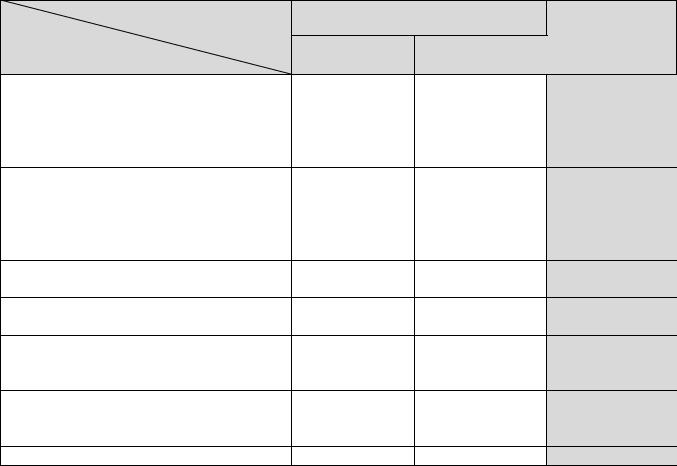
Профиль безопасности ЛС, изучаемых в постмаркетинговых КИ (абс.числа, %)
|
Группа исследуемого ЛС |
Группа сравнения |
|||
|
Кол-во |
Кол-во |
Кол-во |
Кол-во |
|
КТГ |
пациентов в |
пациентов с |
пациентов в |
пациентов с НПР |
|
|
группе |
|
НПР |
группе |
|
Педиатрия |
409 |
1 |
(0,2%) |
104 |
0 |
Кардиология |
6 497 |
72 (1,1%) |
1 043 |
43 (4,1%) |
|
Дерматология |
3 536 |
68 (1,9%) |
81 |
20 (24,7%) |
|
Эндокринология |
303 |
7 |
(2,3%) |
166 |
0 |
Гинекология |
3 423 |
129 (3,8%) |
182 |
16 (8,8%) |
|
Фтизиатрия |
406 |
55 |
(13,5%) |
220 |
52 (23,6%) |
Неврология |
4 416 |
3 500 (79,3%) |
72 |
9 (12,5%) |
|
142
Согласно полученным нами данным, НПР встречались у 1,1%
кардиологических больных, пролеченных исследуемыми препаратами и у 4,1%
больных из групп сравнения; у 2,3% больных с эндокринной патологией,
получавших в КИ изучаемые препараты; 79,3% больных неврологического профиля, пролеченных ИП и у 12,5 в группах сравнения; у 3,8% пациенток гинекологического профиля из ГрИП и у 8,5% из ГрСр; у 1,9% больных с аллергическими и кожными заболеваниями, пролеченными исследуемыми препаратами и у 24,7% больных из групп сравнения; у 0,2% пациентов группы педиатрия, получавших ИП; у 13,5% пациентов с туберкулезом, пролеченных ИП
иу 23,6% больных, получавших терапию в группах сравнения.
Втаблице 4.3.4. приведены данные о распределении НПР по органам и системам у пациентов групп исследуемых препаратов и групп сравнения.
|
|
|
Таблица 4.3.4. |
Распределение зарегистрированных в клинических исследованиях НПР по |
|||
органам и системам, группам наблюдаемых пациентов (абс.числ.) |
|||
|
Группы пациентов |
|
|
Группы пациентов |
|
|
ИТОГО |
Виды НПР |
ГрИП |
ГрСр |
по органам и |
по органам и системам |
|
|
системам |
ЦНС |
|
|
|
(сонливость, слабость, головокружение, |
2 194 |
13 |
2 207 |
атаксия, судороги, тремор, головная |
|
|
|
боль, преходящее нарушение мозгового |
|
|
|
кровообращения) |
|
|
|
ЖКТ |
|
|
|
(сухость во рту, металлический привкус |
674 |
36 |
710 |
во рту, снижение аппетита, боли в |
|
|
|
животе, боль в эпигастрии, изжога, |
|
|
|
тошнота, рвота, диспепсия, диарея) |
|
|
|
ОДА |
672 |
0 |
672 |
(мышечная слабость) |
|
|
|
ССС |
156 |
1 |
157 |
(нарушения ритма сердца, гипотония) |
|
|
|
Кожа |
|
|
|
(аллергические реакции, сухость, |
49 |
20 |
69 |
шелушение, зуд) |
|
|
|
МВС |
|
|
|
(дизурия, кандиоз влагалища, |
31 |
0 |
31 |
зуд,жжение половых органов) |
|
|
|
Изменения лабораторных |
|
|
|
143
показателей |
12 |
|
0 |
12 |
|
(гипергликемия, гипогликемия, |
|
|
|
|
|
повышение уровня мочевой кислоты, |
|
|
|
|
|
снижение уровня гемоглобина, |
|
|
|
|
|
эритроцитов, лейкоцитов, повышение |
|
|
|
|
|
АЛТ и АСТ) |
|
|
|
|
|
Органы зрения |
2 |
|
0 |
2 |
|
(нарушения зрения) |
|
|
|
|
|
Органы дыхания |
2 |
|
0 |
2 |
|
(кашель) |
|
|
|
|
|
Отеки |
2 |
|
0 |
2 |
|
(отеки голеней) |
|
|
|
|
|
Неклассифицируемые НПР |
83 |
|
89 |
172 |
|
|
|
|
|
|
|
ИТОГО НПР по группам: |
|
3 877 |
|
159 |
4 036 |
|
|
|
|
|
|
|
|
|
|
|
|
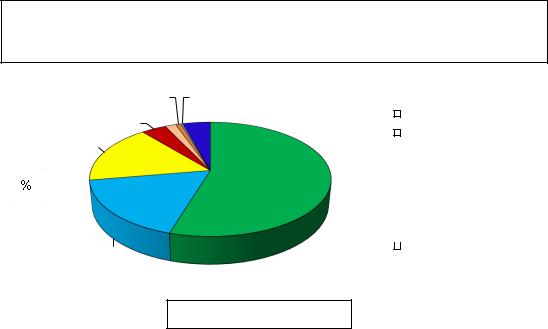
Наиболее часто нежелательные реакции развивались со стороны ЦНС - 54,7%,
ЖКТ - 17,6%, ОДА -16,7%, значительно реже - со стороны ССС (3,9%), кожи
(1,7%), МВС (0,8%), изменение лабораторных показателей было зарегистрировано в 0,3% случаев, на долю неклассифицируемых НПР приходилось 4,3% (рис. 4.3.1.).
Общее количество НПР в КИ = 4036 Количество пациентов с НПР = 3 972 (19,0%) Количество пациентов в КИ = 20 859
0,8 |
0,3 |
|
|
1,7 |
4,3 |
|
ЦНС |
|
|||
3,9 |
|
|
|
|
54,7 |
|
ЖКТ |
|
|
||
|
|
16,7

 ОДА
ОДА

 ССС
ССС

 Кожа
Кожа

 МВС
МВС

 Лабораторные показатели
Лабораторные показатели
 Неклассифицируемые НПР
Неклассифицируемые НПР
17,6
КИ = 169; ТН ЛС = 59
Рис. 4.3.1. Распределение НПР, зарегистрированных в ходе КИ, по органам и
системам (доля,%)
144
На рисунке 4.3.2. представлены данные по распределению НПР у пациентов
групп исследуемых препаратов по органам и системам.
Количество НПР у пациентов ГрИП = 3 877 Количество пациентов с НПР = 3 832 (20,2%)
Количество пациентов ГрИП = 18 991
1,3 |
0,8 |
0,3 |
|
|
|
|
|
2,25 |
|
|
ЦНС |
||
4 |
|
|
|
|
||
|
|
|
|
|||
|
|
|
|
|
|
|
17,3 |
|
|
|
56,6 |
|
ЖКТ |
|
|
|
|
|||
|
|
|
|
|||
|
|
|
|
|
||
|
|
|
|
|
ОДА |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
ССС |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Кожа |
|
|
|
|
|
|
|
|
|
|
|
|
|

 МВС
МВС

 Лабораторные показатели
Лабораторные показатели
17,4

 Неклассифицируемые НПР
Неклассифицируемые НПР
Рис. 4.3.2. РаспределениеНПР по органам и системам у пациентов, леченных в группах исследуемых препаратов (доля,%)
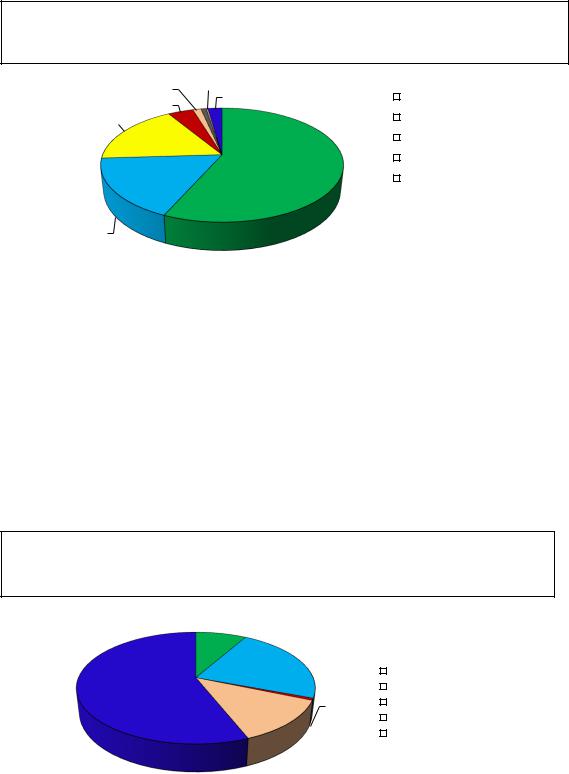
На рисунке 4.3.3. представлены данные по распределению НПР у пациентов групп сравнения по органам и системам.
Количество НПР у пациентов ГрСр = 159 Количество пациентов с НПР = 140 (7,5%)
Количество пациентов ГрСр = 1 868
8,2
22,6
56,0
|
|
ЦНС |
|
|
|
|
|
|
0,6 |
|
ЖКТ |
|
||
|
||
|
ССС |
|
|
||
|
||
|
|
Кожа |
|
|
|
|
|
|
|
|
Неклассифицируемые НПР |
|
|
|
|
|
 12,6
12,6
Рис. 4.3.3. РаспределениеНПР по органам и системам у пациентов, леченных в
группах сравнения (доля,%)
145
Анализ полученных нами данных показал, что в группах исследуемых препаратов НПР наиболее часто развивались со стороны ЦНС - 56,6%, ЖКТ -
17,4% и ОДА - 17,3%, редко - со стороны ССС - 4%, кожи - 1,3%, МВС - 0,8%,
изменение лабораторных показателей - 0,3%, неклассифицируемые - 2,25%.
В группах сравнения наиболее часто развивались неклассифицируемые НПР
(ввиду отсутствия описания реакции в анализируемых отчетах) - 56,0%, со стороны ЖКТ - 22,6%, кожи - 12,6%, ЦНС - 8,2%, очень редко - со стороны ССС
(0,6%). На наш взгляд, такую разницу в количестве НПР в группах терапии можно объяснить большим числом несравнительных по дизайну клинических исследований.
146
4.4. Особенности постмаркетинговых клинических исследований
лекарственных средств отечественного производства из различных
терапевтических направлений
Клинические исследования направления
«Кардиология»
Анализируя данные по проведенным исследованиям в контексте клинико-
терапевтических групп необходимо отметить, что самое большое их число пришлось на кардиологические препараты - в 53 исследования было включено 7 541 пациент, из них 3 570 женщин и 3 971 мужчина, в возрасте от 44 до 82 лет (средний возраст 56,69 ± 6,43), продолжительность наблюдения пациентов в исследованиях составляла от 4 до 24 недель (всреднем 18,14 ± 6,29).
Препараты изучались у больных с АГ (49,1%), ХСН (37,7%), ИБС (19,0%).
Вгруппах исследуемых препаратов наблюдалось 6 498 пациентов, в группах сравнения - 1 073. Разница количественного состава пациентов в основных и контрольных группах объяснима преимущественным числом несравнительных по дизайну КИ.
Входе всех анализируемых исследований НПР (нарушения ритма сердца, гипотония, умеренные головные болии др.) были зарегистрированы только у 115 пациентов (1,5%), из них пациенты ГрИП составили 62,6%, которым в 25,2% случаев препарат отменяли, в 4,3% потребовалось уменьшение дозы, в 33,0% случаев коррекция не потребовалась.
Вгруппах сравнения было 37,4% пациентов от общего числа с НПР, отмена препарата потребовалась в 23,5% случаев, 13,9% - без коррекции.
Врезультате НПР из всех исследований кардиологического направления выбыло 56 пациентов (0,7%), 7 443 завершили участие в соответствии с протоколами.
Наибольшим по численности включенных пациентов в данной клинико-
терапевтической группе было несравнительное фармакоэпидемиологическое исследование препарата Энаренал® - «ПОЛОНЕЗ» (№ 63 в Приложении 2, Глезер
147
М.Г., 2006 г.), в котором участвовало 4 291 пациент (из них 2 140 женщин) с АГ 1-
2 степени тяжести, пациенты принимали препарат на протяжении 8 нед., все завершили исследование.
В 29-ти исследованиях по изучению эффективности и безопасности препарата Акридилол® принимало участие 2 342 пациента (898 женщин и 1 444 мужчин),
завершили исследования 2 275 пациентов, в группы исследуемого препарата было включено было включено 1 493 чел., в группы сравнения - 849 чел.
Наиболее значимыми проектами по изучению эффективности и безопасности Акридилола являлись:
«АККОРД» (№28 в Приложении 2, Оганов Р.Г., 2007 г.) - 592 пациента (416 женщин и 176 мужчин) с АГ 1-2 степени тяжести в сочетании с СД 2 типа; продолжительность наблюдения пациентов составила 24 нед.; в ГрИП было включено 291 чел, в ГрСр (стандартная терапия без БАБ) - 301 чел.; завершили участие в исследовании 582 чел.
«АРХИМЕД» (№29 в Приложении 2, Беленков Ю.Н., 2007 г.) - 448
пациентов (205 женщин и 243 мужчины) с ХСН II-III ФК по NYHA;
продолжительность наблюдения пациентов в исследовании - 24 нед.; в ГрИП включено 223 пациента, в ГрСр (стандартная терапия без БАБ) - 225 чел.; завершили участие в исследовании 415 пациентов.
«АТЛАНТ» (№30 в Приложении 2, Морозова Т.Е., 2011 г) -
фармакоэпидемиологическое исследование по изучению влияния терапии карведилолом отечественного производства (Акридилол®) на сексуальную функцию у мужчин с неосложненной АГ 1-2 степени тяжести. В исследование было включено 200 мужчин; продолжительность наблюдения составила 8 нед.; все пациенты завершили исследование в соответствии с протоколом.
«КАБРИОЛЕТ» (№31 в Приложении 2, Марцевич С.Ю., 2011 г.) - 105
мужчин с АГ 1-2 степени с избыточной массой тела; продолжительность
наблюдения - 24 нед., в ГрИП включено 53 пациента, в ГрСр - 52; завершили
участие 98 чел.
148
В 13 клинических исследованиях изучалась эффективность и безопасность препарата Акрипамид® у 496 пациентов (300 женщин и 196 мужчин); в ГрИП было включено 429 пациентов, в ГрСр - 67 чел.; завершили участие в исследованиях 483 пациента.
Препарат Метокард® изучался в 4 КИ с общим участием 1134 пациентов (70 женщин и 64 мужчины), в ГрИП было включено 107 чел, в ГрСр - 27.
Акридипин® изучался в 2 КИ у 60 пациентов (45 женщин и 15 мужчин), в ГрИП включено 38 чел., в ГрСр - 22 чел.; выбывших из КИ пациентов не было.
Капозид® изучался в 1 КИ у 50 пациентов (25 женщин и 25 мужчин), в исследуемые групы было включено равное количество больных (Капозид = 25; Нолипрел форте = 25), период наблюдения составлял 24 нед., все пациенты завершили участие в соответствии с протоколом.
Препарат Тригрим® изучался в 1 КИ «ТРИОЛЯ» (№ 60 в Приложении 2, Агеев Ф.Т., 2012 г) у 108 пациентов (59 женщин и 49 мужчин) с ХСН II-III ФК по
NYHA; продолжительность наблюдения составила 24 нед.; в ГрИП было включено 55 пациентов, в ГрСр (фуросемид) - 53; завершили участие в исследовании 95 чел.
Препарат Тромбопол® изучался в 1 перекрестном по дизайну исследовании терапевтической эквивалентности «ИКАР» (№59 в Приложении 2, Марцевич С.Ю., 2010 г.) у пациентов высокого риска сердечно-сосудистых осложнений. В исследовании участвовало 30 пациентов (16 женщин и 14 мужчин) которые наблюдались на протяжении 9 нед. Согласно дизайну исследования все пациенты принимали исследуемый препарат и препарат сравнения (Аспирин Кардио®),
выбывших из КИ пациентов не было.
Клинические исследования направления
«Эндокринология»
По эндокринологии в 16 КИ было включено 469 пациентов, 295 женщин и 174 мужчины, в возрасте от 43 до 66 лет (средний возраст 56,75 ± 5,47),
149
продолжительность наблюдения пациентов в исследованиях составила от 2 до 52
нед. (в среднем 15,57 ± 11,84). Завершили участие в исследованиях 462 чел.
В 81,2% КИ изучение препаратов проводилось у пациентов с СД 2 типа, в
12,5% - с гипофункцией щитовидной железы, 6,3% - у пациентов с гипотиреозом.В группы исследуемых препаратов было включено 303 чел., в
группы сравнения - 166 чел.
В ходе всех исследований только у 7 пациентов были зарегистрированы НПР,
что составило 1,5% от числа больных, участвовавших в них. Одному пациенту препарат был отменен, всем остальным коррекция не потребовалась.
Наиболее изученными из числа препаратов данного направления были сахароснижающие препараты Глимекомб®, Глиформин® и Глидиаб® МВ, в 13 КИ по данным препаратам было включено 409 пациентов с СД 2 типа (254 женщины и 155 мужчин), в ГрИП было включено 243 чел, в ГрСр. - 166 чел., завершили исследования 405 пациентов.
Препарат L-Тироксин-Акри® изучался в 3 несравнительных КИ у 60 пациентов
(41 женщина и 19 мужчин) с заболеваниями щитовидной железы, из которых завершили исследования 57 чел.
Клинические исследования направления
«Неврология»
В группе неврологических препаратов за весь анализируемый период времени было проведено 10 КИ, в которых участвовало 4 488 пациентов, 2 835 женщин и
1 653 мужчины в возрасте от 35 до 50 лет (средний возраст 40,76 ± 5,76),
продолжительность наблюдения в исследованиях составила от 1 до 12 нед. (в
среднем 4,0 ± 3,16). В группы ИП было включено 4 416 пациентов, в ГрСр - 72
(что объяснимо преимущественно несравнительным дизайном проводимых исследований). Завершили участие по протоколам 4 456 чел.
Среди изучаемых нозологий 50,0% приходилось на МБС, 20% - на мигрень, по
10% - на эпилепсию, тригеминальную невралгию, дисциркуляторную энцефалопатию.
150
В ходе исследований НПР были зарегистрированы у 3 509 (78,2%) пациентов, при этом выбыли из исследований ввиду НПР только 29 (0,6%). В группах исследуемых препаратов НПР развивались у 3 500 (79,3%) пациентов, в группах сравнения - у 9 (12,5%).
Наиболее изученным препаратом являлся Баклосан®, по которому было проведено 4 КИ с общим числом пациентов 4 291. Самым крупным проектом было исследование «BRAVO» (№95 в Приложении 2, Корешкина М.И., 2009 г.), в котором участвовало 4 201 пациент (2 668 женщин и 1 533 мужчины) с дорсопатиями; продолжительность наблюдения пациентов в исследовании составила 4 нед. В ходе данного исследования НПР были зарегистрированы у 3 474 (82,7%) пациентов (1134 - сонливость; 714 - головокружение; 672 -
мышечная слабость; 462 - тошнота; 147гипотензия; 126 - атаксия; 84 - судороги;
63 - диарея; 42 - тремор; 21 - рвота; 9 - дизурия), которые в большей мере не требовали коррекции, при этом только 29 (0,7%) пациентов выбыли из участия из-
за плохой переностимости Баклосана.
Препараты Карбалепсин® ретард и Топалепсин® изучались только в пилотных проектах с небольшим числом участников (12 и 18 соответственно), впоследствии были выведены из промоции и дальнейшего изучения в клинических исследованиях не получили.
Сумамигрен изучался в 2 клинических исследованиях у 57 пациентов с мигренью, Месипол® и Диакарб® изучались в 1 исследовании каждый с участием 50 и 60 пациентов соответственно. В целом, переносимость данных препартов в исследованиях была хорошей, в результате НПР выбывших пациентов не было. Однако на Месипол® было зарегистрировано 13 НПР (10 - со стороны ЖКТ и 3 -
со стороны ЦНС).
Клинические исследования направления
«Гинекология»
По препаратам гинекологического направления было проведено 25 ПмИс с общим числом включенных в них женщин 3 605, в том числе 311 беременных в
