
Общие вопросы / Хосева 2014 Диссертация
.pdf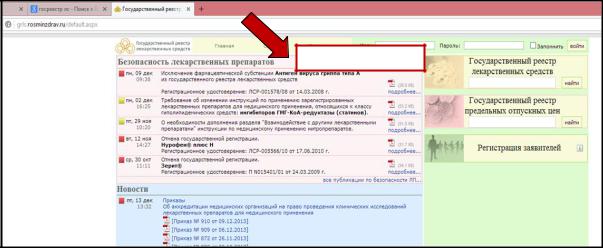
191
незарегистрированные или зарегистрированные для временного входа пользователи могли бы заполнить электронную версию формы. Кроме того,
данная форма должна быть доступна в формате word-документа для распечатки,
заполнения и отправки почтой/факсом, либо сканированным документом.В этом же поле может располагаться разработанная специально для пациентов форма-
извещение о НПР (рис. 7.1.4.).
Извещение о НПР
Рис. 7.1.4. Дополнительная закладка на главной странице Государственного реестра ЛС с бланком формы-извещения о НПР
Таким образом, внесение дополнительных полей в Государственный реестр лекарственных средств сделает данный ресурс более информативным для всех субъектов обращения лекарственных средств.
192
7.2. Совершенствование системы мониторинга эффективности и
безопасности лекарственных средств на уровне
учреждений практического здравоохранения
Несмотря на активную работу регуляторных органов по развитию и совершенствованию системы фармаконадзора в нашей стране, на сегодняшний день остается много нерешенных проблем.
Анализ литературы и результаты нашего исследования показали, что среди причин занижения врачами сведений о НПР, наиболее значимыми являются непонимание актуальности данной проблемы, большая загруженность медицинских работников и отсутствие у них времени для составления отчетов,
наличие бюрократических процедур, страх преследования и последствий сообщения, отсутствие обратной связи на локальном уровне, которая является важным мотивационным фактором для врача.
Среди врачей, участвующих в нашем опросе, только половина (56%) знают, что в ЛПУ есть врач-клинический фармаколог, остальные не знают или утверждают,
что такого специалиста нет. При этом за консультацией к нему «всегда» обращаются только 14% врачей, «иногда» – 28%; основными мотивами таких обращений служат случаи выявления НПР (33%), уточнение дозировок ЛС (12%)
и лекарственных взаимодействий (24%).
Вместе с тем, наше исследование показало, что половина (54%) опрошенных фармацевтов и около четверти (23%) врачей рекомендуют лекарства с нарушением предписаний к применению («off-label»), по несоответствующим показаниям и в неадекватных дозировках.
Подавляющее большинство респондентов отметили, что нуждаются в специальных обучающих программах по вопросам безопасности лекарственной терапии.
На уровне ЛПУ наиболее компетентным сотрудником, выполняющим функции уполномоченного по фармаконадзору, является врач-клинический фармаколог, в должностные обязанности которого входит «организация
193
регистрации неблагоприятных побочных реакций и проведение анализа возникших побочных эффектов лекарственных средств, а также осуществление контроля за своевременным информированием в установленном порядке центров по регистрации неблагоприятных побочных реакций о зарегистрированных побочных эффектах лекарственных средств» [126]. Однако в настоящее время не все ЛПУ имеют в штате врача-клинического фармаколога.
Для осуществления функции мониторинга безопасности ЛС на уровне ЛПУ необходимо:
назначить ответственных лиц по фармаконадзору в лечебном учреждении
[112];
обеспечить сбор и внесение информации о НПР от врачей, среднего медперсонала, фармацевтических работников аптечных пунктов при ЛПУ,
потребителей/пациентов путем заполнения электронной формы-извещения о НПР через автоматизированную информационную систему (АИС - Росздравнадзора)
«Фармаконадзор» или бумажной версии [100];
ведение базы данных/реестра НПР на уровне ЛПУ;
предоставление уточняющей информации о НПР, выявленных на территории ЛПУ, по запросам от региональных центров мониторинга безопасности/территориальных управлений Росздравнадзора/отдела мониторинга эффективности и безопасности ЛС Росздравнадзора;
доведение до сведения медицинских работников ЛПУ изменений законодательной базы в области фармаконадзора в РФ; информационных писем Росздравнадзора об отзыве/приостановлении обращения/возобновлении обращения ЛС на территории РФ в связи с новыми данными по эффективности/безопасности;
информирование сотрудников ЛПУ о порядке заполнения карт-извещений и сроках предоставления информации о НПР уполномоченному лицу по фармаконадзору в ЛПУ и в регуляторные органы; о новых данных по безопасности ЛС, опубликованных на сайте Росздравнадзора;
194
организация врачебных конференций по вопросам рационального применения ЛС, побочным эффектам и лекарственным взаимодействиям;
организация образовательных программ по безопасному применению лекарств и сообщению о случаях НПР для пациентов в рамках школ здоровья;
для пациентов должны быть свободно доступны буклеты, содержащие информацию по основным вопросам безопасности лекарственной терапии, а
также печатные бланки форм-извещений, которые можно размещать в специализированных подставках с надписью «Здесь Вы можете заполнить извещение о побочной реакции лекарства» на стойке медсестринского поста в отделениях стационаров любого профиля, в поликлиниках на стойках регистратуры, либо выделенного для этих целей стола/стойки.
Результаты наших и зарубежных исследований показали низкую вовлеченность работников первого стола аптек в процесс фармаконадзора. В последнее время в данном направлении делаются первые шаги на уровне региональных подразделений системы фармаконадзора.
Так организованный на базе Нижегородского областного центра по контролю качества и сертификации ЛС региональный центр мониторинга безопасности в
2011 г. выступил с инициативой включения в процесс мониторинга аптечных учреждений области. Среди провизоров и фармацевтов ведется информационная работа, разъясняются причины возникновения НПР и действия первостольника при обращении потребителей с данной проблемой, особый акцент сделан на выявление недоброкачественных и фальсифицированных лекарств, вызвавших НПР [113].
На наш взгляд, данный опыт должен быть поддержан на федеральном уровне с привлечением к образовательному процессу учебных учреждений системы послевузовского профессионального образования, региональных центров мониторинга безопасности ЛС и территориальных подразделений Росздравнадзора.
Согласно действующему в нашей стране «Отраслевому стандарту
91500.05.0007-2003«Правила отпуска (реализации) лекарственных средств в
195
аптечных организациях. Основные положения» [105], розничные аптечные организации, при отпуске ЛС населению, предоставляют информацию по надлежащему использованию и хранению препаратов, оказывают консультативную помощь в целях обеспечения ответственного самолечения. В
аптечных организациях должна быть предусмотрена система постоянного повышения профессионального образования сотрудников по вопросам действующего законодательства, применения ЛС и др. Кроме того, согласно данному документу, в розничной аптеке из руководящего персонала назначается сотрудник, уполномоченный по качеству.
По нашему мнению, специалист по качеству ЛС может исполнять обязанности уполномоченного по фармаконадзору.
Для осуществления функции мониторинга безопасности ЛС на уровне розничной аптеки необходимо:
выделить сотрудника, ответственного за мониторинг безопасности ЛС
(специалист/уполномоченный по фармаконадзору/уполномоченный по качеству)
и рассмотреть вопрос о возможности получения персонифицированного доступа в систему АИС-Росздравнадзора «Фармаконадзор»;
в аптеке должны быть в наличии бланки-извещения о НПР, которые могут быть заполнены сотрудником, прошедшим подготовку по основам фармаконадзора, либо непосредственно пациентом;
специалист по фармаконадзору должен проводить информационно-
образовательную работу среди сотрудников своей аптеки с освещением общих вопросов фармаконадзора; правил работы с потребителями в случае их обращения по поводу сомнительного качества ЛС, НПР/отсутствия ожидаемого терапевтического эффекта; принципов заполнения и отправки спонтанных сообщений;
ответственный по фармаконадзору должен регулярно мониторировать информацию о безопасности, отзыве с рынка ввиду ухудшения качества, случаях выявления фальсифицированных ЛС, БАД, лекарственного растительного сырья на сайте Росздравнадзора и доводить ее до сведения сотрудников аптеки;
196
в аптеках необходимо распространение информации о безопасности лекарств среди потребителей в виде плакатов и буклетов, содержащих информацию о НПР и фармаконадзоре, куда и как они могут сообщить о НПР;
для потребителей должны быть свободно доступны печатные бланки форм-
извещений, которые можно размещать в специализированных подставках с надписью «Здесь Вы можете заполнить извещение о побочной реакции лекарства» на выделенном столе, где потребителям (в большинстве аптек есть данная опция) проводится контроль артериального давления, либо выделить для этого отдельный стол/стойку.
Таким образом, внедрение системы фармаконадзора на уровне учреждений практического здравоохраненияповысит ответственностьмедицинских работников в отношении мониторинга эффективности и безопасности ЛС,
обращающихся на фармацевтическом рынке в нашей стране, а также позволит повысить информированность населения в вопросах эффективности и безопасности ЛС, будет способствовать привлечению пациентовк системе фармаконадзора.
197
7.3. Образовательные программыпо вопросам фармаконадзора и Надлежащей клинической практики (GCP) для специалистов практического здравоохранения и сотрудников фармацевтических компаний
В настоящее время ключевыми направлениями государственной политики нашей страны в сфере ЛО являются всеобщность, доступность, качество,
эффективность и безопасность, рациональность, открытость и
сбалансированность. Эти приоритеты закреплены в одобренной в конце 2012 г.
Стратегии лекарственного обеспечения населения Российской Федерации на период до 2025 года (далее - Стратегия ЛО) [140].
Среди основных проблем ЛО в нашей стране Стратегией обозначены:
недостаточное развитие российской фармацевтической промышленности, как источника доступных ЛС; случаи нерациональных и неэффективных лекарственных назначений; самолечение и безответственное применение ЛС без
медицинских показаний; низкий уровень вовлечения профессиональных
ассоциаций в повышение квалификации медицинских и фармацевтических кадров.
Весьма перспективным направлением в рамках Стратегии является повышение
информированности населения в вопросах ЛО путем формирования
ответственного отношения к своему здоровью (поддержка и развитие «школ пациента»); повышение квалификации медицинских и фармацевтических работников на этапах профессиональной и последипломной подготовки по рациональному использованию ЛС.
Политика нашего государства в сфере рационального применения ЛС согласуется с мировыми тенденциями в этой области. Так в Меморандуме ВОЗ по национальной стратегии в области безопасных ЛС и их надлежащего
использования говорится о том, что хорошо организованная система
фармаконадзора способствует снижению рисков, связанных с применением ЛС,
предупреждению развития НПР [98]. Особый акцент в Меморандуме сделан в
198
отношении вузовского и непрерывного образования медицинских работников в области оценки пользы/риска и рационального использования лекарств, а также предоставления специалистам и населению информации о безопасности ЛС с целью уменьшения случаев нерациональной фармакотерапии и самолечения.
Образовательные программы в системе дополнительного профессионального образования специалистов практического здравоохранения
и сотрудников фармацевтических компаний
Учитывая изменения законодательства РФ в сфере обращения ЛС, а также следуя перспективным направлениям Стратегии ЛО, с 2010 г. нами были разработаны и внедрены в образовательный процесс кафедры клинической фармакологии и фармакотерапии ИПО ГБОУ ВПО Первого МГМУ им. И.М.
Сеченова Минздрава России образовательные программы в виде отдельных дополнительных модулей для врачей-терапевтов по вопросам фармаконадзора и контроля безопасности лекарственной терапии.
Более глубокие знания по фармаконадзору, включающие теоретические,
практические и административные аспекты, получают врачи-клинические фармакологи, проходящие обучение по программе повышения квалификации и программе профессиональной переподготовки по специальности «Клиническая фармакология».
Также в рамках специальности «Клиническая фармакология» нами разработаны учебно-методические комплексы (УМК) программ повышения квалификации «Актуальные вопросы фармаконадзора и контроля безопасности лекарственных средств» и «Клинические исследования лекарственных средств по правилам Надлежащей клинической практики (GCP)».
Модуль по НПР и фармаконадзору в рамках УМК имеет продолжительность от
18 до 72 академических часов, по Надлежащей клинической практике - 72
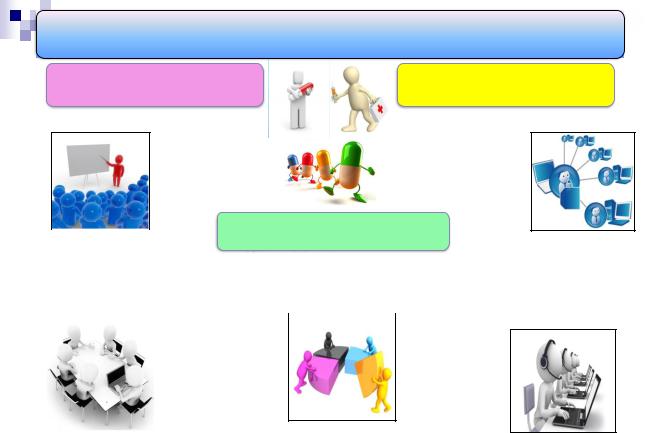
академических часа, и состоит из теоретического и практического блоков. На рисунке 7.3.1. представлены формы обучения по основам фармаконадзора и
199
Надлежащей клинической практике (GCP).
Программы повышения квалификации
Основы фармаконадзора и Надлежащей клинической практики (GCP)
«Клиническая фармакология» |
|
|
|
|
«Терапия» |
Врачи-клинические фармакологи |
|
|
|
|
Врачи лечебных специальностей |
Лекционный блок |
|
|
|
|
Вебинар |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
«Фармация / Аптечное дело» |
|||
|
|
|
|
Фармацевты |
||
Основы рациональной фармакотерапии |
||||||
Сотрудники фармацевтических компаний |
||||||
Термины/определения по фармаконадзору |
||||||
|
|
|
||||
Методы выявления/изучения НПР |
|
|
|
|||
|
Классификации НПР |
|
|
|
||
Особенности системы фармаконадзора |
Активное обучение |
|||||
|
ПСС «НПР-ЛС» |
|||||
|
|
(ролевая игра) |
||||
|
|
|
|
|||
Практические занятия |
|
|
|
|||
|
|
|
||||
|
|
|
Модель ситуации «Случай НПР у пациента» |
|
|
|
|
Правила заполнения формы-извещения о НПР |
Роли участников тренинга: |
||
Сроки и способы отправки спонтанных сообщений |
Врач/Пациент/Клинический фармаколог/ |
||
Оценка ПСС «НПР-ЛС» по алгоритму Наранжо |
Провизор/Фармкомпания/ |
||
|
Решение ситуационных задач |
Сотрудник регионального центра МБЛС/ |
|
|
Тестовый контроль |
Сотрудник центра МБЛС Росздрава/ |
|
|
|
|
Центр безопасности ЛС ВОЗ |
Теоретическая часть:
Система фармаконадзора, терминология, Классификации и методы выявления НПР, Практическая часть:
Заполнение Формы-извещения о НПР ПСС «НПР-ЛС» по алгортму Наранжо
Дистанционное обучение
Программное обеспечение e-Learning Теоретическая часть
(основы фармаконадзора) Практическая часть: Тестовый контроль
Заполнение форм-извещений о НПР
Рис. 7.3.1. Формы обучения по основам фармаконадзора и Надлежащей клинической практики (GCP)
Теоретический материал содержит основные сведения о проблеме безопасности ЛС; о принципах рациональной фармакотерапии; термины и определения в области фармаконадзора; классификации НПР; методы выявления и изучения НПР; определение степени достоверности причинно-следственных связей НПР с приемом ЛС; особенности организации системы фармаконадзора на уровне нашей страны и мира в целом; алгоритм взаимодействий участников системы фармаконадзора.
Особое внимание уделено спонтанным сообщениям, особенностям заполнения карт-извещений о НПР, срокам предоставления информации о НПР и способам отправки сообщений в регуляторные органы.
200
Особенностью преподавания основ фармаконадзора в рамках УМК является дифференцированный подход к организации учебного процесса в зависимости от целевой аудитории и уровня базовых знаний слушателей.
Так для врачей лечебных специальностей первичного звена особое внимание уделено актуальности проблемы с целью формирования осознанного отношения к НПР, необходимости их выявления и предупреждения; роли медицинских ошибок, полипрагмазии, нерационального использования ЛС и самолечения в развитии НПР; проблеме назначения лекарств с нарушением предписаний в инструкции по медицинскому применению (off-label);
особенностям развития НПР у пациентов групп высокого риска (дети, пожилые люди, беременные и кормящие женщины); навыкам заполнения и срокам отправки спонтанных сообщений в регуляторные органы.
С врачами клиническими фармакологами кроме общих вопросов обсуждаются особенности организации системы фармаконадзора на уровне ЛПУ;
обязанности врача клинического фармаколога по мониторингу безопасности ЛС;
особенности работы с АИС-Росздравнадзора «Фармаконадзор»; роль врача клинического фармаколога в организации образовательных программ для сотрудников ЛПУ и пациентов.
Практическая часть занятий включает работу с формой-извещением о НПР,
алгоритмом Наранжо для определения степени причинно-следственных связей НПР-ЛС, решение ситуационных задач и тестовый контроль.
Впервые в рамках практических занятий нами внедрен метод активного обучения (ролевая игра), направленный на развитие знаний, умений и навыков у слушателей цикла. В процессе игры моделируется ситуация возникновения у пациента НПР, каждый участник тренинга выступает в определенной роли
(пациент, врач, провизор, врач-клинический фармаколог, компания-
производитель ЛС, сотрудник регионального центра мониторинга безопасности ЛС, сотрудник центра мониторинга безопасности ЛС Росздравнадзора, сотрудник центра безопасности ЛС ВОЗ), что позволяет понять принцип функционирования каждого звена и системы фармаконадзора вцелом в условиях, приближенных к
