
- •1. Терминология,
- •2. Энергетика процессов
- •3. Критерии направленности процессов и равновесия
- •4. Химическое равновесие
- •1. Терминология, основные понятия и определения
- •1.1. Термодинамическая система
- •1.2. Термодинамические параметры
- •1.3. Термодинамический процесс и термодинамическое равновесие
- •1.4. Функции пути осуществления процесса и функции состояния
- •1.5. Химический процесс и химическая переменная
- •1.6. Модели идеальных систем в химической термодинамике. Реальные системы
- •2. Энергетика процессов
- •2.1. Первое начало термодинамики (постулат о существовании внутренней энергии)
- •2.2. Термодинамическая работа
- •2.3. Внутренняя энергия и теплота
- •2.4. Энтальпия
- •2.5. Взаимосвязь работы и теплоты с изменениями внутренней энергии и энтальпии в изопроцессах с участием идеального газа
- •2.6. Теплоёмкость
- •2.7. Фазовые переходы I рода
- •2.8. Зависимость теплоёмкости от температуры
- •Простых веществ
- •2.9. Зависимость внутренней энергии и энтальпии от температуры
- •2.10. Зависимость внутренней энергии, энтальпии и теплоемкости от давления
- •2.11. Изменение внутренней энергии и энтальпии в химических реакциях
- •2.12. Экспериментальные методы определения тепловых эффектов химических реакций
- •2.13. Стандартные тепловые эффекты
- •2.14. Зависимость теплового эффекта от температуры. Уравнение Кирхгофа
- •Температуры:
- •2.15. Интегрирование уравнения Кирхгофа
- •2.16. Зависимость энтальпии реакции от давления
- •3. Критерии направленности процессов и равновесия в системах постоянного и переменного составов
- •3.1. Второе начало термодинамики (постулат о существовании энтропии)
- •3 .1.1.С в о и ств а энтропии. Энтропия как критерий направленности самопроизвольных процессов и равновесия в изолированных системах
- •3.1.2. Связь энтропии с параметрами
- •3.1.4. Изменение энтропии при обратимых фазовых переходах I рода
- •3.1.5. Статистическое толкование энтропии. Уравнение б ольцма иа -Пл анка
- •3.1.7. Расчет абсолютных значений энтропии
- •Абсолютной энтропии
- •3.1.8. Изменение энтропии в химических
- •3.2. Критерии направленности процессов и равновесия в неизолированных системах
- •3.2.1. Объединенное уравнение первого и второго начал термодинамики
- •3.2.4. Зависимости энергии Гиббса и энергии Гельмгольца от основных параметров состояния
- •Веществ
- •Веществ
- •Веществ
- •Веществ
- •При наличии фазовых превращений
- •3.2.7. Уравнения г и б б с а-г е л ь м г о л ь ц а
- •3.2.8. Вывод уравнений для зависимостей термодинамических функций от давления и объема
- •3.2.9. О "сложности" преобразований при выводе уравнений химической термодинамики
- •Функций по параметрам состояния
- •3.3. Критерии направленности процессов и равновесия в системах переменного состава
- •3.3.1. Химический потенциал
- •3.3.2. Свойства химического потенциала
- •3.3.3. Химический потенциал моля идеального газа
- •3.3.4. Химический потенциал компонента смеси идеальных газов
- •4. Химическое равновесие
- •4.1. Химическое равновесие в смеси идеальных
- •4.2. Расчет стандартного химического сродства
- •4.3. Стандартное химическое сродство и термодинамическая константа равновесия как характеристики равновесного состояния
- •4.4. Химическое сродство как критерий направленности процесса
- •4.5. Зависимость константы равновесия от температуры
- •4.5.1. Дифференциальная форма уравнений изобары и изохоры химической реакции
- •4.6. Расчет термодинамической константы равновесия
- •4.6.1. Общая характеристика фонда справочных данных
- •4.6.2. Способы расчета термодинамической константы равновесия
- •4 . 7 . 1.Реа к ц и и в смесях газов.
- •Связь термодинамической константы равновесия с
- •Эмпирическими (концентрационными) константами
- •Равновесия:Кр', кх,кп,кс
- •4.7.2.Реакции в гомогенной конденсированной фазе (реакции в растворах)
- •4.7.3. Реакции в гетерогенных системах
- •4.8. Расчет состава равновесной смеси по величине термодинамической константы равновесия
- •4.8.1.Химическое превращение представлено единственным уравнением
- •4.8.2.Химическое превращение представлено двумя уравнениями
- •4.8.3. Множественные реакции
- •4.9. Влияние различных факторов на состав
4.4. Химическое сродство как критерий направленности процесса
в смесях произвольно заданного состава
,
Чтобы ответить на вопрос о направленности химического процесса, необходимо при заданной температуре знать начальный состав смеси и величину термодинамической константы равновесия.
Запишем уравнение изотермы в несколько иной форме:

и проанализируем полученное выражение, рассмотрев с этой целью три ситуации:
1) если Y[> Kg , то ArGp)T > 0 и, следовательно, прямая реакция не идет, а
самопроизвольно протекает обратная, в ходе которой расходуются продукты;
2) если ]"[< Ка , то ArGpj <0 - самопроизвольно идёт прямая реакция, и
расходуются исходные вещества;
3) если концентрация продуктов в смеси равна нулю, то ArGp>T =-oo и,
следовательно, реакция обязательно начнется независимо от того, чему равно стандартное сродство ArGy и, соответственно, К° .
Таким образом, направление процесса характеризует величина ДгОрт>
тогда как ArGj является характеристикой равновесного состояния. При данной температуре может существовать бесконечное множество значений ArGpjT, но единственное значение ArG^-. Это показано на рис.22.
126
[p# 129]

Рис. 22. Изменение энергии Гиббса в закрытой системе переменного состава, обусловленное протеканием химической реакции
Минимум на кривой, приведенной на рис.22, отвечает равновесному составу смеси. Состав смесей, находящихся слева и справа от точки минимума должен изменяться в связи с самопроизвольным протеканием реакции. Слева от минимума происходит прямая реакции, справа - обратная.
На рис.23 показано, как изменяется положение минимума энергии Гиббса в зависимости от величины константы равновесия. Как видно, чем больше К^, тем меньше концентрация исходных веществ в равновесной смеси,
Может возникнуть вопрос, сталкиваемся ли мы с определением знака ArGptT при решении технологических задач? Ответ однозначен - сталкиваемся
постоянно. Для иллюстрации рассмотрим один из примеров. Известно, что термодинамическая константа реакции
СОС12(г)оС12(г) + СО(г)
составляет 21,4 при 1000 К. Требуется определить в какую сторону будет направлен процесс, если при общем давлении, равном 2 атм, смесь, содержащая 1 моль фосгена, 3 моля хлора и 1 моль СО будет нагрета до указанной температуры.
4. Химическое равновесие
127
[p# 130]
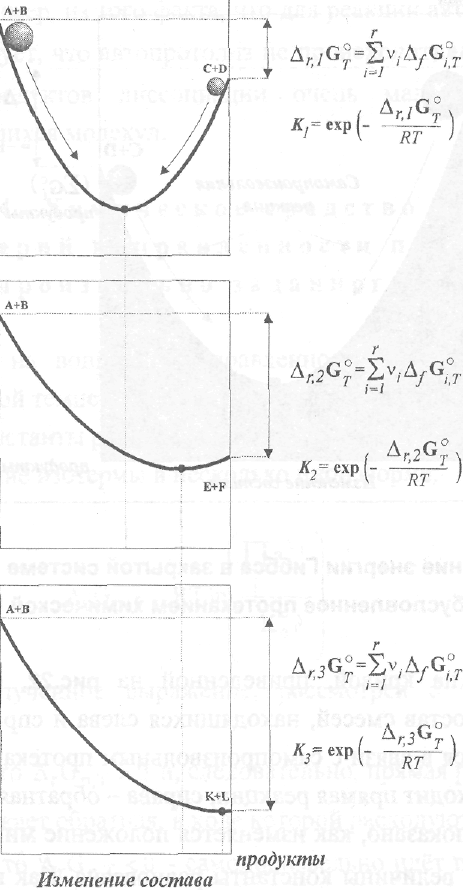
Рис. 23. Изменение координаты состава равновесной смеси, обусловленное возрастанием константы равновесия: К° <К° < К°
Решение задачи сводится к определению знака химического сродства. С этой целью необходимо, воспользовавшись выражением

вычислить отношение термодинамической константы равновесия рассматриваемой реакции (Кт) к величине произведения, совпадающего по
128
[p# 131]
форме с Кт, но относящееся к исходным характеристикам реакционной смеси
<ГК! )•
i
Поскольку реакция проводится при высокой температуре и сравнительно невысоком давлении, можно полагать, что активности компонентов газовой смеси совпадают с их парциальными давлениями:
![]()
![]()
С учетом изложенного получаем:

Отрицательный знак химического сродства указывает на развитие процесса в направлении диссоциации введенного фосгена.
Сходные задачи приходится решать при постановке самых разнообразных задач, например:
будет ли осуществляться превращение SC>2 в 8Оз при подаче в реактор смеси SC>2, SC>3 и О2 заданного состава или же, наоборот, 8Оз будет разлагаться?
будет ли происходить окисление металла при заданной температуре в среде с известным парциальным давлением кислорода?
будут ли разлагаться карбонаты при термообработке в среде с известным давлением СС>2?
будет ли выветриваться кристаллогидрат в среде с известной влажностью?
• будет ли образовываться осадок малорастворимой соли при смешивании растворов, содержащих ионы, образующие эту соль?
[p# 132]
4. Химическое равновесие
129
[p# 133]
