- •1.Факторы, влияющие на растворимость газов. В предельно разбавленных растворах растворимость газов пропорциональна их парциальному давлению над раствором -з-н Генри).
- •2.Зависимость растворимости газа от температуры.
- •Соударения молекул газа с поверхностью жидкости
- •3.Факторы,влияющие на растворимость газов в жидкостях
- •Природа растворённого газа и растворителя
- •Давление газа
- •Присутствие др. Вещ-в ( особенно электролитов)
- •4.Типы растворов жидкостей в жидкостях, причины их разнообразия.
- •5.Идеальные растворы. Построение их диаграммы «давление – состав», температура кипения – состав.
- •6.Вывод зависимости давления насыщенного пара смеси от состава жидкой и паровой фаз.
- •7. Реальные р-ры жидкостей неограниченно растворимые друг в друге. Причины отклонения давления паров над раствором от з-на Рауля.
- •8.Диаграммы давление –состав и температура – состав для реaльных растворов
- •9.Первый з-н Канавалова
- •10.Методы разделения смесей. Ректификация.
- •11. Диаграмма состояния р-ров ,образующих азеотропы.2й з-н Коновалова.
- •Термодинамическое док-во II з-на Кановалова
- •12.Диаграмма «давление – состав» и «температура – состав» Жидкости, ограниченно растворимых друг в друге.
- •13.Диаграммы “Давление-состав” и “температура-состав” для жидкостей, взаимно нерастворимых друг в друге.
- •15. Трехкомпанентные системы. Графическое представление. Определение методами Розебома и Гиббса.
- •19.Проводимость в газах, жидкостях и твердых телах. Электропроводность удельная и эквивалентная. Основные полож-я теории сильных эл-тов. Термодтнамика р-ров сильных эл-тов.
- •20. Скорость движ-ния иона,абсолютная ск-сть движ-я иона,подвижность.
- •21. Вывод уравнения, связывающего эквивалентную электропроводность с подвижностями ионов.
- •23.Влияние различных факторов на электропроводность для р-ров сильных электролитов.
- •25. Ионная сила р-ра. Ионный радиус, ионная атмосфера. Электрофоретическое и релаксационное торможение. Эффект Вина,понятие дисперсии электропроводности.
- •26. Активности и коэффициенты активности электролитов. Вычисление средних коэффициентов активности ионов.
- •27. Кондуктометрическое титрование как метод определения точки эквивалентности при титровании, изменения состава растворов для расчета степени диссоциации, констант диссоциации.
- •28. Понятие об электродвижущих силах, полуэлементе, элементе. Термодинамический вывод уравнения для определения электродного потенциала, уравнение Нернста.
- •29. Термодинамика гальванических элементов.
- •30. Водородный скачок потенциала. Стандартные электродные потенциалы.
- •31. Виды гальванических элементов. Электроды 1-го и 2-го рода. Обратимые, необратимые цепи. Знаки эдс-элементов. Вычисление эдс обратимого гальванического элемента.
- •32. Окислительно-восстановительные электроды или редокс-элементы.
- •33. Химические цепи. Уравнение для расчета эдс.
- •34. Концентрационные цепи. Уравнение для расчета эдс
- •35. Диффузионный скачок потенциала.
- •Потенциометрическое титрование. Электрохимические методы определения рН растворов.
- •Основные понятия химической кинетики: молекулярность, скорость реакции (начальная, истинная и средняя), константа скорости.
- •Вывести уравнение Аррениуса. Энергия активации. Предэкспоненциальный множитель. Методы их определения.
- •39. Порядок реакции по реагенту и методы его экспериментального определения. Лимитирующая стадия химического процесса.
- •Вывод интегрального кинетического уравнения для необратимой и обратимой реакции первого порядка.
- •Вывод интегрального кинетического уравнения для необратимой реакции второго порядка.
- •Вывести уравнение кинетики для параллельных реакций.
- •Вывести уравнение кинетики для гомогенной необратимой последовательной реакции первого порядка
- •Вывести уравнение скорости процесса в потоке, режим идеального вытеснения в стационарных условиях.
- •45. Кинетика гомогенных реакций первого порядка, протекающих в условиях идеального перемешивания.
- •Теория активных соударений и расчет скорости по числу соударений.
- •47. Теория переходного состояния и вывод основного уравнения.
- •50.Кинетика р-ий с неразветвленными цепями.
- •51.Вывод кинетических уравнений цепных р-ий в стационарном приближении
- •52.Пределы воспламенения и взрыва. Механизмы вопламенения.
- •53. Связь кинетики и макрокинетики при протекании экзотермических реакций (теория теплового взрыва)
- •Теория теплового взрыва была разработана в работах Зельдовича и Франк-Каменецкого. Кратко рассмотрим анализ теплового режима в случае сильно экзотермической реакции.
- •Где cp и r означают молярную теплоемкость и плотность газообразной смеси. Окончательное выражение для критической температуры t* имеет вид
- •55.Особенности кинетики р-ий в р-рах. Влияние природы р-рителя на скорость процесса, ур-ие Бренстеда.
- •56. Влияние ионной силы и давления на кинетику реакций в растворе.
- •Если в бимолекулярной реакции реагенты а и в представляют собой ионы с зарядами zА и zВ, и заряд ак z* в линейном приближении равен сумме
- •Тогда из выражения (5.7) можно выразить влияние ионой силы j на константу скорости реакции в растворе:
- •Или для водных растворов
- •58.Общий и специфич. Кислотно-основ.Катализ.
- •59.Катализ комплексами переходных металлов и ферментатив.Катализ.
- •63.Температурная зависимость наблюдаемой скорости реакции
- •70.Топохимические реакции.
11. Диаграмма состояния р-ров ,образующих азеотропы.2й з-н Коновалова.
Жидкости, имеющие максимум или минимум на кривых давление -состав соответствуют минимумы и максимумы на кривых Ткип – состав, причем в точках минимума и максимума составы жидкой и паровой фазы равны.
Отклонение свойств реальных растворов от св-в идеальных могут быть настолько большими, что кривые давления насыщенного пара или Ткип в зависимости от состава раствора могут иметь максимум или минимум давлении температуры кипения.
*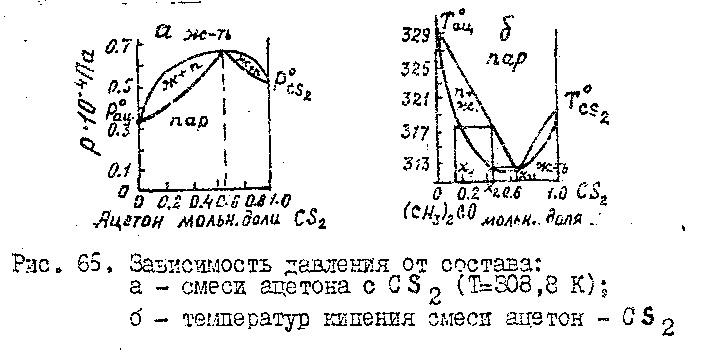 еще
два графика, но наоборот, т.е минимум
давление, максимум температура
еще
два графика, но наоборот, т.е минимум
давление, максимум температура
Максимум на кривых давление – состав появляется у р-ров жидкостей, полиэдры кот. однородного состава более прочны, чем полиэдры разнородного состава, и наоборот. В точках максимума или минимума давлений или Ткип составы жидкой и паровой фаз равны (х=у). Смеси такого состава называются азеатропами или неразделяющимися.
При разгонке азеатропов с максимумом Ткип в отгоне будут содержаться жид-ть А или В, а в остатке –азеатроп, содержащий оба компонента (А+В). При разгонке жидкостей с минимумом Ткип с парами будет уходить из разгоночного аппарата азеатроп, а в остатке будет содержаться один из компонентов.
Методы разделения гетероазеатропных смесей:
1) Химический метод разделения азеатропа (вода+спирт ,с добавлением водоотнимающего агента, например СаО )
2) Разгонка в колоннах под вакуумом.
3) Разделение азеатропа путем перегонки с добавлением третьего компонента.(К раствору вода+спирт добавляем бензол .образуется двухслойная жидкость,кипящая при 64 ºС и давлении 1 атм. Остаток после отгонки бензольного раствора явл. абс. спирт).
Термодинамическое док-во II з-на Кановалова
Жидкости, имеющие максимум или минимум на кривых давление -состав соответствуют минимумы и максимумы на кривых Ткип – состав, причем в точкх минимума и максимума составы жидкой и паровой фазы равны.
Док-во: исходя из уравнения Гиббса - Дюгема, которое для бинарной смеси жидкостей на небольшом удалении от экстремума можно записать в таком виде.
![]()
Подставляем в это выражение
Х1=1-Х2 :
![]()
Выделяем из dp1 :
![]()
Давление p1 и р2 по з-ну Дальтона можно связать с составом паровой фазы:
р1=(1-у2)Р и р2=у2Р
Подставляем в предыдущее уравнение:
![]()
Полное давление по з-ну Дальтона равно сумме парциальных давлений:
Р=р1+ р2
Дифференцируем dP=dp1 +dp2
![]()
Поделим на dx2
![]()
В точке экстремума
![]()
И кроме того первая производная
![]()
Откуда
![]()
![]()
Это равенство выполняется при условии, что у2=х2 ,что и требовалось доказать.
12.Диаграмма «давление – состав» и «температура – состав» Жидкости, ограниченно растворимых друг в друге.
Если система образована из 2х летучих ограниченно смешивающихся жидкостей, то при испарении такой двухфазной сис-мы пар будет содержать оба компонента и находиться в равновесии с каждой из жидких фаз.
Согласно правилу сосуществования фаз в гетерогенной сис-ме две фазы, находящиеся порознь в равновесии с третей фазой равновесны м/д собой.
Известно 2 типа систем, состоящих из ограниченно растворимых жидкостей. В системах первого типа общее давление пара над растворами любого состава больше давлений паров чистых жидкостей при той же температуре (Рº1<P> Pº2). Такая зависимость общего давления пара чистых компонентов и относительно малой взаимной растворимостью жидкостей (анилин-вода)
В системах второго типа общее давление пара над р-рами любого состава лежит между давлениями пара чистых жидкостей при той же температуре (Рº1<P< Pº2) Такая зависимость наблюдается в системах с резко отличающимися давлениями чистых жидкостей и относительно большой взаимной растворимостью жидкостей(никотин-вода)
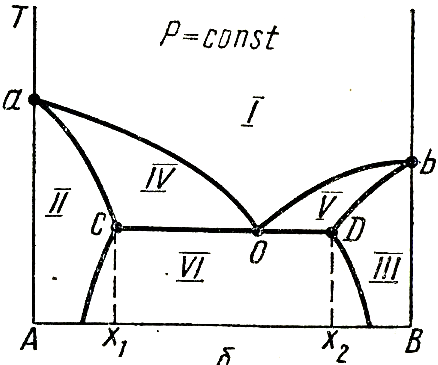
Каждая диаграмма кривыми пара и жидкости делиться на ряд облостей:
I - область пара;
II – область первого жидкого раствора ;
III – область второго жидкого раствора ;
IV – область пара и первого жидкого раствора
V – область пара и второго жидкого раствора
VI – область двух жидких растворов.
Пунктиром показана кривая расслоения, которая полностью проявляется при более высоких давлениях.
С-му с ограниченной взаимной растворимостью компоненов 1-го типа перегонкой можно разделить на гетероазеатроп и один из чистых компонентов. Гетероазеатроп –гетерогенная жидкая сис-ма (т.О на рис.),состоящая из 2х ограниченно смешивающихся жидкостей, общий состав кот. Совпадает с составом пара, равновесного с 2-мя жидкими фазами (т.С и D). В с-мах с гетероазеатропом пар имеет состав, промежуточный м/д составами сосуществующих с ним жидких фаз. Гетероазеатропная смесь имеет наинизшую Ткип по сравнению с Ткип смесей любого др. состава, ее нельзя разделить методом перегонки на чистые компоненты.
1) Жидкости образующие гетероазеатроп
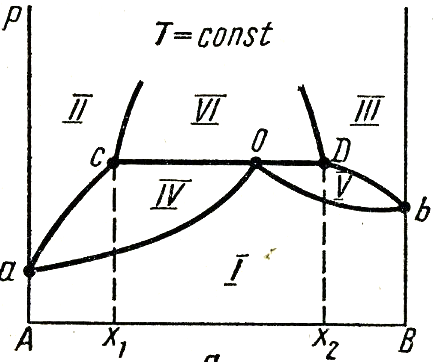
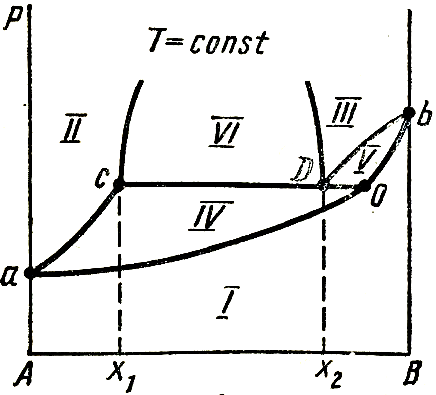
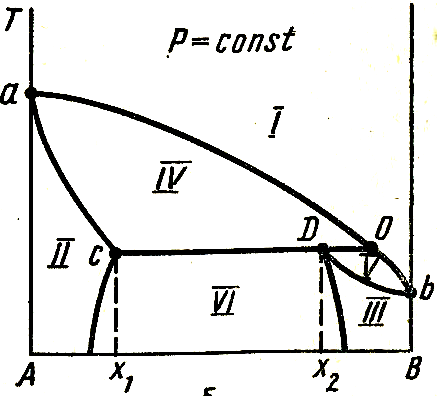
2) Не образующие гетероазеатроп
Если система образована из 2х летучих ограниченно смешивающихся жидкостей, то при испарении такой двухфазной сис-мы пар будет содержать оба компонента и находиться в равновесии с каждой из жидких фаз.
Согласно правилу сосуществования фаз в гетерогенной сис-ме две фазы, находящиеся порознь в равновесиис третей фазой.равновесны м/д собой.
При этом химические потенциалы равны между собой, т.е одинаковые.
Если рассматривать пар как ид. газ, то
μi (пар)= μºi(пар)+ RT ln Pi
Поскольку μºi(пар)= const при заданной температуре, то парциальное давление пара Pi одного и того же компонента над каждой из равновесных жидких фаз одинаково. Так как общее давление пара над раствором равно сумме парциальных давлений компонентов, то над обоими жидкими слоями при равновесии общее давление пара также одинаково
Известно 2 типа систем, состоящих из ограниченно растворимых жидкостей. В системах первого типа общее давление пара над растворами любого состава больше давлений паров чистых жидкостей при той же температуре (Рº1<P> Pº2). Такая зависимость общего давления пара чистых компонентов и относительно малой взаимной растворимостью жидкостей (анилин-вода)
В системах второго типа общее давление пара над р-рами любого состава лежит между давлениями пара чистых жидкостей при той же температуре (Рº1<P< Pº2) Такая зависимость наблюдается в системах с резко отличающимися давлениями чистых жидкостей и относительно большой взаимной растворимостью жидкостей (никотин-вода).
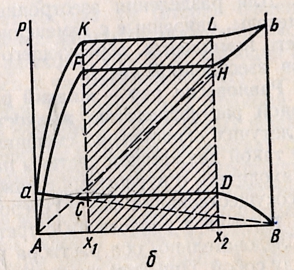
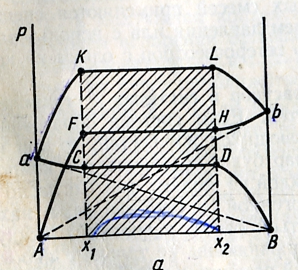
Характер изменения общего и парциальных давлений пара от состава раствора с ограниченной растворимостью жидкостей показана на рис. Заштрихованная область на диаграмме соответствует области расслоения при температуре Т. Пунктирная линия Аb и Ва показан характер изменения парциальных давлений компонентов в системе, подчиняющиеся з-ну Рауля. Кривые аCBD и AFHb изображают изменения парциальных давлений пара компонентов А и В, а кривая аKLb – изменение общего давления пара в зависимости от состава жидких фаз