
- •Водород. Вода. Водород.
- •Образцы решения задач
- •Образец тестового опроса. Водород. Вода.
- •Контрольные вопросы и упражнения
- •2.Пероксид водорода н2о2
- •Образцы решения задач
- •Образец тестового опроса.
- •Контрольные вопросы и упражнения
- •Элементы viia подгруппы Галогены
- •Образцы решения задач
- •Образец тестового опроса Галогены
- •Контрольные вопросы и упражнения
- •4.Элементы viа подгруппы
- •Физические свойства
- •Кислород
- •Подгруппа серы
- •Подгруппа селена: Se, Te, Po
- •Образцы решения задач
- •Образец тестового опроса
- •Контрольные вопросы и упражнения
- •5. Элементы va подгруппы
- •Азотистая кислота и нитриты
- •Мышьяк. Сурьма. Висмут.
- •Образцы решения задач и упражнений
- •Образцы тестового опроса азот
- •Контрольные вопросы и упражнения
- •6. Элементы iva подгруппы
- •Кремний.
- •Химические свойства
- •Способы получения кремния.
- •Германий
- •Образцы решений задач и упражнений
- •Образцы тестового опроса
- •Контрольные вопросы и упражнения
- •7. Элементы III-a подгруппы
- •Химические свойства бора
- •Алюминий.
- •Галлий, индий, таллий
- •Образцы решения задач и упражнений
- •Образец тестового опроса
- •Контрольные вопросы и упражнения
- •8. Элементы iiа подгруппы
- •Физические свойства
- •Образцы решения задач
- •Образец тестового опроса. Элементы iiа подгруппы
- •Контрольные вопросы и упражнения
- •9. Элементы iа подгруппы
- •Физические свойства
- •Образцы решения задач
- •Образец тестового опроса Элементы iа подгруппы
- •Контрольные вопросы и упражнения
- •Комплексные соединения Двойные соли и комплексные соединения.
- •Строение комплексных соединений. Теория Вернера.
- •I. Электролитами II. Неэлектролитами
- •Устойчивость комплексных соединений
- •Способы разрушения комплексных соединений
- •Номенклатура комплексных соединений.
- •Комплекс - анион.
- •Комплекс - катион и анион.
- •Соединения без внешней сферы.
- •Классификация комплексных соединений.
- •Метод валентных связей.
- •Теория кристаллического поля
- •Порядок убывания силы поля лигандов (комплекс - октаэдр)
- •Низко - и высокоспиновые комплексы.
- •Характеристика ионов в октаэдрическом поле
- •Образцы решения эадач.
- •Образец тестового опроса Комплексные соединения
- •Контрольные вопросы и упражнения
- •11. Элементы ib подгруппы
- •Физические свойства
- •Образцы решения задач
- •Образец тестового опроса
- •Контрольные вопросы и упражнения
- •12. Элементы iib подгруппы
- •Физические свойства
- •Растворение сульфидов
- •Применение Zn, Cd, Hg в микроэлектронике.
- •Образцы решения задач
- •Образец тестового опроса
- •Контрольные вопросы и упражнения
- •Элементы ivb подгруппы
- •Применение Ti, Zr, Hf
- •Образцы решения задач
- •Образец тестового опроса
- •Контрольные вопросы и упражнения
- •14. Элементы vb подгруппы
- •Физические свойства
- •Образцы решения задач
- •Образец тестового опроса
- •Контрольные вопросы и упражнения
- •15. Элементы vib подгруппы
- •Физические свойства
- •Образцы решения задач и упражнений
- •Образец тестового опроса
- •Контрольные вопросы и упражнения
- •16. Элементы viiв подгруппы
- •Физические свойства
- •Образцы решения задач
- •Образец тестового опроса
- •Контрольные вопросы и упражнения
- •Элементы viiib подгруппы
- •Физические свойства
- •Получение металлов
- •Химические свойства
- •Образцы решения задач
- •Образец тестового опроса
- •Контрольные вопросы и упражнения
- •Платиновые металлы
- •Физические свойства
- •Образцы решения задач и упражнений
- •Образец тестового опроса Платиновые металлы
- •Контрольные вопросы и упражнения
- •3. Элементы viia подгруппы Галогены
- •4.Элементы viа подгруппы
- •5.Элементы vа подгруппы
- •4. Элементы III-a подгруппы
- •Элементы ivв подгруппы
- •Элементы vb подгруппы
- •Элементы viв подгруппы
- •Константы диссоциации воды и некоторых слабых кислот и оснований в водных растворах при 18 c
- •Области перехода некоторых индикаторов
- •Степень гидролиза солей (в 0,1 м растворах при 25c)
- •Произведения растворимости труднорастворимых в воде веществ при 25c
- •Стандартные электродные потенциалы некоторых окислительно-восстановительных систем
- •Ряд напряжений металлов
- •Константы нестойкости некоторых комплексных ионов
- •Растворимость некоторых солей и оснований в воде
- •Содержание
Элементы viia подгруппы Галогены
Фтор, хлор, бром,
йод, астат составляют VIIА
подгруппу, их атомы имеют электронную
конфигурацию внешнего уровня ns2p5.
Астат получают искусственным путем,
радиоактивен, период полураспада
![]() =
8,3 часа, поэтому он изучен недостаточно.
Фтор проявляет единственную степень
окисления -1, остальные элементы могут
переходить в возбужденное состояние
(распаривать свои электроны в пустыеd-ячейки)
и проявлять дополнительно степени
окисления +1, +3, +5, +7.
=
8,3 часа, поэтому он изучен недостаточно.
Фтор проявляет единственную степень
окисления -1, остальные элементы могут
переходить в возбужденное состояние
(распаривать свои электроны в пустыеd-ячейки)
и проявлять дополнительно степени
окисления +1, +3, +5, +7.
При обычных условиях молекулы галогенов полиатомны и существуют в виде Г2 (в отличие от VIIB подгруппы).
Физические свойства. Фтор и хлор – газы, бром – красно-бурая жикость, йод – кристалличекое вещество – темно-фиолетовые кристаллы сослабым металлическим блеском, обладают способностью к возгонке. Все они обладают резким запахом и при вдыхании в большом количестве могут вызвать отравление. Растворимость галогенов в различных растворителях может быть хорошей иллюстрацией правила "подобное растворяется в подобном". Неполярные молекулы галогенов плохо растворяются в воде (фтор энергично разлагает воду2F2 + 2H2O = 4HF + O2↑) и хорошо - в неполярных органических растворителях (бензоле, толуоле, СС14 и др.). Способность хорошо растворяться в органических растворителях используют для извлечения галогенов из водных растворов методом экстракции.
Получение. В промышленности фтор получают путем электролиза расплавов смеси KF + HF; хлор – электролизом раствора хлоридов натрия или калия, бром и йод – из бромидов и иодидов, действуя на их растворы хлором.
В лаборатории их получают действием различных окислителей (KMnO4, K2Cr2O7, MnO2) на cоляную кислоту или бромиды и иодиды калия или натрия в кислой среде.
MnO2 + 4HCl = MnCl2 + Cl2 + 2H2O
2KMnO4 + 10KI + 8H2SO4 = 2MnSO4 + 5I2 + 6K2SO4 + 8H2O
Химическая активность галогенов от фтора к йоду уменьшается. Так, фтор реагирует практически со всеми элементами при комнатной температуре (даже с золотом и платиной), для хлора некоторые реакций идут лишь при нагревании, для брома температура реакции должна быть еще выше, йод даже при сильном нагревании реагирует с ограниченным количеством элементов.
Взаимодействие наиболее активных неметаллов фтора и хлора с простыми и сложными веществами может быть представлено схемой:

Галогены - хорошие окислители. Уменьшение окислительной способности от фтора к иоду видно из окислительных потенциалов:

Значением окислительных потенциалов и различным сродством к электрону объясняется вытеснение одних галогенов другими из их соединений:
|
F2 |
вытесняет |
Cl- |
Br- |
I- |
|
Cl2 |
вытесняет |
- |
Br- |
I- |
|
Br2 |
вытесняет |
- |
- |
I- |
|
I2 |
вытесняет |
- |
- |
- |
Например, Cl2 + 2KI = I2 + 2КСl, но I2 + КСl ≠ (реакция не идет).
Для быстрого связывания галогенов применяют тиосульфат натрия Na2S2O3:
Na2S2O3 + Cl2 + Н2О = Na2SO4 + S+ 2НСl,
с йодом образуется тетратионат натрия Na2S4O6:
2 Na2S2O3 + I2 = Na2S4O6 + 2NaI.
Галогеноводороды НГ хорошо растворяются в воде, водные растворы - сильные кислоты (кроме HF). Степень диссоциации α для 0,1 н. растворов составляет:
|
НГ |
HF |
HCl |
HBr |
HI |
|
α, % |
8 |
92,6 |
93,5 |
95 |
Плавиковая кислота относится к кислотам средней силы, так как в водном растворе ионы водорода частично связаны в ионы HF2-, Но HF- прекрасный комплексообразующий реагент, он входит в состав многих травителей для металлов и полупроводников, стекла, кремния и др. Ион F– не бывает восстановителем; ион Сl–` может быть восстановителем лишь в концентрированных растворах соляной кислоты (NaCl не является восстановителем), а от Br– к I– восстановительная способность возрастает; KI - один из наиболее распространенных восстановителей.
В кислородных соединениях все галогены, кроме фтора, проявляют положительные степени окисления. Так, хлор может проявлять положительные степени окисления +1, +3, +5, +7 (табл.).
Таблица
Кислородные соединения хлора
|
Степень окисления
|
Кислоты |
Соли |
|
+1 |
НСlO хлорноватистая |
Гипохлориты |
|
+3 |
НСlO2 хлористая |
Хлориты |
|
+5 |
НСlO3 хлорноватая |
Хлораты |
|
+7 |
НСlO4 хлорная |
Перхлораты |
Для брома и йода степень окисления +7 не характерна, для них наиболее устойчива степень окисления +5:
3I2+ 10HNO3 = 6НIO3 + 10NO+ 2Н2О
I2 + 5Сl2 + 6Н2О = 2НIO3 + 10НСl.
Многие соли кислородных кислот хлора обладают окислительно-восстановительной двойственностью, являются составными компонентами многих травителей полупроводников. Наибольшее применение находят гипохлориты и хлораты.
Гипохлориты получают взаимодействием хлора с холодными щелочами:
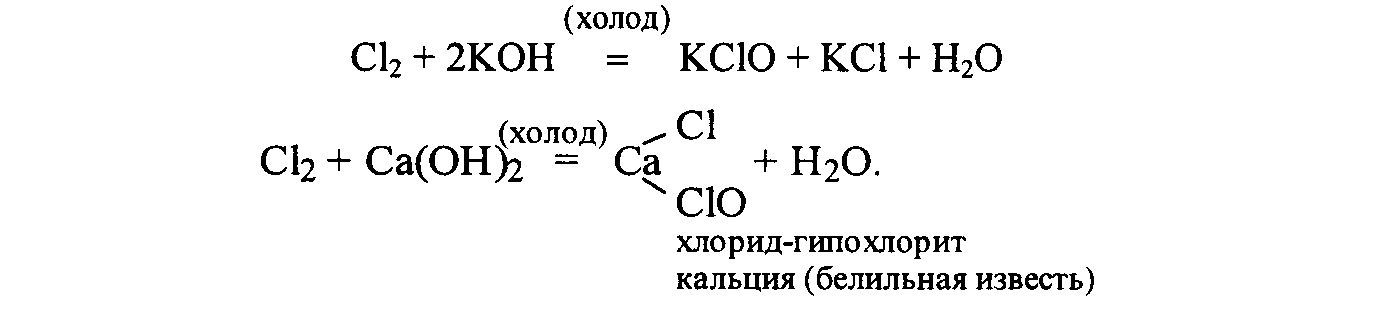
Двойственную природу гипохлоритов (Сl+1) можно представить схемой:

NaClO+ MnSO4+ Н2О = NaCl + МnО2 + Н2SO4
окислитель
3KClO + 4KMnO4+ 2Н2О = 3KClO3 + 4МnО2 + 4КОН
восстановитель
Хлораты получают пропусканием газообразного хлора в нагретые до 60 - 70ºС растворы щелочей:
ЗCl2 + 6KOH = КСIО3 + 5КСl + 3Н2О
Х лораты
менее сильные окислители, чем гипохлориты,
и тоже проявляют двойственность:
лораты
менее сильные окислители, чем гипохлориты,
и тоже проявляют двойственность:
Для них, как и для гипохлоритов, характерна реакция диспропорциони-рования:
4КСlО3 = 3КСlO4 + KCI
Реакция протекает при умеренном нагревании. При сильном нагревании образующийся перхлорат разлагается с выделением кислорода:
КСlO4
![]() КСl
+ 2O2
КСl
+ 2O2
Из кислородных соединений брома и йода наибольшее применение в качестве окислителей находят бромат и йодат калия. Они обладают меньшей окислительной способностью, чем хлораты:
КIО3+ 5КI+ 3Н2SO4 = 3I2+ 3К2SO4 + ЗН2О
Галогены и их соединения находят самое разнообразное применение.
Из фтора получают фторопроизводные углеводородов с уникальными свойствами, например, тефлон, обладающий исключительной стойкостью к различным химическим реагентам, фреоны - охлаждающие жидкости. Жидкий фтор используется как один из самых эффективных окислителей в ракетном топливе. Для этих же целей применяются перхлораты аммония и калия (NH4ClO4, КСlO4).
В микроэлектронике свободные галогены и их соединения находят широкое применение в качестве компонентов травителей полупроводников, в процессах фотолитографии (Сl2, Вг2, HF, НСl, HBr, HIO3, HClO, НСlO4 и др.).
Легколетучие соединения галогенов с неметаллами (PCl3, РСl5, ВСl3, SiCl4, GeCl4 и др.) используются в качестве диффузантов и промежуточных веществдля получения полупроводников простого и сложного составов заданного типа проводимости.
