
- •Федеральное агентство по рыболовству
- •Принципы молекулярной логики живого
- •Глава 1 химический состав организмов
- •Важнейшие классы органических соединений
- •Структура, свойства и биологические функции воды
- •Содержание основных катионов и анионов внутри клетки и во внеклеточных жидкостях организма человека (по а.Е. Строеву)
- •Вопросы для самоконтроля
- •Глава 2 белки
- •Протеиногенные аминокислоты
- •Классификация протеиногенных аминокислот
- •Химические свойства аминокислот
- •Сложные белки
- •Вопросы и задания для самоконтроля к главе 2 «белки»
- •Глава 3 нуклеиновые кислоты
- •Функции мононуклеотидов
- •Вопросы для самоконтроля к главе 3
- •Глава 4 Биосинтез белка
- •Вопросы для самоконтроля к главе 4 «Биосинтез белка»
- •Глава 5 Биологический катализ. Ферменты
- •Строение фермента
- •Классификация ферментов.
- •Свойства ферментов
- •Регуляция активности ферментов
- •Вопросы для самоконтроля к главе 5 «Биологический катализ. Ферменты»
- •Глава 6 витамины
- •Витамины, их коферментные формы и катализируемые реакции
- •Вопросы для самоконтроля к главе 6 «Витамины»
- •Глава 7 Углеводы Классификация углеводов, строение, свойства
- •Вопросы для самоконтроля к главе 7 «Углеводы»
- •Глава 8 Обмен веществ и энергии. Обмен углеводов
- •Обмен углеводов Переваривание и всасывание углеводов
- •Дихотомический путь распада глюкозы
- •Цикл Кребса (цтк)
- •Дыхательная цепь (электронтранспортная цепь)
- •Прямой путь окисления глюкозы (пентозофосфатный цикл).
- •Вопросы для самоконтроля к главе 8 «Обмен веществ и энергии. Обмен углеводов»
- •Глава 9 Липиды
- •Некоторые природные жирные кислоты
- •Вопросы для самоконтроля к главе 9 «Липиды»
- •Глава 10 обмен жиров Внешний обмен жиров
- •Метаболизм глицерина
- •Окисление жирных кислот
- •Синтез жиров
- •Вопросы для самоконтроля к главе 10 «Обмен жиров»
- •Глава 11 обмен белков
- •Распад белков в тканях
- •Вопросы для самоконтроля к главе 11 «Обмен белков»
- •Глава 12 гормоны. Взаимосвязь процессов обмена веществ
- •Пептидные гормоны
- •Гормоны – производные аминокислот (прочие гормоны)
- •Фитогормоны
- •Регуляция секреции гормонов
- •Взаимосвязь процессов обмена веществ
- •Вопросы для самоконтроля к главе 12 «Гормоны. Взаимосвязь процессов обмена веществ»
- •Практикум
- •Техника безопасности работы в биохимической лаборатории
- •Рабочий журнал
- •Лабораторная работа № 1 цветные реакции на белки
- •Вопросы к лабораторной работе «Цветные реакции на белки»
- •Лабораторная работа № 2 реакции осаждения белков
- •Вопросы к лабораторной работе «Реакции осаждения белков»
- •Лабораторная работа № 3 нуклеопротеиды
- •Дифениламиновая проба (реакция Дише)
- •Проба Троммера
- •Реакция Толленса
- •Вопросы к лабораторной работе «Качественные реакции на отдельные ферменты»
- •Лабораторная работа № 5 количественное определение аскорбиновой кислоты
- •Вопросы к лабораторной работе «Количественное определение аскорбиновой кислоты»
- •Лабораторная работа № 6 Количественное определение углеводов
- •Содержание глюкозы в 0,1 мл вытяжки, в мг
- •Вопросы к лабораторной работе «Количественное определение углеводов»
- •Лабораторная работа №7 жировые константы Определение йодного числа жира
- •Определение кислотного числа жира
- •Вопросы к лабораторной работе «Жировые константы»
- •Рекомендуемая литература
Важнейшие классы органических соединений
|
Название, общая формула |
Функциональная группа, отличительный признак |
Пример |
|
Галогенпроизводные углеводородов |
|
|
|
Спирты R — ОН (R —алкильный радикал) |
|
|
|
Фенолы R — ОН (R — ароматический радикал) |
| |
|
Простые эфиры
|
|
|
|
Альдегиды |
|
|
|
Кетоны |
|
|
|
Карбоновые кислоты
|
|
|
|
Сложные эфиры
|
|
|
|
Нитросоединения
|
|
|
|
Амины
|
|
|
|
α - Аминокислоты |
|
|
Если все биологические вещества, функционирующие в клетке, расположить по сложности их строения, то получатся определенные уровни организации клетки.
Первый уровень занимают низкомолекулярные предшественники клеточных компонентов, к которым относятся вода, углекислый газ, молекулярные кислород и азот, неорганические ионы, ряд химических элементов. На втором уровне стоят промежуточные химические соединения, такие как аммиак, органические кислоты и их производные, карбамоилфосфат, рибоза и др. Из соединений первого и второго уровней в ходе жизнедеятельности клеток образуются биологические мономеры, которые являются строительным материалом для биополимеров, имеющих большую молекулярную массу и отличающихся огромным разнообразием. Промежуточное положение между биологическими мономерами и биополимерами занимают витамины и коферменты, которые по молекулярной массе ближе к мономерам, но не являются строительными блоками биополимеров. Биополимеры способны ковалентно соединяться друг с другом, образуя сложные макромолекулы: липопротеины, нуклеопротеины, гликопротеины, гликолипиды и т. д. Взаимодействием простых и сложных макромолекул создаются надмолекулярные структуры (мультиэнзимы). Следующий уровень организации клетки — клеточные органеллы: митохондрии, ядра, рибосомы, и др. Система органелл образует клетку.
Структура, свойства и биологические функции воды
Жизнь на планете Земля зародилась в водной среде. Ни один организм не может обходиться без воды. Несмотря на простоту химического состава и строения, вода является одним из удивительных соединений, обладает уникальными физико-химическими свойствами и биологическими функциями. Она удивительна своими самыми обычными свойствами Молекула воды нелинейна (Рис.1).

Рис.1 Строение молекулы воды
Атомы водорода и кислорода расположены в углах равнобедренного треугольника. Длина связи О – Н равна 0,0957 нм. Поскольку атомы водорода и кислорода имеют различную электроотрицательность, электронная плотность связи О – Н смещена к кислороду, а химические связи расположены под углом, отличным от 180о (104,5о), молекула воды полярна. Важной особенностью воды является способность ее молекул объединяться в структурные агрегаты за счет образования водородных связей. Образующиеся ассоциаты (рис. 2) состоят из нескольких молекул воды, поэтому формулу воды правильнее было бы записать как (Н20)n, где n = 2, 3, 4, 5.
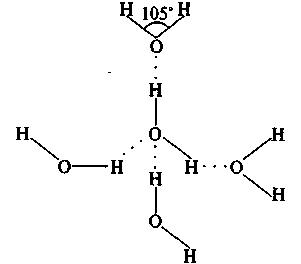
Рис. 2. Ассоциат молекул воды.
Водородные связи имеют исключительно важное значение при формировании структур биополимеров, надмолекулярных комплексов. Если бы между молекулами воды не было водородных связей, вода кипела бы при Т = - 80оС. Это означает, что в обычных условиях Земли вода находилась бы в газообразном состоянии.
Водородная связь — это взаимодействие атома водорода, соединенного с электроотрицательным атомом с другим электроотрицательным атомом, имеющее частично донорно-акцепторный, частично электростатический характер. По энергии водородная связь занимает промежуточное положение между ковалентной (200—400 кДж/моль) и ионной химическими связями и слабыми ван-дер-ваальсовыми взаимодействиями, находясь в пределах 12—30 кДж/моль.
Необычная структура воды обусловливает ее уникальные физико-химические свойства. Все биохимические процессы в организме протекают в водной среде. Вещества, находящиеся в водном растворе, имеют водную (гидратную) оболочку, которая образуется в результате взаимодействия полярных молекул воды с заряженными группами макромолекул или ионов. Чем больше такая оболочка, тем лучше растворимо вещество.
По отношению к воде молекулы или их части делят на гидрофильные (водорастворимые) и гидрофобные (водонерастворимые). Гидрофильными являются все органические и неорганические соединения, диссоциирующие на ионы, биологические мономеры и биополимеры, имеющие полярные группы. К гидрофобным следует отнести соединения, молекулы которых содержат неполярные группы или цепи (триацилглицерины, стероиды и др.). Молекулы некоторых соединений содержат как гидрофильные, так и гидрофобные группы; такие соединения называются амфифильными (от греч. amphy — двоякий). К ним относятся жирные кислоты, фосфолипиды и др.
Физико-химические свойства воды определяют ее биологические функции:
Вода является прекрасным растворителем.
Вода выполняет функцию регулятора теплового баланса организма, так как ее теплоемкость значительно превышает теплоемкость любого биологического вещества. Поэтому вода может долго сохранять тепло при изменении температуры окружающей среды и переносить его на расстояние.
Вода способствует сохранению внутриклеточного давления и формы клеток (тургор).
•В определенных биохимических процессах вода выступает в качестве субстрата.
Содержание воды зависит от возраста животного, от его физиологического состояния, степени упитанности и т.д. Чем моложе животное, тем выше содержание воды. У новорожденных вода составляет 75% от массы тела, у детей от 1 года до 10 лет — 60—65%, а у людей старше 50 лет — 50—55%. При повышении жирности количество воды в их тканях уменьшается. Внутри клеток содержится 2/3 общего количества воды, внеклеточная вода составляет 1/3. Необходимое содержание воды в организме человека поддерживается за счет поступления ее извне (примерно 2 л в сутки); около 0,3 л в сутки образуется в процессе распада веществ внутри организма. Нарушение водного баланса в клетках организма приводит к тяжелым последствиям вплоть до гибели клеток. Функции клеток зависят от общего количества внутриклеточной и внеклеточной воды, от водного окружения макромолекул и субклеточных структур. Потеря воды в количестве 1 % от массы тела человека приводит к появлению чувства жажды, а при потере организмом 20 % воды в клетках происходят необратимые изменения, приводящие к гибели. Суточная потребность взрослого мужчины в воде составляет 35 г на 1 кг массы тела, а грудного ребенка – в 3-4 раза больше. Запаса воды хватает только на четыре дня, поэтому человек не может прожить без воды больше пяти-семи дней.
Неорганические ионы, их свойства и биологические функции
Неорганические или, иначе, минеральные вещества находятся в клетках в виде ионов. Основными катионами в клетках и внеклеточных жидкостях организма человека являются: Na+, K+, Са2+, Mg2+, Zn2+, Fe2+. Среди анионов преобладают РО32-, CI-, SО42-, НСО3-.
Концентрации основных неорганических катионов и анионов в межклеточной жидкости и в плазме крови почти не отличаются (табл. 2). Как видно из таблицы 2, Na+ является основным катионом во внеклеточной среде, а К+ — внутри клеток. Из анионов вне клетки преобладает С1-, а внутри клетки — Р032-.
Живой организм подчиняется физико-химическому закону электронейтральности: суммы положительных зарядов катионов и отрицательных зарядов анионов должны быть равны. Для соблюдения этого закона в организме не хватает некоторого количества неорганических анионов. Недостаток отрицательных зарядов компенсируют анионы органических кислот и белков.
Таблица 2
