
- •Оглавление.
- •Раздел I введение в технологию
- •Глава 1
- •Основные понятия и определения
- •§ 1.1. Предмет и содержание курса технологии отраслей промышленности
- •§ 1.2. Связь технологии с экономикой
- •§ 1.3. Понятие о технологических процессах: принципы их классификации
- •§ 1.4. Материальные и энергетические (тепловые) балансы
- •§ 1.5. Понятие о себестоимости и качестве промышленной продукции
- •§ 1.6. Общие положения по технике безопасности и охране труда на промышленных предприятиях
- •Глава 2 сырье, вода и энергия в промышленности § 2.1. Сырье в промышленности
- •Минеральное сырье
- •Растительное и животное сырье
- •Обогащение сырья
- •Комплексное использование минерально-сырьевых ресурсов
- •§ 2.2. Вода в промышленности
- •Промышленная водоподготовка
- •Промышленные сточные воды и их очистка
- •§ 2.3. Роль энергии в технологических процессах
- •Рациональное использование энергии
- •Глава 3 научно-техническая революция и научно-технический прогресс в промышленности § 3.1. Сущность, значение и основные направления научно-технического прогресса
- •§ 3.2. Нтр и технология
- •§ 3.3. Химизация народного хозяйства - важное направление нтп
- •§ 3.4. Нтп в области промышленных материалов
- •§ 3.5. Нтп в области орудий труда. Механизация, автоматизация и роботизация производства
- •§ 3.6. Применение вычислительной техники и асу в технологии
- •§ 3.7. Экологические проблемы нтп
- •Раздел II
- •§ 4.2. Основные закономерности, определения и классификация химических процессов
- •§ 4.3. Понятие о скорости и равновесии химических процессов
- •§ 4.4. Выход продукции в химико-технологических процессах
- •§ 4.5. Общие принципы интенсификации химико-технологических процессов
- •Перспективы развития и совершенствования химико-технологических процессов
- •Глава 5. Высокотемпературные процессы § 5.1. Сущность и значение высокотемпературных процессов
- •Влияние температуры на процессы, идущие в кинетической области
- •Влияние температуры на скорость процессов в диффузионной области
- •Условия, ограничивающие применение высоких температур
- •Типовое оборудование
- •§ 5.2. Тенденции совершенствования высокотемпературных процессов
- •§ 5.3. Высокотемпературные процессы в металлургии
- •Высокотемпературные процессы черных металлов в производстве
- •§ 5.4. Высокотемпературные процессы в производстве строительных материалов
- •§ 5.5. Высокотемпературная переработка топлива
- •Термические процессы переработки нефти и нефтяных фракций
- •§ 5.6. Высокотемпературные процессы в химической промышленности
- •Глава 6 электрохимические процессы § 6.1. Значение и сущность электрохимических процессов
- •Основные закономерности электрохимических процессов
- •§ 6.2. Электролиз водных растворов Электрохимическое производство хлора и едкого натра (каустической соды)
- •Электролиз воды
- •Электрохимическое производство продуктов окисления
- •§ 6.3. Гидроэлектрометаллургия
- •§ 6.4. Электролиз расплавленных сред
- •Свойства расплавленных электролитов
- •Глава 7 каталитические процессы § 7.1. Роль каталитических процессов, основные закономерности и определения
- •§ 7.2. Применение каталитических процессов в промышленности
- •§ 7.3. Производство аммиака
- •§ 7.4. Каталитические процессы нефтепереработки
- •Глава 8 процессы, идущие под повышенным или пониженным давлением § 8.1. Роль давления в технологии
- •§ 8.2. Давление как фактор интенсификации газообразных процессов
- •§ 8.3. Роль давления в жидкофазных и твердофазных процессах
- •Глава 9 биохимические процессы § 9.1. Основные понятия и определения
- •§ 9.2. Применение биотехнологических процессов в промышленности
- •Глава 10 фотохимические процессы
- •Глава 11 радиационно-химические процессы
- •Глава 12 плазмохимические процессы § 12.1. Общие понятия и определения
- •§ 12.2. Виды плазмохимических процессов
- •Глава 13 общие сведения о физических процессах химической технологии § 13.1. Значение физических процессов и их классификация
- •§ 13.2. Виды физических процессов Физико-механические процессы
- •Массообменные процессы
- •Раздел III
- •§ 14.2. Кислоты, щелочи Неорганические кислоты
- •§ 14.3. Минеральные удобрения
- •§ 14.4. Полимеры Общие сведения о полимерах, их строении, свойствах и способах получения
- •Пластмассы, их свойства, значение и применение в народном хозяйстве
- •Химические волокна и их применение в народном хозяйстве
- •Каучуки и резина
- •§ 14.5. Нефтепродукты
- •Глава 15 строительные материалы § 15.1. Общие сведения
- •§ 15.2. Основные виды строительных материалов Природные (естественные) материалы, применяемые в строительстве
- •Керамические материалы
- •Огнеупорные материалы
- •Минеральные вяжущие
- •Бетон, железобетон и строительные растворы
- •Силикатные (автоклавные) материалы
- •Асбестоцементные материалы
- •Стекло и изделия на его основе
- •Теплоизоляционные материалы
- •Глава 16 металлы и сплавы § 16.1. Общие сведения
- •§ 16.2. Методы определения качества металла (сплава)
- •§ 16.3. Термическая и химико-термическая обработка
- •§ 16.4. Черные металлы и сплавы
- •Материалы со специальными свойствами (стали, сплавы)
- •Магнитные материалы
- •Инструментальные материалы
- •§ 16.5. Цветные металлы и их сплавы
- •§ 16.6. Коррозия металлов
- •Классификация коррозионных процессов
- •Электрохимическая коррозия металлов
- •§ 16.7. Защита металлов от коррозии Защита металлов от химической коррозии
- •Экономия на 1 т листа
- •Защита металлов от электрохимической коррозии
- •Технико-экономические показатели и выбор методов защиты
- •Раздел IV
- •Типы производств
- •Типизация технологических процессов
- •Технологичность конструкций изделий
- •Качество изделий
- •Понятие о точности обработки
- •Основные методы и средства контроля качества изделий
- •Шероховатость поверхности
- •Выбор заготовок
- •§ 17.2. Экономическая оценка технологического процесса
- •Глава 18
- •Литье в песчано-глинистые формы
- •Специальные способы литья
- •§ 18.2. Основы технологии производства заготовок методами пластической деформации
- •Формообразование заготовок, изделий из пластмасс и резины методами пластической деформации
- •Формообразование деталей методами порошковой металлургии
- •§ 18.3. Изготовление неразъемных соединений Понятие о неразъемных соединениях. Виды неразъемных соединений
- •Сущность процессов сварки материалов и их классификация
- •Сварка плавлением
- •Огневая резка материалов
- •Сварка давлением
- •Контроль качества сварных соединений
- •Клеевая технология
- •§ 18.4. Обработка конструкционных материалов резанием
- •Обработка на станках-автоматах и полуавтоматах
- •Чистовая обработка наружных поверхностей тел вращения
- •Обработка внутренних поверхностей тел вращения.
- •Обработка плоских поверхностей
- •Обработка фасонных поверхностей
- •Методы изготовления деталей зубчатых зацеплений
- •Обработка резанием неметаллических материалов
- •Обработка заготовок на агрегатных станках
- •§ 18.5. Электрофизические методы обработки
- •Применение ультразвука в промышленности
- •Плазменная обработка материалов
- •Лазерная обработка
- •Глава 19 основные технологические процессы электроники и микроэлектроники § 19.1. Технология изготовления интегральных микросхем
- •Фотолитография в микроэлектронике
- •Нанесение тонких пленок в вакууме
- •Осаждение из газовой фазы
- •§ 19.2. Технология изготовления печатных плат
- •Технологические процессы изготовления пп
- •Субстрактивные методы изготовления печатных плат
- •Технология изготовления многослойных печатных плат
- •Аддитивные методы изготовления печатных плат
- •Печатные платы с многопроводным монтажом
- •Глава 20 технология сборочных процессов § 20.1. Понятие о технологическом процессе сборки и его организационных формах
- •§ 20.2. Контроль и испытание готовых изделий
- •Глава 21 основы технологии строительного производства § 21.1. Роль капитального строительства в развитии народного хозяйства ссср
- •§ 21.2. Строительные работы
- •§ 21.3. Основные направления совершенствования строительства
- •Глава 22 оптимизация технологических процессов § 22.1. Общая постановка задач оптимизации технологических процессов
- •§ 22.2. Методы оптимизации технологических процессов
- •Регрессионный и корреляционный методы анализа при оптимизации технологических процессов
- •Методы планирования эксперимента для оптимизации технологических процессов
§ 4.3. Понятие о скорости и равновесии химических процессов
Любой процесс химических превращений складывается из трех последовательных взаимосвязанных актов: подвода реагирующих компонентов в зону реакции, химической реакции и отвода полученных продуктов из зоны реакции.
Суммарная скорость такого процесса определяется скоростями перечисленных элементарных стадий, которые также протекают с различной скоростью. Общая скорость процесса в итоге определяется скоростью его наиболее медленной стадии. Поэтому на практике для ускорения любых производственных и технологических процессов в первую очередь интенсифицируют скорость наиболее медленной стадии.
Подвод реагентов в зону реакции и отвод продуктов из зоны реакции может совершаться физическим транспортированием вещества за счет беспорядочного движения самих молекул (молекулярной диффузии), естественного или принудительного переноса (конвекции) либо интенсивного перемешивания (турбулентной диффузии).
В многофазных системах твердые компоненты подводятся в реакционную зону растворением в жидкости, плавлением, испарением или возгонкой с конденсацией паров, а газообразные — растворением в жидкости либо улавливанием твердым поглотителем. При этом переход из одной фазы в другую по схеме
![]()
во многих случаях оказывается наиболее медленным и потому лимитирующим скорость технологического процесса.
Химические реакции составляют основу химико-технологических процессов и отличаются чрезвычайным разнообразием фазового достояния реагентов, условиями проведения и механизмом протекания. Обычно химическое превращение вещества может состоять из ряда последовательных или параллельных химических реакций, в результате которых образуются как основные и побочные продукты, имеющие народнохозяйственное значение, так и отходы производства. Побочные продукты и отходы могут получаться как в результате основных, так и побочных реакций вследствие неизбежного присутствия примесей в сырье.
При оценке скорости взаимодействия веществ учитываются не все реакции, а лишь те, которые имеют определяющее влияние на качество и количество получаемых основных продуктов.
Многие химические превращения протекают как в прямом, так и в обратном направлении, что усложняет оценку скорости процесса. По этому признаку различают обратимые и необратимые реакции. Необратимые реакции в отличие от обратимых протекают лишь в одном направлении.
Все обратимые реакции стремятся к равновесию, при котором скорости прямого и обратного процессов уравниваются. При достижении равновесия суммарная скорость процесса оказывается равной нулю, а соотношение между компонентами — неизменным. Лишь изменением внешних условий, например температуры, давления, концентрации компонентов, можно нарушить равновесие и направить протекание процесса в том или ином направлении до наступления нового равновесного состояния.
Качественное влияние условий процесса на равновесие химических реакций определяется принципом Ле-Шателье, согласно которому в системе, выведенной внешним воздействием из состояния равновесия, самопроизвольно происходят изменения, стремящиеся вернуть систему к равновесию.
Использование принципа Ле-Шателье позволяет качественно оценивать целесообразность применения того или иного внешнего воздействия для направленного смещения равновесия в сторону, обеспечивающую максимальный выход конечного продукта.
Так, например, если обратимая реакция типа
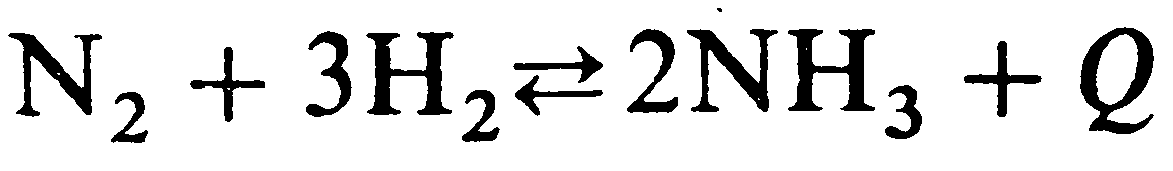
протекает с выделением теплоты, то в соответствии с принципом Ле-Шателье для сдвига равновесия вправо необходимо: понижать температуру (отводить теплоту), так как процесс экзотермический; повышать давление, так как гомогенный процесс в газовой фазе протекает с уменьшением объема (из 1 + 3 = 4 молекул азотоводородной смеси получается 2 молекулы аммиака); уменьшать концентрацию аммиака в системе (непрерывно отводить аммиак из зоны реакции); повышать концентрацию исходных веществ (азота и водорода), поскольку повышение концентрации одного из них увеличивает степень превращения другого.
Таким образом, для сдвига равновесия реакции вправо обычно в качестве практических приемов используют подвод или отвод теплоты, изменение давления, увеличение концентрации реагирующих компонентов, вывод конечных продуктов из зоны реакции. Эти и другие факторы значительно изменяют скорость химических превращений.
Скорость обратимых реакций зависит от степени приближения взаимодействующих систем к равновесному состоянию.
Количественно подвижное равновесие между исходными веществами и продуктами реакции для всех химических процессов определяется константой равновесия Кр , при которой скорости прямой и обратной реакции равны.
Обычно константы равновесия определяются опытным путем либо приводятся в специальных справочниках. Это позволяет по известному значению величины Кр рассчитывать состав продуктов реакции при условии равновесия, а также равновесную степень превращения при различных условиях процесса. Таким образом, зная константу равновесия, можно определить предельную полноту протекания процесса, достигаемую в условиях равновесия реакции.
Как известно, скорость химико-технологического процесса представляет собой результирующую скорость прямой, обратной и побочных реакций, а для гетерогенных процессов также скорость транспортирования (диффузии) исходных веществ в зону реакций и продуктов из зоны.
Результирующая скорость химико-технологического процесса определяется не только скоростью химической реакции, но и скоростью подвода и отвода веществ из реакционной зоны. При существующих методах физической транспортировки вещества скорость его подвода или отвода из зоны реакции определяется в конечном итоге скоростью диффузии компонентов.
Скорость диффузии зависит от свойства вещества, температуры, давления и скорости потока. Так, пособность молекул газа диффундировать в неподвижную жидкость в 104 — 105 раз меньше способности газа диффундировать в другой газ. Таким образом, молекулярная диффузия является весьма медленным процессом, особенно в неподвижных жидкостях. В движущихся или перемешиваемых жидкостях, газах, газожидкостных или других взаимодействующих потоках скорость диффузии прямо пропорциональна скорости движущегося потока. Поэтому турбулизация потоков является важнейшим приемом интенсификации процесса переноса компонентов из фазы в фазу через границу раздела в системах Г - Ж, Ж - Ж, Ж - Г, Г - Т.
Влияние остальных факторов (температуры и особенно давления) на скорость диффузии по сравнению со скоростью химической реакции проявляется в значительно меньшей степени.
Поскольку результирующая скорость химико-технологического процесса определяется скоростью его наиболее медленной стадии, то для интенсификации и ускорения процесса в целом необходимо знать, какой области процесса соответствует наиболее медленная стадия. По этому признаку в химико-технологическом процессе различают диффузионную, кинетическую и переходную области.
Так, если скорость химической реакции больше скорости диффузии, то скорость всего процесса будет определяться скоростью более медленной диффузии. В этом случае процесс протекает в диффузионной области и для ускорения его следует использовать факторы, интенсифицирующие диффузию.
Если скорость химической реакции значительно меньше, чем скорость диффузии, то скорость всего процесса определяется скоростью химической реакции. В этом случае процесс протекает в кинетической области и для его интенсификации следует принять меры для ускорения реакции.
Если же скорости диффузии и реакции соизмеримы, то процесс идет в переходной области и для его ускорения необходимо воздействовать и на диффузию, и на химическую реакцию.
Установление области, в которой протекает процесс, производится анализом экспериментальных данных по влиянию температуры и скорости потока на скорость превращения.
Если при низких температурах суммарная скорость реакции не зависит от скорости подачи реагентов, но значительно возрастает с увеличением температуры, то это значит, что при низких температурах процесс протекает в кинетической области. Если в некотором интервале температур суммарная скорость реакции заметно увеличивается с ростом температуры и на ее рост оказывает влияние повышение скорости подвода реагентов, то это значит, что при данных температурных условиях процесс протекает в переходной области. В случае, когда результирующая скорость химической реакции практически не зависит от температуры, но значительно возрастает с увеличением скорости подачи реагентов, процесс протекает в диффузионной области.
