
- •Часть I
- •Часть I
- •Предисловие
- •4. Содержание обучения.
- •Часть I модуль 1 «общие закономерности метаболизма. Метаболизм углеводов, липидов, белков и его регуляция» введение
- •Литература
- •Тема для самостоятельного изучения биохимия как наука. Этапы развития биохимии. Методы биохимических исследований
- •Найти материал для освоения этих вопросов можно в одном из следующих источников: Обязательная литература.
- •1.Губський ю.Г. Біологічна хімія. - Київ-Тернопіль: Укрмедкнига, 2000. - с. 9-11.
- •Приложение 1 Граф логической структуры
- •Содержательный модуль 1. «роль ферментов и витаминов в обмене веществ»
- •Найти материал для освоения этих вопросов можно в одном из следующих источников: Обязательная литература
- •1.Губський ю.Г. Біологічна хімія. - Київ-Тернопіль: Укрмедкнига, 2000. - с. 18-36.
- •Инструкция к практическому занятию Работа №1 «Количественное определение белка биуретовым методом»
- •Работа №2 «Доказательства белковой природы ферментов»
- •Приложение 1 Граф логической структуры
- •Тема 1.2. Исследование структуры и физико-химических свойств ферментов
- •Основные теоретические вопросы, позволяющие выполнить целевые виды деятельности:
- •Найти материал для освоения этих вопросов можно в одном из следующих источников: Обязательная литература
- •Инструкция к практическому занятию
- •Граф логической структуры
- •Тема 1.3. Определение активности ферментов. Исследование кинетики ферментативного катализа и влияния активаторов и ингибиторов
- •Содержание обучения
- •Основные теоретические вопросы, позволяющие выполнить целевые виды деятельности:
- •Найти материал для освоения этих вопросов можно в одном из следующих источников: Обязательная литература
- •1.Губський ю.Г. Біологічна хімія.- Київ-Тернопіль:Укрмедкнига, 2000.-с.88-89, 98-112
- •Инструкция к практическому занятию: “ Определение активности ферментов, исследование кинетики ферментативного катализа и влияния активаторов и ингибиторов“
- •Граф логической структуры
- •Тема 1.4. Исследование роли кофакторов и коферментных форм витаминов в каталитической активности ферментов
- •Задание 4. Образуемая при работе в мышцах молочная кислота в покое частично превращается в пировиноградную, отдавая водород, в реакции называемой: а. Дегидратацией в. Дегидрированием
- •Основные теоретические вопросы, позволяющие выполнить целевые виды деятельности:
- •Найти материал для освоения этих вопросов можно в одном из следующих источников: Обязательная литература
- •1.Губський ю.Г. Біологічна хімія. - Київ-Тернопіль.: Укрмедкнига, 2000.- с. 89-92, 209-210, 399-404.
- •Работа і. Изучение коферментной функции витамина в1
- •Работа іі «Изучение коферментной функции витамина рр»
- •Граф логической структуры
- •Тема 1.5. Исследование участия витаминов и коферментных форм витаминов в различных биохимических процессах
- •Конкретные цели: Цели исходного уровня:
- •D. Пиримидин
- •Содержание обучения
- •Найти материал для освоения этих вопросов можно в одном из следующих источников: Обязательная литература
- •С. Фолиевая кислота
- •Работа III. Количественное определение витамина р в чае
- •Граф логической структуры
- •Задания для самопроверки и самокоррекции содержательного модуля «роль ферментов и витаминов в обмене веществ»
- •Содержательный модуль 2 «обмен веществ и энергии»
- •Тема 1.6. Исследование окислительного фосфорилирования и синтеза атф, ингибиторы и разобщители окислительного фосфорилирования
- •Конкретные цели: Исходный уровень:
- •Задание 1. Соединения а, в, с, д и е имеют соответственно редокс-потенциалы, равные
- •Основные теоретические вопросы, позволяющие выполнить целевые виды деятельности:
- •Найти материал для освоения этих вопросов можно в одном из следующих источников: Обязательная литература
- •1. Губський ю.Г. Біологічна хімія. - Київ-Тернопіль.: Укрмедкнига, 2000. - с. 122-142
- •Инструкция к практическому занятию «Иследование окислительного фосфорилирования и синтеза атф. Ингибиторы и разобщители окислительного фосфорилирования».
- •2. Раствор яблочной кислоты (малат) 0,5 0,5
- •3. Раствор 2,6-дхфи 0,5 0,5
- •4. Суспензия митохондрий - 0,5
- •2. Сукцинат 0,5 0,5
- •3. Раствор 2,6-дхфи 0,5 0,5
- •4. Суспензия митохондрий - 0,5
- •Г р а ф логической структуры
- •Организация дыхательной цепи в митохондриях
- •Цитохромы
- •Тема 1.7. Обмен веществ и энергии. Исследование функционирования цикла трикарбоновых кислот
- •Задание 1. В результате окислительно-восстановительной реакции окраска 2,6-дхфи обесцветилась. Что произошло с этим индикатором в окислительно – восстановительной реакции ?
- •Основные теоретические вопросы, позволяющие выполнить целевые виды деятельности:
- •D. Пиридоксина
- •Инструкция к практическому занятию
- •Граф логической структуры
- •Задания для самопроверки и самокоррекции содержательного модуля «обмен веществ и энергии»
- •Содержательный модуль 3. «метаболизм углеводов и его регуляция»
- •Тема 1.8. Исследование особенностей переваривания углеводов. Биосинтез и катаболизм гликогена. Превращение других моносахаридов в глюкозу
- •Основные теоретические вопросы, позволяющие выполнить целевые виды деятельности:
- •Найти материал для освоения этих вопросов можно в одном из следующих источников: Обязательная литература
- •1. Губський ю.Г. Біологічна хімія.- Київ-Тернопіль.:Укрмедкнига, 2000.-с. 57-65, 163-165, 176-179, 395-396.
- •Инструкция к практическому занятию “Определение активности -амилазы слюны»
- •Граф логической структуры
- •Тема 1.9. Анаэробное окисление углеводов. Гликолиз. Биосинтез глюкозы – глюконеогенез
- •Содержание обучения
- •Основные теоретические вопросы, позволяющие выполнить целевые виды деятельности:
- •Задача 2 Эритроциты не имеют митохондрий. Какой конечный продукт окисления глюко- зы в них образуется?
- •Инструкция к практическому занятию Работа I. Моделирование реакций гликогенолиза
- •Граф логической структуры
- •Тема 1.10. Исследование аэробного окисления глюкозы. Пентозофосфатный путь преобразования глюкозы
- •Основные теоретические вопросы, позволяющие выполнить целевые виды деятельности:
- •Найти материал для освоения этих вопросов можно в одном из следующих источников: Обязательная литература
- •1.Губський ю.Г. Біологічна хімія.- Київ-Тернопіль.:Укрмедкнига, 2000.-с.144-145, 153, 156-162, 154-155.
- •Инструкция к практическому занятию «Количественное определение пировиноградной кислоты в моче»
- •Граф логической структуры
- •Задания для самопроверки и самокоррекции содержательного модуля «метаболизм углеводов и его регуляция»
- •Содержательный модуль 4 «метаболизм липидов и его регуляция»
- •Тема 1.11. Структура и функции клеточных мембран
- •Основные теоретические вопросы, позволяющие выполнить целевые виды деятельности:
- •Найти материал для освоения этих вопросов можно в одном из следующих источников: Обязательная литература
- •1.Губський ю.Г. Біологічна хімія.- Київ-Тернопіль.:Укрмедкнига, 2000.-с. 78-85.
- •Граф логической структуры
- •Мембраны – главный структурный элемент клетки
- •Липосома
- •Приложение 3 пол (перекисное окисление липидов)
- •Защита биомембран от пол
- •Неферметативные антиоксиданты
- •Тема 1.12. Исследование особенностей переваривания липидов. Возможные нарушения переваривания липидов и транспорта в крови экзогенных липидов
- •Конкретные цели : Цели исходного уровня:
- •Основные теоретические вопросы, позволяющие выполнить целевые виды деятельности:
- •1. Губський ю.І. Біологічна хімія. – Київ – Тернопіль: Укрмедкнига, 2000. – с. 190-194, 224-228, 389, 396-398
- •Инструкция к практическому занятию «Кинетика действия панкреатической липазы»
- •Граф логической структуры
- •Тема 1.13. Исследование обмена жирных кислот и кетоновых тел. Бета-окисление жирных кислот.Биосинтез и трансформация холестерола
- •Основные теоретические вопросы, позволяющие выполнить целевые виды деятельности:
- •Найти материал для освоения этих вопросов можно в одном из следующих источников. Обязательная литература
- •Инструкция к практическому занятию: «Количественное определение холестерина в крови и кетоновых тел в моче»
- •Граф логической структуры
- •Тема 1.14. Исследование биосинтеза жирных кислот, триацилглицеридов и фосфолипидов. Нарушения липидного обмена: ожирение, жировая инфильтрация печени
- •Основные теоретические вопросы, позволяющие выполнить целевые виды деятельности:
- •Найти материал для освоения этих вопросов можно в одном из следующих источников. Обязательная литература.
- •Граф логической структуры задания для самопроверки и самокоррекции содержательного модуля «метаболизм липидов и его регуляция»
- •Тема 1.15. Исследование химического состава желудочного сока. Особенности переваривания белков
- •Конкретные цели: Цели исходного уровня:
- •Содержание обучения
- •Основные теоретические вопросы, позволяющие выполнить целевые виды деятельности:
- •Обязательная литература
- •Дополнительная литература
- •Задания для самостоятельной аудиторной работы
- •3. 1. Решите задачу
- •Этапы переваривания белков
- •Инструкция к практическому занятию «Химический состав желудочного сока»
- •Обнаружение молочной кислоты в желудочном соке по реакции Уффельмана
- •Ход работы
- •Граф логической структуры
- •Тема 1.16. Исследование преобразований аминокислот (дезаминирование, трансаминирование, декарбоксилирование)
- •Основные теоретические вопросы, позволяющие выполнить целевые виды деятельности:
- •Найти материал для освоения этих вопросов можно в одном из следующих источников. Обязательная литература
- •Дополнительная литература
- •Задания для самостоятельной аудиторной работы
- •Іі. Завершите схемы приводимых ниже метаболических преобразований
- •Инструкция к практическому занятию: «Определение активности АлАт и АсАт»
- •Определение активности АсАт
- •Определение активности АлАт
- •Граф логической структуры
- •Тема 1.17. Исследование процессов детоксикации аммиака и биосинтеза мочевины
- •Основные теоретические вопросы, позволяющие выполнить целевые виды деятельности:
- •Найти материал для освоения этих вопросов можно в одном из следующих источников: Обязательная литература
- •Дополнительная литература
- •Задания для самостоятельной аудиторной работы
- •Задание № 1
- •Задание № 2
- •Задание № 3
- •Задание № 4
- •Инструкция к практическому занятию “Количественное определение мочевины в крови”
- •Ход работы
- •Граф логической структуры
- •Тема 1.18. Специализированные пути обмена отдельных аминокислот. Биосинтез креатина. Нарушения обмена аминокислот
- •Основные теоретические вопросы, позволяющие восполнить целевые виды деятельности
- •Инструкция к лабораторной работе
- •Граф логической структуры
- •Граф логической структуры
Инструкция к практическому занятию: “ Определение активности ферментов, исследование кинетики ферментативного катализа и влияния активаторов и ингибиторов“
Принцип работы:
Активаторы действуют на пространственную конфигурацию белковых молекул, помогая формированию активного центра и, тем самым, активируют фермент. В отличие от коферментов они не принимают непосредственного участия в реакции.
Активаторы некоторых ферментов : для амилазы слюны - хлорид натрия (NaCL), для пепсина- ионы водорода хлористоводородной кислоты, для липазы- желчные кислоты, для аденозинтрифосфатазы - ионы магния и марганца.
Ингибиторы также влияют на активный центр фермента, но при этом снижают каталитическую активность фермента. Нередко они являются конечными продуктами реакций какого либо биохимического процесса. Действие ингибиторов специфично для определенных ферментов или групп ферментов.
Материальное обеспечение: пробирки, 1% раствор крахмала, амилаза, 1% раствор NaCL, 1% раствор CuSO 4 , реактив Люголя
Работа 1.
Ход работы:
Разводят 1 мл слюны в 10 раз. В три пробирки наливают по 1 мл предварительно разведенной слюны. По предложенной ниже схеме ставят опыт:
№№ Фермент Субстрат Исследуемое Количество
(амилаза), слюна

1. 1мл 1мл дист.вода 0,5мл
2. 1мл 1мл 1% NaCL 0,5мл
3 . 1мл 1мл
1% CuSO
4 0,5мл
. 1мл 1мл
1% CuSO
4 0,5мл
-
Все пробирки инкубируют 10 минут при температуре 25 градусов.
-
Определяют влияние исследуемых соединений на каталитическую функцию амилазы. Для этого проводят качественную реакцию на крахмал (субстрат). Во все пробирки добавляют по 1 капле реактива Люголя, содержащего йод, перемешивают, наблюдают окраску и определяют, в какой пробирке действует активатор или ингибитор. Целесообразно в каждую пробирку добавить до 2 мл дист. воды и перемешать. Окраска будет более наглядной.
ВЫВОДЫ:
Работа 2. Выполните лабораторную работу по индивидуальному заданию, полученному у преподавателя.
ВЫВОДЫ:
Подпись преподавателя:
Приложение 1
Граф логической структуры
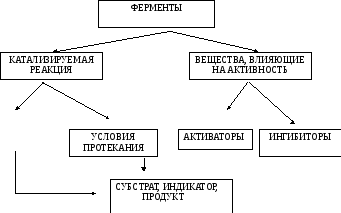
СУБСТРАТ
Тема 1.4. Исследование роли кофакторов и коферментных форм витаминов в каталитической активности ферментов
Актуальность темы
Значение витаминов для нормальной жизнедеятельности организма не вызывает сомнений. Витамины являются составным компонентом сложных ферментов, образуя небелковую часть фермента – кофермент. Без кофермента сложный фермент не может функционировать, т.к кофермент, как правило, непосредственно контактирует с субстратом и является переносчиком электронов, атомов или групп атомов (аминогрупп, метильных групп и др.), тем самым участвуя в катализе определенных типов метаболических реакций. Знание коферментной функции витаминов необходимо для последующего изучения метаболизма органов и тканей в курсе биохимии, а также при изучении фармакологии, клинических и гигиенических дисциплин.Теперь ознакомьтесь с целями занятия.
Общая цель
Уметь обосновать биологическую функцию витаминов как структурных компонентов ферментов для использования на последующих кафедрах при объяснении нарушений метаболизма и их клинических проявлений при недостатке (избытке) витаминов в организме, а также для понимания принципов применения антивитаминов в лечебной практике.
. Конкретные цели: Цели исходного уровня:
Уметь:
|
1.Интерпретировать структуру витаминов и их коферментных форм. |
1.Интерпретировать структуру мононуклеотидов, сложных эфиров (каф. медицинской и фармацевтической химии). |
|
2.Анализировать причины нарушения синтеза коферментов. |
2. Интерпретировать принцип метода определения пирувата в биологических жидкостях (каф. медицинской и фармацевтической химии). |
|
3.Анализировать роль витаминов в обменных реакциях. |
3. Интерпретировать принцип метода определения лактата в биологических жидкостях(кафедра медицинской и фармацевтической химии). |
|
4.Интерпретировать метаболические нару- шения при отсутствии витаминов.
|
|
|
5.Интерпретировать конкурентное действие антивитаминов.
|
|
Для проверки исходного уровня Вам предлагается выполнить ряд заданий.
Задания для самопроверки и самокоррекции исходного уровня.
Задание 1. Студенту предложили синтезировать сложный эфир, предоставив следующие вещества: спирт, кислоту, альдегид, амин. Что он использовал, выполнив задание?
А. Кислоту и амин
В. Только кислоту
С. Только спирт
D. Спирт и альдегид
Е. Спирт и кислоту
Задание 2. Лабораторный анализ после гидролиза вещества выявил в гидролизате аденин, рибозу и фосфорную кислоту. Какой структуры исходное вещество?
А. Пептид
В. Нуклеозид
С. Мононуклеотид
D. Пентозофосфат
Е. Гликозаминогликан
Задание 3. Для определение пирувата его нужно превратить в гидразон по реакции:
СН3 NH-NH 2


 I I
NO2
I I
NO2
 С=О + O2
N
С=О + O2
N
I → гидразон
СООН
Какими функциональными группами реагируют вещества?
А. -СООН группой пирувата и -NO2 группой гидразина
В. О
II
-С- группой пирувата и -NO2 группой гидразина
C. -СООН группой пирувата и -NН2 группой гидразина
D. О группой пирувата и -NН2 группой гидразина
II
-C-


Е. О группой пирувата и - группой гидразина
II
-С-
