
- •Технологія спирту лабораторний практикум
- •6.051701 «Харчові технології та інженерія»
- •Технологія спирту
- •Дослідження органолептичних і фізичних властивостей зерна
- •Основні теоретичні положення
- •Визначання органолептичних показників (гост 10967-90)
- •Проведення визначання
- •Визначання фізичних показників
- •Визначання явно вираженої смітної та зернової домішок
- •Визначання вмісту зіпсованих і ушкоджених зерен
- •Визначання вмісту шкідливої домішки
- •Визначання вмісту особливо враховуваних домішок Визначання вмісту сажкових зерен
- •Визначання вмісту гальки
- •Визначання вмісту металомагнітної домішки
- •Кінцеве обробляння результатів визначання загального вмісту смітної й зернової домішок
- •Визначання вмісту дрібних зерен і крупності
- •Визначання натури зерна (гост 10840-64)
- •Визначання маси 1000 зерен (гост 10842-89)
- •Проведення визначання
- •Визначання зараженості зерна шкідниками (гост 13586.4-83)
- •Проведення визначання
- •Органолептичні та фізичні показники досліджуваного зерна
- •Контрольні питання
- •Основні теоретичні положення
- •Визначання вологи зерна
- •Основний стандартний метод визначання вологи зерна
- •Хід визначання
- •Визначання умовної крохмалистості
- •Підготовка до визначання
- •Виділення наважок для аналізу
- •Проведення аналізу із застосуванням 1,124% - ного розчину соляної кислоти
- •Проведення аналізу із застосуванням розчину хлористого кальцію.
- •Обробляння результатів
- •Визначання загальної лужності або кислотності в мелясі
- •Хід визначання
- •Визначання активної кислотності.
- •Підготовка до визначання Приготування реактиву Герлеса
- •Проведення визначання
- •Обробляння результатів
- •Визначання масової частки суми цукрів, що зброджуються
- •Визначання інверсійної поляризації
- •Підготовка до визначання Приготування розчину соляної кислоти
- •Проведення визначання
- •Обробляння результатів
- •Визначання масової частки редукувальних речовин класичним методом Мюллера
- •Проведення визначання
- •Обробляння результатів
- •Визначання масової частки редукувальних речовин методом Оффнера (метод, який використовується в разі виникнення розбіжностей в оцінці якості)
- •Підготовка до визначання Приготування початкового розчину
- •Проведення визначання
- •Обробляння результатів
- •Визначання доброякісності меляси
- •Хімічні показники зерна
- •Контрольні питання
- •Тема: Визначання вмісту засвоюваного азоту та азоту амінокислот у мелясі. Визначання калію, натрію і кальцію в мелясі.
- •Теоретична основи
- •Визначання вмісту загального азоту в мелясі.
- •Визначання амінного азоту «мідним методом».
- •Визначання калію кобальтонітритним методом у мелясі.
- •Комплексометричний метод визначання кальцію.
- •Визначання кольору меляси.
- •Оцінка якості меляси.
- •Контрольні питання.
- •Тема: Оцінка якості ферментних препаратів, що застосовуються у спиртовому виробництві
- •Теоретична частина
- •Визначання амілолітичної активності (ас)
- •Підготовка до визначання Приготування розчину крохмалю з масовою часткою 1 % (субстрата)
- •Приготування фосфатного буферного розчину з рН 5,6 і рН 6,0
- •Приготування основного розчину йоду
- •Приготування робочого розчину йоду
- •Приготування основного розчину очищених ферментних препаратів
- •Приготування робочого розчину очищених ферментних препаратів
- •Приготування основного розчину із повітряно-сухої культури гриба
- •Приготування робочого розчину із повітряно-сухої культури гриба
- •Приготування основного розчину із культурної рідини бактеріального походження
- •Приготування робочого розчину із культуральної рідини
- •Проведення визначання
- •Обробляння результатів
- •Визначання глюкоамілазної активності
- •Підготовка до визначання
- •Приготування основного і робочого розчинів очищених ферментних препаратів готують за п.1
- •Приготування основного і робочого розчинів із повітряно-сухої культури гриба
- •Приготування робочого розчину із культуральної рідини
- •Побудова градуювального графіка
- •Проведення визначання
- •Обробляння результатів
- •Визначання глюкоамілазної активності (ГлС) глюкооксидазним методом (арбітражний метод)
- •Приготування до визначання
- •Обробляння результатів
- •Визначання оцукрюючої активності (ос)
- •Підготовка до визначання
- •Визначання оцукрюючої активності в очищених препаратах і в культурі гриба, отриманого із Asp. Awamori
- •Визначання оцукрюючої активності в очищених препаратах і в культурі із Bac. Subtilis
- •Обробляння результатів
- •Контрольні питання:
- •Теоретична частина.
- •Визначання якісних показників затору. Відбір середньої проби
- •Визначання концентрації сухих речовин
- •Визначання повноти оцукрювання затору
- •Визначання загальної й активної кислотності
- •Приготування розчину індикатора метилового червоного.
- •Проведення визначання
- •Оцінка якості затору
- •Визначання вмісту незброджених цукрі. Теоретична частина
- •Метод Бертрана
- •Приготування реактивів
- •Хід визначання
- •Приклади розрахунків:
- •Визначання вмісту незброджених розчинних цукрів в зерновій зрілій бражці. Теоретична основа
- •Хід визначання
- •Визначання загального вмісту незброджених розчинних вуглеводів і нерозчинного крохмалю
- •Хід визначання
- •Оцінка якості
- •Контрольні питання
- •Теоретична частина.
- •Порядок виконання роботи. Визначання кольоровості, загального вигляду смаку та запаху.
- •Визначання вологості
- •Визначання кислотності.
- •Визначання підйомної сили.
- •Оцінка якості
- •Приклад
- •Визначання об'ємної частки спирту етилового
- •Підготовка до визначання
- •Проведення визначання
- •Обробляння результатів
- •Контроль якості вимірювань
- •Визначання проби на чистоту
- •Проведення визначання
- •Визначання проби на фурфурол
- •Підготовка проби спирту до визначання
- •Проведення визначання
- •Обробляння результатів
- •Визначання окислюваності спирту
- •Проведення визначання
- •Контроль якості вимірювань
- •Визначання масової концентрації альдегідів
- •Визначання масової концентрації альдегідів з фуксиносірчистим реактивом 1 у спирті етиловому ректифікованому
- •Підготовка проби спирту до визначання
- •Проведення визначання
- •Обробляння результатів
- •Визначання масової концентрацїї альдегідів з фуксиносірчистим реактивом і у спирті етиловому — сирці
- •Контроль якості вимірювань
- •Визначання масової концентрації сивушного масла
- •Визначання масової концентрації сивушного масла з саліциловим альдегідом
- •Кількісне визначання масової концентрації сивушного масла в спирті
- •Проведення визначання
- •Обробляння результатів
- •Контроль якості вимірювань
- •Визначання масової концентрації сивушного масла (ізоамілового, ізобутилового і пропілового спиртів) з парадиметиламінобензальдегідом (п-дмаба)
- •Готування дослідних водно-спиртових розчинів
- •Готування розчину парадиметиламінобензальдегіду (п-дмаба) в сірчаній кислоті
- •Кількісне визначання масової концентрації сивушного масла в спирті етиловому ректифікованому
- •Обробляння результатів
- •Контроль якості вимірювань
- •Випробовування етилового спирту-сирцю на вміст сивушного масла
- •Визначання масової концентрації кислот
- •Проведення визначання
- •Обробляння результатів
- •Контроль якості вимірювань
- •Визначання масової концентрації органічних речовин, що омилюються Визначання масової концентрації органічних речовин методом омилювання
- •Проведення визначання
- •Обробляння результатів
- •Визначанні масової концентрації естерів у спирті етиловому-сирці проводять методом омилювання ,аналогічно попередньому досліду. Контроль якості вимірювань
- •Визначання масової концентрації естерів
- •Готування розчину солянокислого гідроксиламіну концентрацією 2 моль/дм3
- •Моль/дм3
- •Готування розчинів реакційної суміші
- •Проведення визначання
- •Обробляння результатів
- •Контроль якості вимірювань
- •Випробовування спирту етилового — сирцю
- •Обробляння результатів
- •Контроль якості вимірювань — за таблицею 12. Визначання об'ємної частки метилового спирту
- •Підготовка до визначання Готування водного розчину динатрієвої солі хромотропової кислоти з масовою часткою 2 %
- •Готування водного розчину перманганату калію
- •Обробляння результатів
- •Аналіз етилового спирту - сирцю на вміст метилового спирту проводять аналогічно попередньому досліду Контроль якості вимірювань
- •Визначання масової концентрації сухого залишку
- •Проведення визначання
- •Обробляння результатів
- •Контрольні питання
- •Тема: Органолептичний аналіз спирту етилового ректифікованого Мета роботи: в процесі дегустації визначити головні показники якості: смак, запах, прозорість. Основні теоретичні положення.
- •Колір, прозорість.
- •Сприйняття смаку
- •Сприйняття запаху
- •Умови і порядок проведення дегустації. Види і характер дегустації.
- •Приміщення для дегустації
- •Порядок і методи проведення дегустації
- •Система дегустаційних оцінок
- •Контрольні питання.
- •Література: Основна література:
- •Додаткова література:
- •З лабораторних робіт
Приклади розрахунків:
1.Гідроліз бражки проведено звичайним методом. Для Визначання взято 20 см3 гідролізату, що відповідає 10 см3 вихідної бражки. Витрати перманганату калію на титрування досліджуваного розчину 9,8 см3. Поправка на реактиви складає 0,2 см3 розчину перманганату калію. Дійсні витрати перманганату
калію – 9,8-0,2=9,8 см3.1 см3 розчину перманганату калію відповідає 10 мг міді, а 9,6 см3 його – 96 мг міді.
За таблицею 2 ця кількість міді відповідає 50,35 мг глюкози.
Вміст незброджуваного цукру (г глюкози в 100 см3 бражки) складе
50,35·100/10·1000=0,50,
Де 10 – кількість вихідної бражки, см3;
100 – коефіцієнт для перерахунку на 100 см3;
1000 - коефіцієнт для переводу мг в г.
2. Гідроліз проведено пришвидченим методом. Для Визначання взято 20 см3 гідролізату, що відповідає 4 см3 вихідної бражки. Витрати KMnO4 на титрування дослідного розчину 4,0 см3, правка на реактиви 0,2 см3. Дійсні витрати перманганату калію 4,0-0,2=3,8 см3, що відаповідає 38 мг міді.
За табл. 2 ця кількість міді відполвідає 18,95 мг глюкози.
Вміст незброджених цукрів (г глюкози в 100 см3 бражки) складе
18,95·100/4·1000=0,47.
Таблиця 2.Співвідношення між міддю і глюкозою (в мг) при визначенні
редукованих речовин по Бертрану.
|
Мідь |
Глюкоза |
Мідь |
Глюкоза |
Мідь |
Глюкоза |
|
2 3 4 5 6 7
8 9 10 11 12 13
14 15 16 17 18 19
20 21 22 23 24 25
26 27 28 29 30 31
32 33 34 35 36 37
38 39 40 41 42 43
|
0,98 1,37 1,82 2,27 2,94 3,43
3,92 4,41 4,90 5,40 5,92 6,37
6,86 7,35 7,84 8,33 8,92 9,31
9,80 10,30 10,80 11,31 11,84 12,35
12,85 13,35 13,85 14,37 14,90 15,40
15,90 16,40 16,90 17,40 17,90 18,42
18,95 19,45 19,95 20,47 21,00 21,53 |
44 45 46 47 48 49
50 51 52 53 54 55
56 57 58 59 60 61
62 63 64 65 66 67
68 69 70 71 72 73
74 75 76 77 78 79
80 81 82 83 84 85 |
22,05 22,58 23,10 23,63 24,16 24,70
25,21 25,74 26,26 26,79 27,30 27,84
28,37 28,90 29,42 29,95 30,50 31,05
31,58 32,11 32,67 33,21 33,74 34,25
34,83 35,39 35,94 36,47 37,00 37,55
38,10 38,63 39,17 39,72 40,28 40,83
41,39 41,94 42,50 43,05 43,51 44,18
|
86 87 88 89 90 91
92 93 94 95 96 97
98 99 100 101 102 103
104 105 106 107 108 109
110 111 112 113 114 115
116 117 118 119 120 121
122 123 124 125 126 127 |
44,80 45,33 45,89 46,44 47,00 47,55
48,11 48,67 49,22 49,78 50,35 50,94
51,50 52,07 52,65 53,23 53,82 54,39
54,94 55,53 56,11 56,67 57,23 57,8/2
58,39 58,94 59,53 60,12 60,71 61,29
61,88 62,47 63,06 63,65 64,23 64,82
65,41 66,00 66,59 67,18 67,76 68,35 |
Визначання вмісту незброджених розчинних цукрів в зерновій зрілій бражці. Теоретична основа
Вміст розчинних незброджених вуглеводів (крохмалю, декстринів, мальтози, глюкози) в зерновій бражці визначають фото калориметричним антроновим методом. Цей метод дає змогу визначити вміст в бражці зброджуваних вуглеводів, які мали збродити, але не збродили через неповне оцукрення і бродіння – так званих незброджуваних вуглеводів в бражці. Користуючись калориметричним антроновим методом, можна провести пряме визначання незброджуваних вуглеводів в бражці. Антрон дає забарвлення зі всіма вуглеводами, в тому числі і з пентозанами.
Антрон – тверда кристалічна речовина, товарна назва 10-дигідро-9-кетоантроцена. Реакцію цукрів з антроном проводять при нагріванні в сильно кислому середовищі. При цьому від молекули цукру відщеплюються три молекули води і із пентоз утворюється фурфурол:

Гексози в цих умовах перетворюються в оксиметилфурфурол:
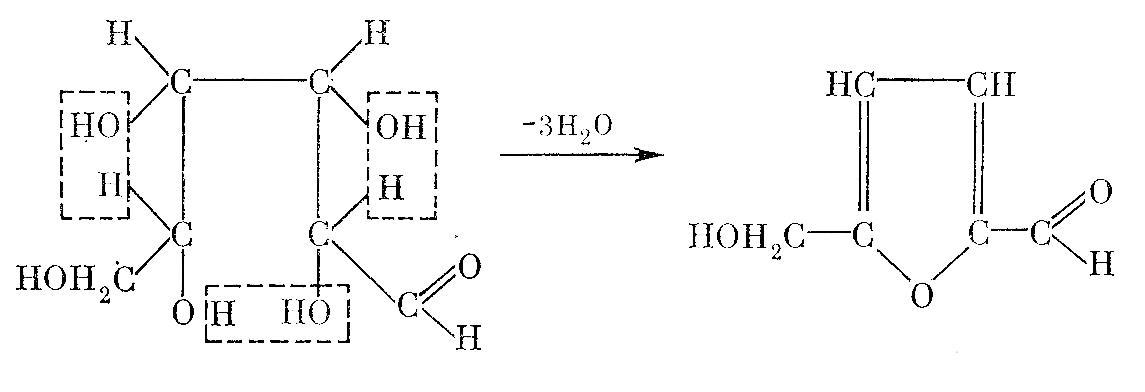
Складні сахариди в умовах досліду попередньо гідролізуються до моносахаридів.
Фурфурол і оксиметилфурфурол, вступаючи в реакцію з антроном, утворюють забарвлені сполуки: похідне фурфуролу з антроном має жовтий колір, а оксиметилфурфуролу-блакитно-зелений колір. Тому максимуми світлопоглинання у них знаходяться в різних областях спектру: у похідних пентоз з довжиною хвилі 413 нм, а гексоз – 610 нм. Різниця в максимумах світлопоглинання дає можливість визначити один цукор в присутності іншого.
Залежність оптичної густини від концентрації виражається рівнянням:
с=Д·l:х,
де с – концентрація розчину, моль/дм3;
Д – оптична густина розчину;
l – товщина шару розчину, що поглинає світло, см;
х – молярний коефіцієнт поглинання, що характеризує поглинаючу здатність досліджуваної речовини при довжині хвилі максимального поглинання.
Реактиви, посуд.
-Колби К-2-200-2, 2-250-2 згідно з ГОСТ 1770;
-Пробірки місткістю 20 см3 і 50 см3 з пришліфованими корками згідно з чинними нормативними документами;
-Піпетки 1-1-2-0,5, 1-2-2-5 і 1-2-2-10 згідно з ГОСТ 29227;
-Склянки з пришліфованими корками місткістю 100 см3;
-Колориметр фотоелектричний лабораторний (фотоелектроколориметр) типу -КФК згідно з чинними нормативними документами;
-Розчин сульфату цинку ZnSO4·7H2O з масовою часткою 30% ;
-Розчин гексаціаноферату (ІІ) калію – К4[Fe(CN)6]·6H2O з масовою часткою 15%;
Розчин антрону – 0,9175 г х.ч. антрону вводять в мірну колбу на 250 см3, додають 100-150 см3 сірчаної кислоти з відносною густиною 1,830 і перемішують до повного розчинення антрону; потім об´єм рідини в колбі доводять сірчаною кислотою до мітки. Приготовлений розчин витримують при кімнатній температурі протягом 4 годин в темноті, після чого використовують для аналізу . Розчин антрону зберігають при температурі
4-6ºС в темному місці, його можна використовувати протягом 12-15 діб.
