- •Алициклические углеводороды
- •Моноциклические насыщенные углеводороды (циклопарафины, циклоалканы, полиметиленовые углеводороды)
- •Номенклатура циклопарафинов
- •Изомерия циклопарафинов
- •Соединения с четырех- и пятичленными кольцами
- •Соединения ряда циклогексана
- •Способы получения
- •Физические свойства
- •Химические свойства
- •Химические свойства соединений с трехчленными циклами
- •1.Реакции присоединения
- •Химические свойства циклобутана и его гомологов
- •2.Окисление
- •3.Реакции термического разложения
- •4.Реакции присоединения
- •Взаимные превращения циклов
- •Способы получения
- •Химические свойства
- •Отличительные реакции
- •2.Отличительные особенности химических свойств циклопентадиена.
- •Ароматические соединения
- •Основные признаки ароматичности
- •Ароматические соединения
- •1 Группа – ароматические соединения бензоидного строения (ароматические углеводороды)
- •Отличительные особенности химического поведения ароматических углеводородов
- •Гомологический ряд, изомерия и номенклатура ароматических углеводородов
- •Названия ароматических радикалов
- •Способы получения ароматических углеводородов
- •Химические превращения углеводородов в процессе ароматизации
- •Б. Синтетические способы получения ароматических углеводородов
- •Физические свойства ароматических углеводородов
- •Химические свойства
- •Механизм электрофильного замещения
- •I. Реакции электрофильного замещения в ароматическом ядре
- •Правила электрофильного замещения в ароматическом ядре
- •Нитрование гомологов бензола
- •Реакции присоединения (нетипичны)
- •Галоидпроизводные ароматических углеводородов Классификация, изомерия, номенклатура
- •Получение
- •Физические свойства галогенопроизводных ароматических углеводородов
- •Химические свойства
- •Физические свойства
- •Химические свойства
- •I тип реакций. Реакции, характерные для органических кислот.
- •II тип реакции. Восстановление сульфогруппы
- •III тип реакций. Реакции нуклеофильного замещения сульфогруппы
- •IV тип реакций. Реакции электрофильного замещения в ядре идут в соответствии с правилами замещения
- •Нитросоединения ароматического ряда
- •1.Нитросоединения с нитрогруппой в ядре
- •Физические свойства
- •Химические свойства
- •II. Реакции в ядре
- •II. Нитросоединения с группой no2 в боковой цепи
- •Способы получения
- •Химические свойства ароматических нитросоединений с группой no2 в боковой цепи
- •Ароматические амины Классификация
- •I. По положению аминогруппы относительно ароматического ядра.
- •II. По количеству радикалов, связанных с азотом
- •III. По количеству аминогрупп
- •Получение
- •Физические свойства
- •Химические свойства
- •II. Реакции замещения водорода в аминогруппе
- •IV. Окисление
- •V. Реакции замещения в ароматическом ядре
- •Механизм реакции галоидирования
- •VI. Реакции конденсации ароматических аминов с другими органическими и неорганическими соединениями
- •Диазо- и азосоединения
- •Ароматические диазосоединения
- •Способы получения
- •1. Реакция диазотирования - -получение солей диазония.
- •Таутомерия и физические свойства ароматических диазосоединений
- •Химические свойства солей диазония
- •I. Реакции с выделением азота
- •II. Реакции диазосоединений без выделения азота
- •Азокрасители
- •Связь строения с цветностью
- •Индикаторные свойства азокрасителей
- •Ароматические оксисоединения
- •Классификация
- •Способы получения
- •Физические свойства фенолов
- •Химически свойства фенолов
- •I. Реакции подвижного водорода в группе он
- •II. Реакции электрофильного замещения в ядре
- •III. Окислительно-восстановительные реакции
- •IV. Конденсация фенолов с другими органическими соединениями
- •Ароматические спирты
- •Способы получения
- •Физические свойства
- •Химические свойства
- •Ароматические альдегиды и кетоны
- •Способы получения
- •II. Частные способы получения альдегидов и кетонов
- •Физические свойства
- •Химические свойства
- •Отдельные представители альдегидов
- •Отдельные представители кетонов
- •Ароматические кислоты
- •Способы получения
- •Физические свойства
- •Химические свойства
- •Двухосновные ароматические кислоты
- •Другие поликарбоновые ароматические кислоты
- •Полициклические ароматические углеводороды и их производные
- •Ароматические углеводороды с изолированными ядрами
- •Способы получения
- •Физические свойства
- •Химические свойства
- •Наиболее важные группы многоядерных соединений. Группа дифенила
- •Группа трифеиилметана
- •Красители типа трифенилметана
- •Полициклические ароматические углеводороды с конденсированными ядрами
- •Получение
- •Физические свойства
- •Особенности химических свойств
- •Аминопроизводные нафталина
- •Гетероциклические соединения
- •Ароматические гетероциклические соединения
- •Ароматические моноциклические пятичленные гетероциклы
- •Номенклатура гетероциклических соединений
- •Способы получения
- •Физические свойства
- •Химические свойства
- •Пятичленные гетероциклы с несколькими гетероатомами
- •Получение
- •Отличительные особенности свойств
- •Бициклические соединения с пятичленными гетероциклами
- •Получение инденкумароновых смол
- •Химические свойства
- •Значение
- •Применение и значение пятичленных гетероциклических соединений
- •Шестичленные гетероциклы с одним гетероатомом
- •Получение
- •Реакционноспособность некоторых заместителей в пиридиновом кольце
- •Получение
- •Понятие об алкалоидах
III тип реакций. Реакции нуклеофильного замещения сульфогруппы
При нагревании до 200-3000с щелочные соли ароматических сульфокислот могут давать реакции замещения сульфогруппы на нуклеофильный реагент.
1) Образование фенолов с помощью реакции щелочного плавления Na-солей сульфокислот.
сплавление
С6H5-SO2ONa + NaOH Na2SO3 + C6H5OH
тв. тв.
натриевая соль БСК
2) Образование нитрилов сплавлением с цианидами
сплавление
С6H5SO3Na + NaCN C6H5CN
цианистый натрий -Na2SO3 бензонитрил
сульфит натрия
натриевая соль
БСК
3) Реакции с другими солями
C6H5SO3Na + NaSH C6H5SH тиофенол
-Na2SO3
кислый сульфид
натрия
C6H5SO3Na + NaNH2 C6H5NH2
-Na2SO3
амид натрия анилин
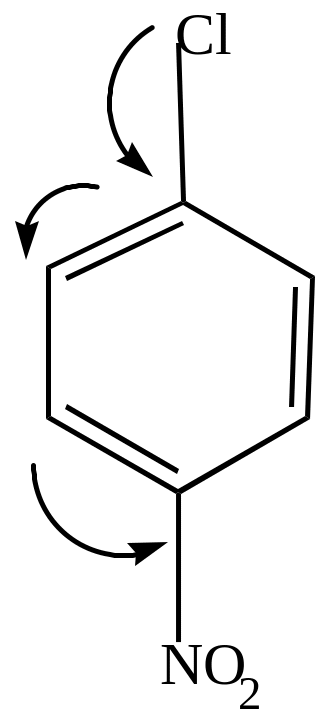
IV тип реакций. Реакции электрофильного замещения в ядре идут в соответствии с правилами замещения
Реакции галоидирования, нитрования и дальнейшее сульфирование ядра происходит в мета-положение к имеющейся группе SO3H, как к заместителю II рода, и труднее, чем в бензоле.

Нитросоединения ароматического ряда
Подразделяются на лекции 7.
1.Нитросоединения с нитрогруппой в ядре.
2.Нитросоединения с нитрогруппой в боковой цепи.
1.Нитросоединения с нитрогруппой в ядре
Способы получения
1.Нитрование ароматических углеводородов в условиях реакции электрофильного замещения (нитрующая смесь).
2.Замещение Cl в галоидарилах, когда Cl активирован нитрогруппой, расположенной в о- или п-положении, например, по механизму электрофильного замещения.
|
+ KNO2 KCl + |
|
п-хлорнитробензол |
азотистокислый калий |
п-динитробензол
|
3. Через соли диазония
|
+ KNO2 KCl + N2 + |
|
п-сульфофенилдиазоний |
азотистокислый калий |
п-нитробензолсульфокислота |
Физические свойства
Жидкие или твердые вещества с характерным миндальным запахом. Окрашены в желтый цвет, ядовиты, в воде не растворимы, d>1.
Полинитросоединения
|
|
Взрывчаты (тротил, тол)
Химические свойства
1.Реакции восстановления нитрогруппы.
Впервые были осуществлены в Казани в 1841 году Н.Н.Зининым (учитель А.М.Бутлерова). Нитросоединения приобрели важнейшее практическое значение ввиду того, что нитросоединения ароматического ряда – вещества легко доступные, а ароматические амины и другие вещества, получаемые при восстановлении нитросоединений, необходимы для производства красителей, лекарств, фотохимикатов, антиоксидантов, полимерных материалов.
Реакция восстановления нитросоединений ароматического ряда может привести к образованию различных продуктов. Решающую роль в направлении реакции играет среда.
1) Восстановление в нейтральной, слабокислой или слабощелочной среде (действие Fe+H2O, электрохимическое восстановление в нейтральной среде).
|
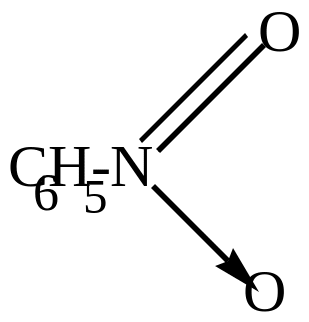
2H 2H + 2H H2O + C6H5-N=O C6H5-NH-OH C6H5NH2 + H2O нитрозобензол фенилгидроксиламин анилин |
|
|
Эту реакцию можно остановить на любой стадии. Фенилгидроксиламин может давать перегруппировку в п-аминофенол, если его поместить в кислую среду.
2) при проведении реакции восстановления в сильнокислой среде промежуточные соединения те же, но реакция идет так быстро, что остановить ее на промежуточных стадиях не удается. Конечный продукт – анилин. Восстановители – Zn, Fe+кислота, H2S.
3) Восстановление в щелочной среде.
Идет более сложно.
+2H
С6H5NO2 + 2H C6H5N=O C6H5NHOH
-H2O
нитробензол фенилгидроксиламин
С6H5-N=O + |
|
H2O + |
|
2H
|
|
|
|
Азоксибензол |
|
2H 2H H2O + C6H5-N=N-C6H5 C6H5-NH-NH-C6H5 2C6H5NH2 азобензол гидразобензол |
||||
Восстановление нитросоединений можно проводить и молекулярным водородом в присутствии катализаторов Cu, Pd, Ni.