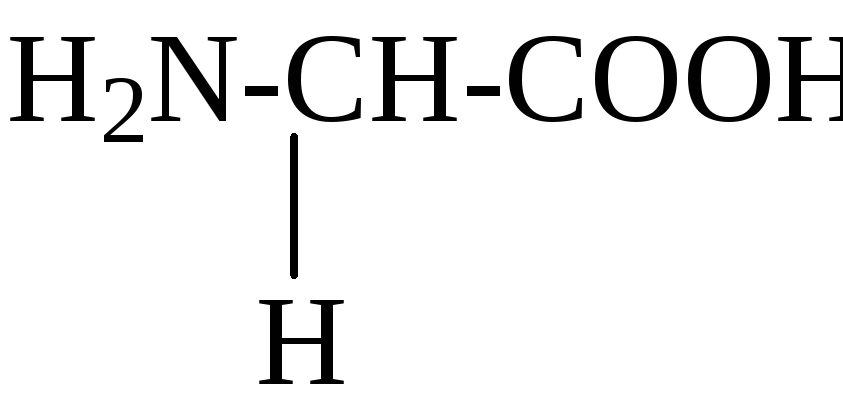- •Основы биологической химии предисловие
- •Введение Предмет и задачи биохимии
- •Основные признаки живой материи
- •Глава 1. Химический состав организмов
- •Глава 2. Структура и свойства белков
- •2.1. Роль и определение белков.
- •2.2. Функции белков в организме
- •2.3. Элементный состав белков. Содержание белков в органах и тканях
- •2.4. Аминокислотный состав белков
- •2.5. Кислотно-основные свойства аминокислот
- •2.6. Стереохимия аминокислот
- •2.7. Строение белков
- •2.8. Уровни структурной организации белков
- •Первичная структура
- •Вторичная структура белков
- •Третичная структура белков
- •Четвертичная структура белков
- •2.9. Физико-химические свойства белков
- •Кислотно-основные свойства белков
- •Растворимость белков
- •Денатурация и ренатурация
- •2.10. Классификация белков
- •2.11. Методы выделения и очистки белков
- •Очистка белков
- •Глава 3. Углеводы
- •3.1. Понятие об углеводах и их классификация
- •3.2. Моносахариды
- •Оптические свойства моносахаридов
- •Структура моносахаридов
- •3.3. Химические свойства моносахаридов Реакции с участием карбонильной группы
- •Реакции с участием гидроксильных групп
- •3.4. Сложные углеводы
- •Олигосахариды
- •Полисахариды
- •Гомополисахариды
- •Гетерополисахариды
- •3.5. Биологические функции углеводов
- •Глава 4. Нуклеиновые кислоты
- •4.1. Общая характеристика нуклеиновых кислот
- •4.2. Химический состав и строение нуклеиновых кислот
- •4.3. Уровни структурной организации нуклеиновых кислот
- •Первичная структура нуклеиновых кислот
- •Вторичная структура днк
- •Вторичная структура рнк
- •Третичная структура рнк и днк
- •Глава 5. Липиды
- •5.1. Общая характеристика и классификация липидов
- •5.2. Липидные мономеры
- •5.3. Многокомпонентные липиды
- •5.4. Биологические функции липидов
- •Глава 6. Ферменты
- •6.2. Химическая природа и структура ферментов
- •6.3. Кофакторы ферментов Ионы металлов как кофакторы ферментов
- •Коферменты
- •6.4. Механизм действия ферментов
- •6.5. Свойства ферментов
- •6.6. Специфичность действия ферментов
- •6.7. Факторы, влияющие на скорость ферментативного катализа
- •Влияние температуры на активность ферментов
- •Влияние рН на активность ферментов
- •Влияние концентраций субстрата и фермента на скорость ферментативной реакции
- •Зависимость скорости реакции от времени
- •6.8. Регуляция активности ферментов
- •Активация ферментов
- •Ингибирование ферментов
- •Аллостерическая регуляций действия ферментов
- •6.9. Определение активности ферментов
- •6.10. Номенклатура и классификация ферментов
- •6.11. Локализация ферментов в организме и клетке
- •6.12. Применение ферментов
- •Глава 7. Витамины
- •7.1.Понятие о витаминах
- •7.2. Классификация витаминов
- •7.3. Жирорастворимые витамины
- •7.4. Водорастворимые витамины
- •7.5. Витаминоподобные вещества
- •Глава 8. Общие закономерности обмена веществ и энергии в организме
- •8.1. Обмен веществ
- •8.2. Обмен энергии
- •Глава 9. Биологическое окисление
- •9.2. Дыхательная цепь
- •9.3. Окислительное фосфорилирование
- •Глава 10. Обмен углеводов
- •10.1. Переваривание углеводов
- •10.2. Метаболизм глюкозы
- •10.3. Биосинтез гликогена
- •10.4. Распад гликогена
- •10.5. Анаэробный гликолиз
- •10.6. Аэробный распад глюкозы
- •Аэробный распад глюкозы в мозге
- •10.7. Пентозофосфатный цикл
- •10.8. Биосинтез глюкозы (глюконеогенез)
- •10.10. Регуляция обмена углеводов
- •Глава 11. Обмен липидов
- •11.1. Переваривание липидов
- •11.2. Метаболизм глицерина
- •11.3. Метаболизм жирных кислот
- •11.4. Биосинтез жиров
- •11.5. Регуляция обмена липидов
- •Глава 12. Обмен нуклеиновых кислот
- •12.1. Пути распада рнк и днк
- •12.2. Распад пуриновых и пиримидиновых оснований
- •12.3. Биосинтез нуклеотидов
- •Биосинтез пурииовых нуклеотидов
- •Биосинтез пиримидиновых нуклеотидов
- •Биосинтез дезоксирибонуклеотидов
- •12.4. Биосинтез нуклеиновых кислот
- •Биосинтез днк (репликация)
- •Биосинтез рнк (транскрипция)
- •Безматричный синтез рнк
- •12.5. Путь информации от генотипа к фенотипу
- •Глава 13. Обмен белков
- •13.1. Понятие об обмене белков
- •13.2. Переваривание белков пищи и распад белков тканей Переваривание белков
- •Распад белков в тканях
- •13.3. Метаболизм аминокислот
- •Трансаминирование аминокислот
- •Дезамииирование аминокислот
- •Превращение углеродных скелетов аминокислот. Реакции декарбоксилирования
- •13.4. Удаление аммиака из организма. Орнитиновый цикл
- •13.5. Синтез аминокислот
- •13.6. Биосинтез белков (трансляция)
- •Глава 14. Водно-солевой и минеральный обмен
- •14.1. Водно-солевой обмен Содержание воды в организме и клетке
- •Роль и функции воды в процессе жизнедеятельности
- •14.2. Регуляция водно-солевого обмена
- •Регуляция рН
- •14.3. Минеральный обмен Минеральные вещества
- •Функции минеральных веществ
- •Минеральные вещества и обмен нуклеиновых кислот
- •Минеральные вещества и обмен белков
- •Минеральные вещества и обмен углеводов и липидов
- •14.4. Регуляция минерального обмена
- •Глава 15. Взаимосвязь обмена белков, жиров, углеводов и нуклеиновых кислот
- •Глава 16. Гормоны, нервно-гормональная регуляция обмена веществ
- •16.1. Понятие о гормонах. Основные принципы регуляции обмена веществ
- •16.2. Классификация гормонов
- •16.3. Общие представления о действии гормонов
- •16.4. Гормоны щитовидной и паращитовидных желез Гормоны щитовидной железы
- •Гормоны паращитовидных желез
- •16.5. Гормоны поджелудочной железы
- •16.6. Гормоны надпочечников
- •16.7. Гормоны половых желез
- •16.8. Гормоны гипоталамо-гипофизарной системы
- •16.9. Гормоны тимуса и эпифиза
- •16.10. Простагландины
- •16.11. Биохимическая адаптация
- •Рекомендуемая литература
- •Оглавление
2.4. Аминокислотный состав белков
С химической точки зрения белки - это высокомолекулярные азотсодержащие органические соединения (полиамиды), молекулы которых построены из остатков аминокислот. Мономерами белков служат α-аминокислоты, общим признаком которых является наличие карбоксильной группы -СООН и аминогруппы -NH2 у второго углеродного атома (α-углеродный атом):

Аминокислоты классифицируют: - по полярности радикалов на полярные (гидрофильные) и неполярные (гидрофобные);
- по природе радикалов на алифатические (глицин, аланин, валин, лейцин, изолейцин); гидроксиаминокислоты (серии, треонин); дикарбоновые, кислые, (аспарагиновая, глутаминовая и их амиды - аспарагин и глутамин); тиоаминокислоты (цистеин, метионин); диаминомонокарбоновые, щелочные (лизин, аргинин); ароматические (фенилаланин, тирозин); гетероциклические (триптофан, гистидин, пролин).
В настоящее время известно более 200 аминокислот, существующих в природе. В организме человека содержится около 60 различных аминокислот и их производных. В белках же всех видов живых существ - от бактерий до человека - обнаруживают менее 30 из них.
Эти аминокислоты делят на две группы: постоянно встречающиеся в белках (главные) и иногда встречающиеся (редкие). К первой группе относят 20 аминокислот (в том числе и пролин, который, по существу, является иминокислотой) (табл.4).
Таблица 4. Аминокислоты, постоянно встречающиеся в составе белков
|
№ п/п |
Название |
Структура |
Сокращенное обозначение русское, латинское |
pI |
|
1 |
2 |
3 |
4 |
5 |
|
I. Неполярные(гидрофобные) аминокислоты | ||||
|
1. |
Аланин |
|
Ала, Ala |
6,02 |
|
2. |
Валин |
|
Вал, Val |
5,97 |
|
3. |
Лейцин |
|
Лей, Leu |
5,98 |
|
4. |
Изолейцин |
|
Иле, Ile |
6,02 |
|
5. |
Триптофан |
|
Три, Try |
5,88 |
|
6. |
Пролин (иминокислота) |
|
Про, Pro |
6,10 |
|
7. |
Фенилаланин |
|
Фен, Phe |
5,98 |
|
8. |
Метионин |
|
Meт, Met |
5,75 |
|
1 |
2 |
3 |
4 |
5 |
|
II. Полярные (гидрофильные) незаряженные аминокислоты | ||||
|
9. |
Глицин |
|
Гли, Gly |
5,97 |
|
10. |
Серин |
|
Сер, Ser |
5,68 |
|
11. |
Треонин |
|
Тре, Thr |
6,53 |
|
12. |
Цистеин |
|
Цис, Cys |
5,02 |
|
13. |
Тирозин |
|
Тир, Tyr |
5,65 |
|
14. |
Аспарагин |
|
Асн, Asn |
5,41 |
|
15. |
Глутамин |
|
Гли,Gln |
5,65 |
|
1 |
2 |
3 |
4 |
5 |
|
III. Отрицательно заряженные (кислые) аминокислоты | ||||
|
16. |
Аспарагиновая кислота (Аспартат) |
|
Асп, Asp |
2,95 |
|
17. |
Глутаминовая кислота (Глутамат) |
|
Глу, Glu |
3,22 |
|
IV. Положительно заряженные (основные) аминокислоты | ||||
|
18. |
Лизин |
|
Лиз, Lys |
9,74 |
|
19. |
Аргинин |
|
Арг, Arg |
10,76 |
|
20. |
Гистидин |
|
Гис, His |
7,58 |
К группе редко встречающихся аминокислот принадлежат, например, гидроксипролин, гидроксилизин, орнитин, йодтирозин, α-аминоизомасляная кислота и некоторые другие. Они имеют следующее строение:
|
|
|
| |
|
α-аминоизомасляная кислота |
гидроксипролин |
орнитин | |
|
|
| ||
|
йодтирозин |
гидроксилизин | ||
Эти аминокислоты образуются из главных уже после включения их в состав белковой молекулы.