
- •Нейроиммунология
- •Вступление
- •Часть I Экспериментальная нейроімунологія/Нейроімунофізіологія
- •Микроглиальные клетки.
- •Часть іі Нероимунопатология
- •Вывод. Тема №1. Нейроиммунология – самостоятельная научная дисциплина.
- •Общие свойства нервной и иммунной систем организма
- •Морфофункциональни и гуморальные аспекты взаимодействия нервной и иммунной систем
- •Нейроиммунология – новая комплексная междисциплинарная наука
- •Тема № 2. Филогенез и онтогенез нейроиммунной системы
- •Этапы эволюционного развития нервной и иммунной систем
- •Молекулярная эволюция белков нейроиммунной системы
- •2.1. Лектини как общее звено в филогенезе нейроиммунной системы
- •2.1.1. Лектини s-типу
- •2.1.2. Лектини с-типу
- •2.2. Сверхсемья иммуноглобулинов
- •Эволюция структур мозга, который определяет особенности функционирования нейроиммунной системы
- •3.1. Гематоенцефаличний барьер (геб)
- •3.2. Мозговые оболочки и субарахноидальные пространства
- •3.3. Ликвор
- •Свойства нейроиммунной системы, которые обусловлены онтогенетический ранней изоляцией центральной нервной системы.
- •5. Вывод
- •Важность связей нервной, эндокринной и иммунной систем.
- •2. Гуморальные факторы иммунной системы.
- •3. Влияние эндокринной системы на нервную и иммунную.
- •4. Влияние нервной системы на эндокринную и иммунную.
- •5. Вывод.
- •Тема № 4. Иммунные свойства клеток головного мозга
- •1. Местная иммунная система мозга как следствие его иммунологической изолированности.
- •2. Макрофаги мозга.
- •3. Микроглиальные клетки.
- •4. Астроциты
- •5. Олигодендроцити
- •6. Нейроны
- •7. Иммунная толерантность в цнс
- •8. Иммунный ответ в цнс
- •9. Экспрессия нервными клетками молекул, которые принимают участие в иммунном ответе.
- •Микроглиальные клетки.
- •9.2. Астроциты
- •9.3. Нейроны
- •10. Роль цитокинов в развитии патологических иммунных реакций в цнс
- •11. Вывод
- •Тема № 5. Влияние клеток головного мозга на клеточный и гуморальный иммунный ответ
- •1. Представление о механизмах нейроиммунного взаимодействия.
- •2. Симпатичный и парасимпатический отделы вегетативной нервной системы и регуляция иммунного ответа.
- •3. Гипоталамо-гипофизарно-наднирникова система
- •Молекулярные механизмы влияния клеток головного мозга на клетки иммунной системы.
- •5. Влияние изменений в центральной нервной системе на иммунную систему.
- •6. Презентация антигенов в центральной нервной системе.
- •Тема № 6. Влияние клеток головного мозга на функциональную активность фагоцитирующих клеток
- •Молекулярные основы взаимодействия полімофноядерних лейкоцитов с клетками головного мозга.
- •2. Роль нейтрофилов и макрофагов при развитии патологических процессов, которые возникают в головном мозге.
- •3. Влияние разных фракций клеток головного мозга на фагоцитарную активность клеток иммунной системы.
- •Механизмы центральной регуляции функциональной активности нейтрофилов нервными клетками.
- •5. Вывод
- •1. Понятие о гематоенцефалічний барьере и его транспортные функции.
- •2. Морфология и формирование гематоенцефалічного барьера
- •3. Физиология гематоенцефалічного барьера
- •4. Метаболические функции гематоенцефалічного барьера
- •5. Механизмы нарушения проницаемости гематоенцефалічного барьера при некоторых заболеваниях цнс.
- •5.1. Острая церебральная ишемия.
- •5.2. Опухоли головного мозга.
- •5.3. Рассеянный склероз.
- •6. Вывод
- •Тема № 8. Влияние иммунной системы на функциональную активность нервной системы
- •Гуморальные факторы, общие для нервной и иммунной системы
- •2. Влияние мононуклеарных клеток на синтез гамк и катехоламинов нейронами мозга.
- •3. Влияние разных популяций клеток иммунной системы на синтез нейромедиаторов и фактора некроза опухолей.
- •3.1. Катехоламины.
- •3.2. Гамк
- •4. Вековые особенности взаимодействия клеток нервной и иммунной систем in vitro.
- •5. Вывод
- •Тема № 9. Влияние иммунной системы на активность нервных клеток при развитии патологических процессов в цнс на примере экспериментального аллергического энцефаломиелита
- •Локальная иммунная система цнс
- •2. Микроглия
- •3. Астроциты.
- •4. Функционирование микроглии и астроцитов при условиях развития патологии
- •5. Цитотоксическая активность и синтез цитокинов клетками иммунной и нервной систем.
- •6 Вывод
- •Тема № 10. Нарушение функций нейроиммунной системы в состоянии стресса и стресіндукованої патологии.
- •1. Фазы стресса
- •2. Изменения функционирования организма в условиях стресую
- •3. Иммуносупрессивные эффекты стресса
- •4. Влияние стресса на взаимоотношения нервной, иммунной и гуморальной систем организма.
- •5. Вывод
- •Часть іі Нероимунопатология Тема №11. Черепномозговая травма и травматическая болезнь мозга. Нейроиммунологические аспекты проблемы.
- •1. Общая классификация травматических повреждений.
- •Сотрясение головного мозга
- •Контузия головного мозга
- •1.3.Сдавливание вещества мозга
- •1.4.Открытые травмы черепа
- •2. Посттравматические патофизиологические процессы.
- •2.1. Патогенез первых стадий повреждения мозга
- •2.2. Кислородное голодание и отек мозгу (едема).
- •2.3. Оедема
- •2.4. Воспаление.
- •2.5. Патогенез разрушения клеток.
- •2.5.1. Цитолиз клеток.
- •2.5.2. Ексайтотоксичнисть.
- •2.5.3. Окисел азота.
- •2.5.4. Реактивные производные кислорода.
- •2.6. Механизмы клеточной смерти.
- •2.7.Демиелинизация нервных волокон.
- •2.8.Аксотомия.
- •2.9. Развитие аутоімунних процессов
- •3. Взаимосвязь нервной и иммунной системы и их участие в патофизиологических процессах после травматического повреждения мозга.
- •4. Роль цитокинов.
- •5. Клеточный компонент нейровоспаления.
- •6. Система комплемента.
- •7. Заживление ран. Регенерация.
- •8. Вывод
- •Тема №12 Острая и хроническая недостаточность мозгового кровообращения и их протекания
- •Общая характеристика острой недостаточности мозгового кровообращения.
- •Патофизиологические механизмы инсульта
- •Развитие воспаления при ишемическом инсульте
- •Иммунный компонент патогенеза инсульта.
- •4.1.Роль сосудистой стенки в регуляции клеточного и гуморального иммунитета при инсульте.
- •Иммунная реакция.
- •Механизм гибели нейронов.
- •Вековое и половое влияние на степень и вид нервных нарушений при инсультах.
- •Нарушение трофики нейронов.
- •8. Вывод
- •Тема № 13. Нейроиммунные нарушения, которые развиваются при демиелинизирующих заболеваниях цнс (на примере рассеянного склероза)
- •1. Демиелинизирующие заболевания цнс человека.
- •2.1.Эпидемиология.
- •2.2. Механизм патогенеза рс.
- •2.2.1.Генетическая обусловленность.
- •2.2.2.Роль иммунной системы.
- •3. Моделирование демиелинизирующих заболеваний.
- •Тема № 14. Воспалительные инфекционные процессы в цнс.
- •1.Инфекционно воспалительные процессы головного мозга
- •2.Энцефалит
- •2.1.Клещевой энцефалит
- •2.2. Эпидемический энцефалит
- •2.3. Гриппозный энцефалит
- •2.4.Диагностика
- •3.Менингит
- •3.1.Бактериальные формы менингитов.
- •3.1.1.Цереброспинальный менингит.
- •3.1.2.Вторичные гнойные менингиты.
- •3.1.3.Лечение.
- •3.1.4.Туберкулезный менингит.
- •3.2.Вирусные формы менингитов.
- •3.2.1.Лимфоцитарний хориоменингит.
- •3.2.2.Ентеровирусний менингит.
- •4.Нейроиммунопатология при инфекционных заболеваниях в цнс
- •5.Вывод
- •1.Морфо-функціональні изменения мозга при старении.
- •2.Вековые изменения нервов.
- •3.Старение епіфіза.
- •4.Старение гипоталамуса.
- •5.Молекулярные механизмы клеточного старения.
- •6.Роль дерегуляції апоптоза в патогенезе дегенеративных заболеваний цнс.
- •7.Нейроиммунные и эндокринные вековые нарушения.
- •8.Цитокины и старения.
- •9.Механизмы антистарения.
- •10.Иммунотерапевтические средства противодействия старению.
- •11.Вывод
- •Тема № 16. Нейродегенеративни и вековые заболевания. Особливости нейроиммунологических нарушений.
- •1.Общие характеристика болезни Альцгеймера
- •1.1.Этиология и патогенез.
- •1.2.Генетические механизмы.
- •1.3.Молекулярные аспекты.
- •2. Нейроиммунологические нарушения при болезни Альцгеймера.
- •3. Иммунный статус у пациентов с болезнью Альцгеймера.
- •4. Роль антител в патогенезе болезни Альцгеймера.
- •5. Связь иммунологического статуса с когнитивными нарушениями.
- •6. Вывод.
- •Тема №17. Нейроаутоимунни основы развития органических поражений мозга у детей раннего возраста
- •1.Изменения в нейроиммунной системе при некоторых расстройствах нервной регуляции в детском возрасте
- •2. Причины развития дцп.
- •3.Классификация дцп.
- •4.Синдромы физиологичных нарушений у больных на дцп.
- •5.Патолого-анатомічна картина у больных на дцп.
- •6.Нейроимунопатологични механизмы формирования дцп.
- •7.Иммунный статус и детей из дцп.
- •8.Гормональный статус у больных на дцп.
- •9.Роль нейроспецифических белков в патогенезе дцп.
- •10.Вывод
- •Тема №18. Нейроиммунные нарушения при нейроонкологических заболеваниях
- •Особенности развития злокачественных новообразований в мозге.
- •Нейроиммунные процессы при нейроонкологических заболеваниях.
- •3.Иммунотерапия и иммунопрофилактика злокачественных новообразований мозга.
- •4.Вывод
- •Тема №19. Механизмы нейроиммунных нарушений при нейроэндокринной патологии.
- •1.Общая этиология и патогенез эндокринных расстройств.
- •2. Гипофункция эндокринных желез.
- •3.Гиперфункция эндокринных желез и избыток гормонов.
- •4.Продукция аномальных гормонов.
- •5.Резистентность к действию гормонов.
- •6.Механизм иммунных нарушений при аутоімунних заболеваниях щитообразной железы.
- •6.1.Патогенез азщз.
- •6.2. Иммуногенетика азщз.
- •Тема №20. Нейроиммунные нарушения при психических заболеваниях.
- •1.Классификация, этиология и патогенез депрессий.
- •2.Нейроиммунные механизмы в патогенезе развития депрессий.
- •3.Общая этиология и патогенез шизофрении.
- •4.Нейроиммунные реакции при шизофрении.
- •5.Вывод
2.5.4. Реактивные производные кислорода.
Длительное повышение внутриклеточной концентрации кислорода ведет к образованию аніоних радикалов суперокислов респираторной цепью, цитозольними ферментами (ксантиноксидаза). Это ведет к усилению оксидативного стресса. Мозг является высокочувствительным к оксидативным нарушениям, поскольку характеризуется высоким уровнем оксидативной метаболической активности, интенсивной продукцией реактивных производных кислорода, низким антиоксидантними возможностями, низкой активностью механизма репарации и высоким ядерноцитоплазматичним соотношением. Повышенная продукция реактивных производных кислорода ведет к перекисного окисает липидов. Мозг также содержит большое количество переходных металлов, таких как железо, марганец, медь. Эти редокс-активні металлы могут катализировать продукцию высокотоксичных радикалов через метал-опосередковану реакцию Хабера-Веиса. Поэтому считают, что высокореактивные радикалы длилось продуцируются в мозге, как результат взаимодействия между переходными металлами и обновляющими эквивалентами. Это очень важно при травме, когда мобилизация редокс-активних металлов может происходить, в результате их экспозиции с обновляющими агентами. Через 3-4 часа после травмы нейтрализация реактивных производных кислорода и азота может обеспечить нейропротекцию, антиоксиданты предотвращают разрушение тканей при травме [4].
Некоторые исследования указывают на фермент липооксигеназу как на фактор, который играет важную роль в развитии вторичного впечатления мозга. Оксидативный стресс (перекиснет окисление липидов) сопровождается запуском липооксигеназы в нейронах и эндотелиоцитах. В последних она вызывает деградацию белка плотных контактов эндотелия – клаудину 5. Это в свою очередь ведет к нарушению целостности ГЕБ, которая сопровождается отеком и геморрагическим впечатлением окружающих тканей. Кроме того, как обнаружено, липооксигеназа причастна к деградации митохондрий и других клеточных структур нейронов. Экспериментальные данные подтверждают возможность блокирования липооксигеназы с помощью ингибиторов (байкалеїн, едаравон, мелатонін, некоторые поліфеноли зеленого чая), как нейропротективний мероприятие [7]. С другой стороны известная способность липооксигеназы к синтезу резолвінів и протектинів (resolvin, protectin), что владеют противовоспалительными свойствами, из поліненасичених жирных кислот – ейкозапентаенової и докозагексаенової кислот соответственно [8].
2.6. Механизмы клеточной смерти.
На сегодня описаны два основных пути клеточной смерти: некроз и апоптоз. Первый из них является пассивным процессом, второй – активным.
Некроз – это процесс, который может быть вызван практически всеми патологическими влияниями, в том числе и травматическими поражениями мозга. Последовательность патологических процессов при некрозе всегда подобна: осмолізис, вызванный отеком клеток, приводит до пассивной смерти поврежденных клеток. Некроз поражает не только нервные клетки. Одним из вторичных его эффектов представляется воспаление, вызванное высвобожденным содержимым клеток и сопровождается синтезом цитокинов.
Другим механизмом клеточной смерти является апоптоз – вариант клеточной смерти, при котором активируются внутриклеточные механизмы. В отличие от некроза, апоптоз требует АТФ. Механизмы, которые приводят к апоптичної гибели, включают несколько путей: NF-kB (nuclear factor kappa-light-chain-enhancer of activated B cells), р53-залежний путь, активацию індуцибельних проапоптичних белков семьи bcl.
Апоптоз нейронов, эндотелиоцитов, астроцитов запускаюється через CD95. Обнаружены высокие концентрации CD95-ліганду в спинномозговой жидкости пациентов с тяжелыми травматическими поражениями мозга. В этом процессе ведущая роль принадлежит каспазі 3.
Считают, что гибель нейронов осуществляется за механизмом «Kindergarden effect» (мал.2), который заключается в следующем. Инициирующий нейрон (серый на рис.2.) проходит через сигнальный каскад клеточной смерти, активируются апоптичні каспази, продуцируются диффузионные токсичные факторы (IL-1?, TNF-?) и реактивные производные кислорода.
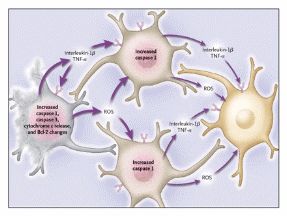
Рис.2. Механизм гибели нейронов.
Эти факторы индуктируют апоптоз в соседних с ними кітинах («kindergarden effect»). Наиболее раннее событие в этом процессе - активация каспази 1 (ИСЕ – інтерлейкін-1р-конвертуюча протеаза). Ведущую роль в активации этого фермента играют митохондриальные факторы, в частности цитохром С. Також каспази активируются при гипогликемии, избытке Са2+, депривації нейротрофических факторов. Поскольку нейроны становятся дизфункціональними, они начинают продуцировать такие же токсичные факторы, которые будут влиять, на соседние здоровые клетки. Клетка умирает, когда достигнет уровня летальных изменений. Процесс гибели клеток может влиять на гибель соседних клеток. При ишемии нейроны продуцируют IL-1?, TNF-? и реактивные производные кислорода. Те нейроны, которые не погибли от ишемии, погибнут от совместимого действия мікрооточеня, которое возникло после ишемии и действия токсичных соединений.
Повреждение мозга сопровождается нарастанием продукции TNF-?, что инициирует нейрональний апоптоз и неврологические нарушения. Запуск TNF-?-залежного апоптозу регулируется уровнем р55 — ізоформного белка, связанного из TNF-? рецептором. Также под воздействием некоторых цитокинов отмечается стимуляция активности стрес-активованих кіназ - р38 мітоген-активованої протеїнкінази (р38МАРК) и Jun-N-термінальної кінази (JNK). Связывание TNF-? из р55 активирует несколько внутриклеточных компонентов, таких, как TNF-рецептор ассоциируемого домену гибели клеток (TRADD), а также домену гибели р55-рецептора и ассоциируемых протеинов (например, каспази 8, TNF-рецептор ассоциируемого фактора TRAF), активация которого приводит в конечном итоге к гибели. В роботе Venters et al. (1999) рассмотренная концепция TNF-?- индуктируемой нейродегенерации. Авторы указывают на возможность существования другого (нового) уровня регуляторных отношений между про- и противовоспалительными цитокинами в мозге. Эта регуляция базируется на внутриклеточном взаимодействии между гетерологічними рецепторами отдельно взятой клетки, и результатом этого взаимодействия может быть как активация, так и притеснение рецепторной активности. Например, если рецептор, ответственный за гибель клетки (например, рецептор TNF-?) взаимодействует с рецептором выживания клетки (например, рецептором IGF-1), он может тормозить IGF-1-залежну нейропротекцию; подобное взаимодействие авторы помечают как «умалчивание сигналов к выживанию» ("silencing of survival signals", SOSS). Хотя механизмы и медиаторы действия IL-1 в процессах нейродегенерации не установлены, механизмы типа SOSS, очевидно, являются достаточно существенными как для IL-1, так и для других прозапальних цитокинов.
Следует отметить, что IL-1, как и TNF-?, индуктируется при разных повреждениях мозга и усиливает эффект ишемии ткани мозга, не будучи при этом токсичным для нормальной ткани или нормальных нейронов. Можно также допустить, что, кроме приведенных механизмов, много других факторов (фосфоліпаза А2, циклооксигеназа, окисел азота, суперокислы и тому подобное), могут быть индуктируемые или активированные под воздействием IL-1 и других прозапальних цитокинов, также могут быть привлеченные в процессы повреждения нейронов. Поскольку прозапальні цитокины не являются нейротоксичными, весьма возможно, что они влияют не только на выживание нейронов, действуя на рецептор-рецепторні механизмы, но и на клеточно-клеточные взаимодействия. На основе экспериментов in vitro, которые засвидетельствовали, что IL-1 и TNF-? усиливают гибель нейронов в смешанной культуре нейронов и глиальных клеток, достаточно вероятно, что цитокины высвобождаются в подобных условиях именно глиальными клетками, которые продуцируют окисел азота. При этом, при первичном повреждении мозга источником IL-1 и TNF-? есть клетки микроглии, хотя астроциты, олігодендроцити и другие клетки относительно этого также активны.
