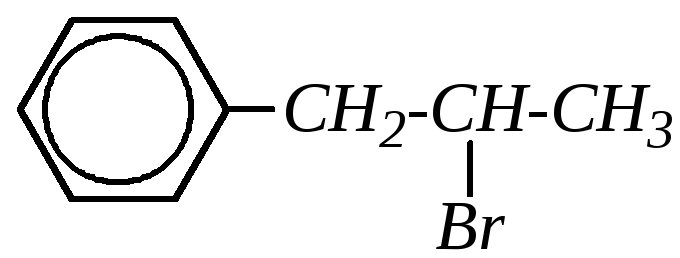- •Глава 10. Функциональные производные углеводородов ряда бензола
- •10.1. Общность строения и свойств монозамещённых бензолов
- •10.1.1. Электронные эффекты заместителей
- •10.1.2. Реакции электрофильного замещения
- •10.1.3. Реакции нуклеофильного замещения
- •10.2. Галогенарены
- •10.2.1. Классификация, номенклатура
- •10.2.2. Строение арилгалогенидов
- •10.2.3. Физические свойства
- •10.2.4. Химические свойства
- •10.2.5. Способы получения
- •10.2.6. Важнейшие представители
- •10.3. Ароматические сульфокислоты
- •10.3.1. Номенклатура
- •10.3.2. Строение
- •10.3.3. Физические и химические свойства
- •10.3.4. Способы получения
- •10.3.5. Производные сульфокислот
- •10.3.6. Медико-биологическое значение и Важнейшие представители
- •10.4. Ароматические нитросоединения
- •10.4.1. Строение нитробензола
- •10.4.2. Физические свойства
- •10.4.3. Химические свойства
- •10.4.4. Способы получения
- •10.4.5. Физиологическое действие и Важнейшие представители
- •10.5. Фенолы. Ароматические спирты. Хиноны
- •10.5.1. Классификация, номенклатура, изомерия фенолов и ароматических спиртов
- •10.5.2. Строение фенола и бензилового спирта
- •Ароматические амины и продукты неполного восстановления нитросоединений
- •10.6.1. Классификация, номенклатура, изомерия ароматических аминов
- •10.6.2. Строение анилина
- •10.6.3. Физические и химические свойства ароматических аминов
- •10.6.4. Способы получения ароматических аминов
- •10.6.5. Важнейшие представители ароматических аминов
- •10.6.6. Продукты неполного восстановления нитросоединений
- •10.7. Ароматические диазосоединения
- •10.7.1. Номенклатура диазосоединений
- •10.7.2. Механизм образования солей арендиазония и строение катиона бензолдиазония
- •10.7.3. Амфотерность диазосоединений
- •10.7.4. Реакции солей арендиазония
- •10.8. Ароматические альдегиды и кетоны
- •10.8.1. Изомерия, номенклатура
- •10.8.2. Строение бензальдегида
- •10.8.3. Физические и химические свойства
- •10.8.4. Способы получения
- •10.8.5. Важнейшие представители
- •10.9. Ароматические карбоновые кислоты и их производные
- •10.9.1. Классификация, номенклатура
- •10.9.2. Строение бензойной кислоты
- •10.9.3. Физические и химические свойства
- •10.9.4. Способы получения
- •10.9.5. Важнейшие представители
- •10.10. Физиологическая роль функциональных производных бензола
- •Вопросы и упражнения
10.2. Галогенарены
Молекулы ароматических углеводородов могут содержать атомы галогенов как в ароматическом кольце, так и в боковой алифатической цепи. Такие соединения принято называть галогенопроизводными ароматических углеводородов, или галогенаренами.
10.2.1. Классификация, номенклатура
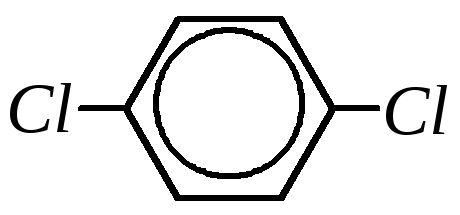
В зависимости от расположения галогена все галогенопроизводные ароматических углеводородов делятся на две группы: 1) соединения с атомом галогена в ароматическом кольце, например:
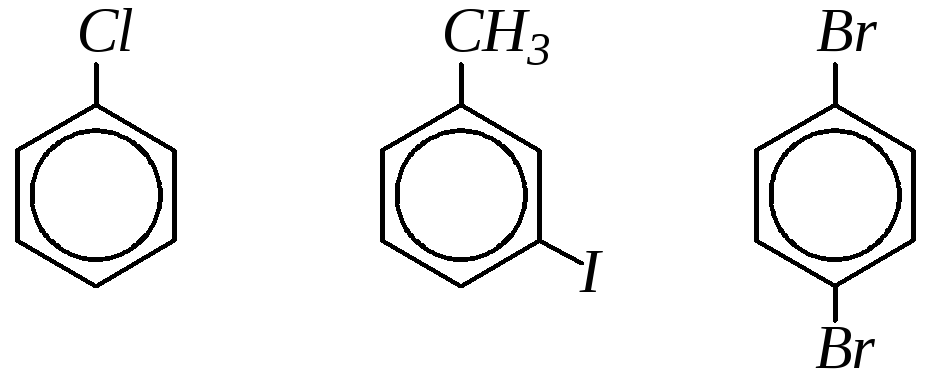
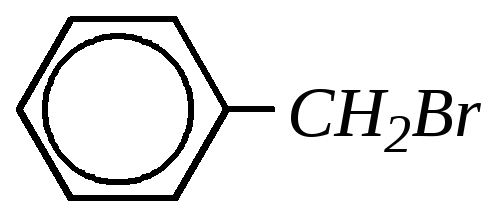
2) соединения с атомом галогена в боковой цепи, например:
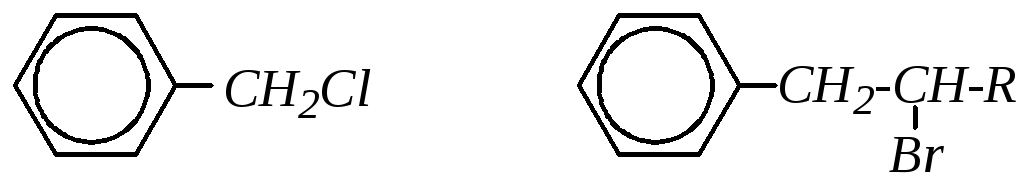
Соединения первой из этих двух групп получили название арилгалогенидов, так как в их молекулах атом галогена связан с ароматическим радикалом – арилом. Поэтому общую формулу галогенаренов с одним атомом галогена в ароматическом кольце можно представить в виде Ar-Hal.
Кроме того, так же, как и алифатические галогенопроизводные, рассматриваемые соединения могут быть классифицированы в зависимости от числа атомов галогена и от их природы.
Для названия галогенаренов могут с успехом применяться как радикало-функциональная, так и заместительная номенклатуры ИЮПАК. По радикало-функциональной номенклатуре необходимо использовать названия углеводородных радикалов, связанных с атомом (или атомами) галогена. Это может быть осуществлено только для относительно несложных по структуре соединений. Например:
|
|
— п-толилхлорид, |
|
|
|
|
|
— бензилбромид, |
|
|
|
|
|
— п-фенилендихлорид. |
Если название даётся по заместительной номенклатуре, то в качестве родоначальной структуры может выбираться либо ароматическое кольцо, либо (для соединений с атомом галогена в боковой цепи) боковая алифатическая цепь. В первом случае для обозначения атомов углерода боковой цепи могут использоваться греческие буквы. Например:
|
|
— 2'-бромпропилбензол, или -бромпропилбензол, или 2-бром-1-фенилпропан |
|
|
|
|
|
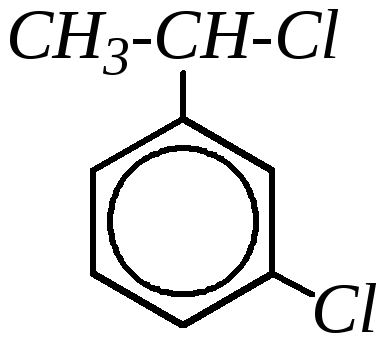
— 3-хлор-1-(1'-хлорэтил)-бензол, или м-хлор--хлорэтилбензол, или 1-хлор-1-(3'-хлорфенил)-этан, или 1-хлор-1-(м-хлорфенил)-этан |
10.2.2. Строение арилгалогенидов
А том
галогена влияет на распределение
электронной плотности в бензольном
кольце за счёт –I-
и +М-эффектов.
том
галогена влияет на распределение
электронной плотности в бензольном
кольце за счёт –I-
и +М-эффектов.
В молекуле хлорбензола –I-эффект выражен сильнее +М-эффекта. Это подтверждается направлением дипольного момента связи C–Cl. За счёт р--сопряжения увеличивается степень двоесвязанности между углеродом и хлором: эта связь имеет 10% -характера. Строение арилгалогенидов сходно со строением галогеналкенов винильного типа (гл. 5.1.2). Так же, как и в винилхлориде, длина связи C–Cl в хлорбензоле меньше, чем в соответствующих предельных галогенопроизводных (в хлорбензоле 0.170 нм, в хлорэтане 0.177 нм), а прочность этой связи больше, чем в галогеналканах (в хлорбензоле 397.8 кДж/моль, в хлорэтане 341.2 кДж/моль).
Положительный мезомерный эффект, хотя и слабее отрицательного индуктивного эффекта, приводит к ряду особенностей в строении и свойствах арилгалогенидов. За счёт +М-эффекта происходит повышение электронной плотности на атомах углерода в о- и п-положениях ароматического кольца по сравнению с углеродными атомами в м-положениях. Распределение электронной плотности можно представить как промежуточное между пятью граничными структурами:

В результате такого сопряжения образуется единая -молекулярная орбиталь. Этому состоянию отвечает мезоформула

Однако вследствие влияния большего по величине индуктивного эффекта электронная плотность на кольце в целом понижена; в наибольшей степени она оказывается понижена в м-положении, так как в о- и п-положениях происходит частичная компенсация дефицита электронной плотности за счёт +М-эффекта. Поэтому в целом распределение электронной плотности в молекуле хлорбензола можно представить следующим образом:
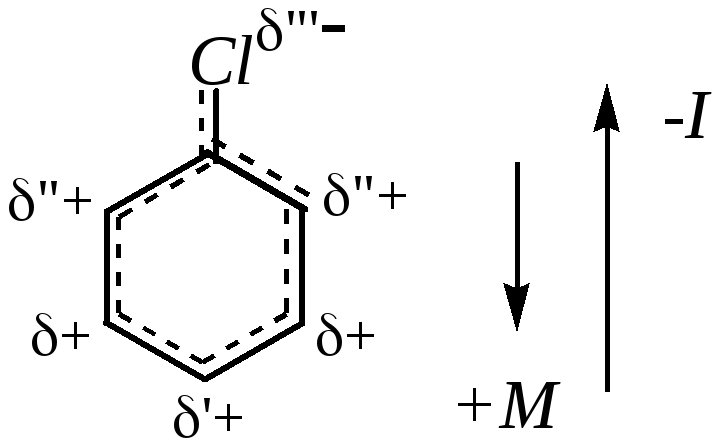 ,
причём +
> '+,
"+
,
причём +
> '+,
"+
В молекулах других галогенобензолов взаимодействие ароматического кольца с атомами галогенов осуществляется за счёт тех же электронных эффектов: индуктивного и мезомерного. Однако существенного повышения или понижения электронной плотности на ароматическом кольце этих галогенопроизводных (в ряду фторбензол—йодбензол) не наблюдается, так как одновременно с уменьшением –I-эффекта атома галогена (от фтора к йоду) происходит и уменьшение +М-эффекта. Уменьшение индуктивного эффекта связано с понижением электроотрицательности в ряду галогенов (фтор—йод); уменьшение электронодонорного мезомерного эффекта связано с возрастанием несоответствия геометрической конфигурации внешних р-орбиталей атомов углерода и галогена (также от фтора к йоду).