
- •Глава 10. Функциональные производные углеводородов ряда бензола
- •10.1. Общность строения и свойств монозамещённых бензолов
- •10.1.1. Электронные эффекты заместителей
- •10.1.2. Реакции электрофильного замещения
- •10.1.3. Реакции нуклеофильного замещения
- •10.2. Галогенарены
- •10.2.1. Классификация, номенклатура
- •10.2.2. Строение арилгалогенидов
- •10.2.3. Физические свойства
- •10.2.4. Химические свойства
- •10.2.5. Способы получения
- •10.2.6. Важнейшие представители
- •10.3. Ароматические сульфокислоты
- •10.3.1. Номенклатура
- •10.3.2. Строение
- •10.3.3. Физические и химические свойства
- •10.3.4. Способы получения
- •10.3.5. Производные сульфокислот
- •10.3.6. Медико-биологическое значение и Важнейшие представители
- •10.4. Ароматические нитросоединения
- •10.4.1. Строение нитробензола
- •10.4.2. Физические свойства
- •10.4.3. Химические свойства
- •10.4.4. Способы получения
- •10.4.5. Физиологическое действие и Важнейшие представители
- •10.5. Фенолы. Ароматические спирты. Хиноны
- •10.5.1. Классификация, номенклатура, изомерия фенолов и ароматических спиртов
- •10.5.2. Строение фенола и бензилового спирта
- •Ароматические амины и продукты неполного восстановления нитросоединений
- •10.6.1. Классификация, номенклатура, изомерия ароматических аминов
- •10.6.2. Строение анилина
- •10.6.3. Физические и химические свойства ароматических аминов
- •10.6.4. Способы получения ароматических аминов
- •10.6.5. Важнейшие представители ароматических аминов
- •10.6.6. Продукты неполного восстановления нитросоединений
- •10.7. Ароматические диазосоединения
- •10.7.1. Номенклатура диазосоединений
- •10.7.2. Механизм образования солей арендиазония и строение катиона бензолдиазония
- •10.7.3. Амфотерность диазосоединений
- •10.7.4. Реакции солей арендиазония
- •10.8. Ароматические альдегиды и кетоны
- •10.8.1. Изомерия, номенклатура
- •10.8.2. Строение бензальдегида
- •10.8.3. Физические и химические свойства
- •10.8.4. Способы получения
- •10.8.5. Важнейшие представители
- •10.9. Ароматические карбоновые кислоты и их производные
- •10.9.1. Классификация, номенклатура
- •10.9.2. Строение бензойной кислоты
- •10.9.3. Физические и химические свойства
- •10.9.4. Способы получения
- •10.9.5. Важнейшие представители
- •10.10. Физиологическая роль функциональных производных бензола
- •Вопросы и упражнения
10.4.4. Способы получения
Существуют три основных способа получения соединений с нитрогруппой в ароматическом кольце и два способа получения соединений с нитрогруппой в боковой цепи.
Важнейшим способом получения нитробензола и его производных является прямое нитрование в бензольное кольцо (гл. 9.5.1.1), которое осуществляется азотной кислотой или нитрующей смесью. Существуют случаи использования и других нитрующих агентов. Это реакции замещения атомов водорода (или сульфогрупп) в бензольном кольце на нитрогруппы.
Другой способ получения — окисление ариламинов.
Ar-NH2
![]() Ar-NO2
Ar-NO2
В качестве окислителей применяют трифторпероксиуксусную кислоту CF3-CОOOH, перманганат калия, азотную кислоту или пероксид водорода. Этот способ применяется для получения таких нитроаренов, которые прямым нитрованием получить нельзя. Например:
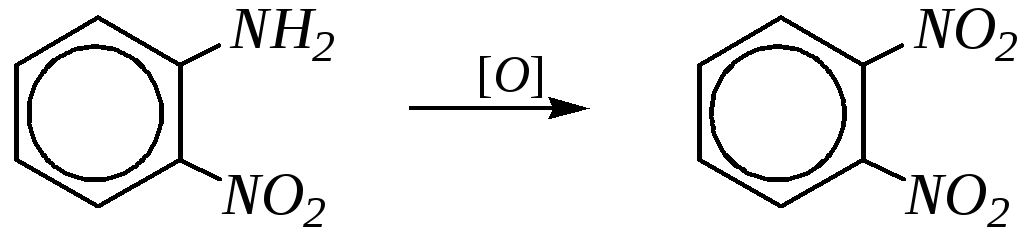
Соединения с нитрогруппой в ароматическом кольце могут быть получены при замене первичной аминогруппы через образование диазосоединений (реакция Зандмейера*–Гаттермана):
Ar-NH2
![]() [Ar-N2]+Cl¯
[Ar-N2]+Cl¯
![]() Ar-NO2
+ KCl + N2
Ar-NO2
+ KCl + N2
Прямое нитрование может быть применено и для получения соединений с нитрогруппой в боковой цепи (аналогично нитрованию алканов по М.И. Коновалову). Так, нитрование толуола и его гомологов разбавленной азотной кислотой при 400 К приводит к образованию -нитрозамещённых. Реакция протекает по радикальному механизму; её направление определяется стабильностью промежуточной частицы – радикала бензильного типа. Например:

Нуклеофильным замещением атома галогена в боковой цепи при взаимодействии с нитритами можно получать не только -, но и -, - и т.д. замещённые нитросоединения, например:
Ar-CH2-CH2-Br + NaNO2 Ar-CH2-CH2-NO2 + NaBr
Эта реакция аналогична нуклеофильному замещению в галогеналканах (гл. 3.2.2.1).
10.4.5. Физиологическое действие и Важнейшие представители
Ароматические нитросоединения угнетают нервную и особенно кровеносную систему, нарушая снабжение организма кислородом. Метаболизм нитросоединений связан с окислительно-восстановительными реакциями, и в частности с окислительным фосфорилированием.
Нитробензол — бесцветная или светло-жёлтая жидкость с запахом горького миндаля; температура плавления 279 К, температура кипения 484 К. Плохо растворим в воде. Является нервным и кровяным ядом.
Нитробензол является одним из важнейших продуктов органического синтеза. Получают его нитрованием бензола. Объём мирового производства нитробензола измеряется сотнями тысяч тонн. Около 90% нитробензола расходуется на производство анилина.
Тринитротолуол (тол, тротил) — жёлтое кристаллическое вещество с температурой плавления 353 К.
Получают нитрованием нитротолуолов. Является одним из наиболее распространённых взрывчатых веществ.
Пикриновая кислота (2,4,6-тринитрофенол) — жёлтое кристаллическое вещество с температурой плавления 396 К. Малорастворима в воде.
Получают нитрованием фенола и нитрофенолов. Использовалась в качестве жёлтого красителя. Её соли термически нестабильны, при нагревании взрываются.
