- •Глава 10. Функциональные производные углеводородов ряда бензола
- •10.1. Общность строения и свойств монозамещённых бензолов
- •10.1.1. Электронные эффекты заместителей
- •10.1.2. Реакции электрофильного замещения
- •10.1.3. Реакции нуклеофильного замещения
- •10.2. Галогенарены
- •10.2.1. Классификация, номенклатура
- •10.2.2. Строение арилгалогенидов
- •10.2.3. Физические свойства
- •10.2.4. Химические свойства
- •10.2.5. Способы получения
- •10.2.6. Важнейшие представители
- •10.3. Ароматические сульфокислоты
- •10.3.1. Номенклатура
- •10.3.2. Строение
- •10.3.3. Физические и химические свойства
- •10.3.4. Способы получения
- •10.3.5. Производные сульфокислот
- •10.3.6. Медико-биологическое значение и Важнейшие представители
- •10.4. Ароматические нитросоединения
- •10.4.1. Строение нитробензола
- •10.4.2. Физические свойства
- •10.4.3. Химические свойства
- •10.4.4. Способы получения
- •10.4.5. Физиологическое действие и Важнейшие представители
- •10.5. Фенолы. Ароматические спирты. Хиноны
- •10.5.1. Классификация, номенклатура, изомерия фенолов и ароматических спиртов
- •10.5.2. Строение фенола и бензилового спирта
- •Ароматические амины и продукты неполного восстановления нитросоединений
- •10.6.1. Классификация, номенклатура, изомерия ароматических аминов
- •10.6.2. Строение анилина
- •10.6.3. Физические и химические свойства ароматических аминов
- •10.6.4. Способы получения ароматических аминов
- •10.6.5. Важнейшие представители ароматических аминов
- •10.6.6. Продукты неполного восстановления нитросоединений
- •10.7. Ароматические диазосоединения
- •10.7.1. Номенклатура диазосоединений
- •10.7.2. Механизм образования солей арендиазония и строение катиона бензолдиазония
- •10.7.3. Амфотерность диазосоединений
- •10.7.4. Реакции солей арендиазония
- •10.8. Ароматические альдегиды и кетоны
- •10.8.1. Изомерия, номенклатура
- •10.8.2. Строение бензальдегида
- •10.8.3. Физические и химические свойства
- •10.8.4. Способы получения
- •10.8.5. Важнейшие представители
- •10.9. Ароматические карбоновые кислоты и их производные
- •10.9.1. Классификация, номенклатура
- •10.9.2. Строение бензойной кислоты
- •10.9.3. Физические и химические свойства
- •10.9.4. Способы получения
- •10.9.5. Важнейшие представители
- •10.10. Физиологическая роль функциональных производных бензола
- •Вопросы и упражнения
10.9.4. Способы получения
Для получения ароматических карбоновых кислот можно использовать способы, применяющиеся для получения их алифатических аналогов (гл. 6.4.5).
Окисление спиртов, альдегидов, кетонов.
Гидролиз ,,-тригалогенаренов.
Металлорганический синтез (карбоксилирование реактивов Гриньяра).
Гидролиз (гидратация) нитрилов.
Однако ароматические карбоновые кислоты и их производные можно получать и другими способами.
Окисление аренов кислородом в присутствии катализаторов (соли кобальта и марганца) или обычными неорганическими окислителями (перманганаты, дихроматы). Эти реакции были рассмотрены в главе 9.5.1.4.
Ацилирование аренов с помощью фосгена — прямой способ получения галогенангидридов:
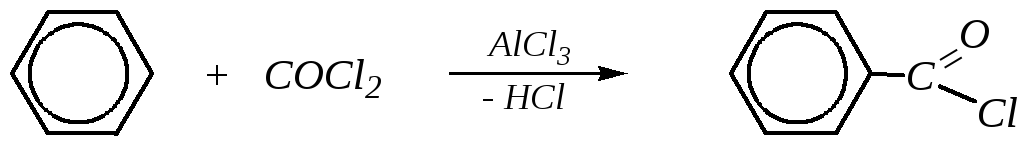
Это обычная реакция электрофильного замещения в ароматическое кольцо; такие реакции рассматривались в свойствах бензола и аренов.
10.9.5. Важнейшие представители
Бензойная кислота — бесцветное кристаллическое вещество с температурой плавления 395 К. Легко возгоняется. Обладает бактерицидными свойствами. В промышленности бензойную кислоту получают окислением толуола.
Используется для получения красителей, душистых и лекарственных веществ.
п-Аминобензойная кислота (витамин H1) участвует во многих жизненно важных процессах в качестве промежуточного вещества. В связи с этим является жизненно важным фактором для многих микроорганизмов, а также необходимым элементом для биосинтеза некоторых витаминов. Эфиры п-аминобензойной кислоты нашли применение в медицине как лекарственные вещества с местноанестезирующим действием. Примерами таких веществ могут служить новокаин и анестезин. Этиловый эфир п-аминобензойной кислоты (анестезин) применяется как местноанестезирующее средство более 70 лет. Получают его из п-нитротолуола по следующей схеме:
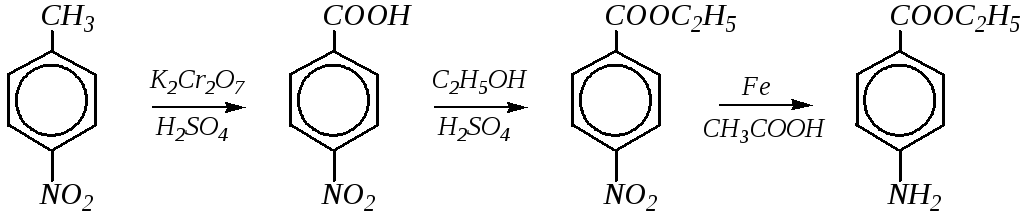
анестезин
Терефталевая кислота — бесцветное кристаллическое вещество с температурой плавления 698 К, но при температуре 573 К возгоняется.
В промышленности терефталевую кислоту получают окислением п-ксилола кислородом воздуха.
Используется в производстве синтетического волокна лавсана (полиэтилентерефталата) и кевлара (поли-п-фенилентерефталата). Такие полимеры обладают прекрасной термической устойчивостью (что определяется наличием ароматических циклов) и очень хорошими механическими свойствами.
Ф талевый
ангидрид—
бесцветное кристаллическое вещество
с температурой плавления 404 К.
талевый
ангидрид—
бесцветное кристаллическое вещество
с температурой плавления 404 К.
В промышленности фталевый ангидрид получают окислением нафталина или о-ксилола.
Применяется для получения полиэфиров, пластификаторов и красителей; используется в органическом синтезе для получения биологически активных соединений.
Салициловая кислота (гл. 10.5.3, 10.9.3.1) — бесцветное кристаллическое вещество с температурой плавления 432 К. Легко возгоняется. В промышленности получают карбоксилированием фенола.
Салициловая кислота и её производные используют в медицине в качестве лекарственных препаратов.
10.10. Физиологическая роль функциональных производных бензола
Как уже указывалось в главе 9.7, при метаболическом окислении ароматических углеводородов в результате ароматического гидроксилирования образуются фенолы. Аналогичные продукты образуются и при окислении различных функциональных производных. Важную роль здесь играет структурная избирательность, зависящая от свойств субстрата. Например, при метаболизме анилина образуются все три возможных изомерных гидроксипроизводных (50 % п-гидроксианилина, 10 %о-изомера и 0.1 %м-изомера), тогда как из нитробензола преимущественно образуютсяп- им-изомеры. Если бензольное ядро ксенобиотика содержит несколько заместителей, то гидроксилирование может идти по нескольким положениям, как, например, в случае салициловой кислоты:

салициловая кислота
Среди лекарственных препаратов на основе салициловой кислоты наиболее известны фенилсалицилат (салол), ацетилсалициловая кислота (аспирин).
Фенилсалицилат является эфиром салициловой кислоты и фенола:
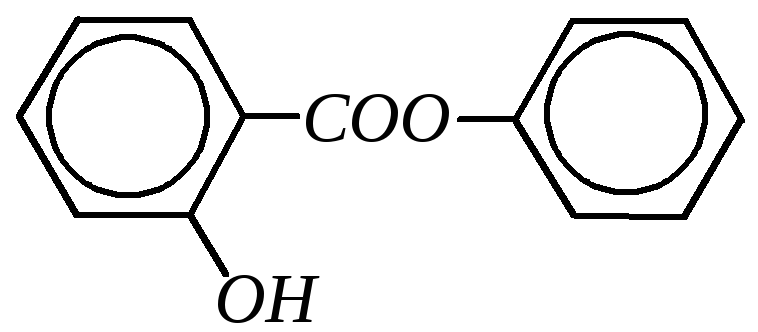
Он применяется в порошках и таблетках при заболеваниях кишечника. Действие препарата основано на том, что в слабощелочном содержимом кишечника фенилсалицилат гидролизуется на салициловую кислоту и фенол, которые угнетающе действуют на кишечную флору. Салициловая кислота и фенол частично выделяются из организма почками и могут оказывать дезинфицирующее действие в мочевых путях.
Действие ацетилсалициловой кислоты во многом сходно с действием на организм салицилата натрия, что понятно, так как ацетильное производное в желудочно-кишечном тракте гидролизуется:
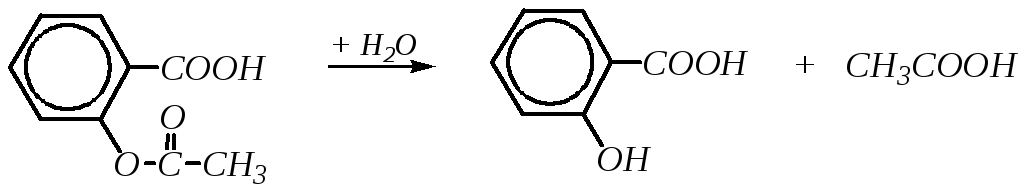
Ацетилсалициловую кислоту применяют внутрь при мигрени, а также как жаропонижающее и болеутоляющее средство. Она оказывает противовоспалительное действие.
При метаболическом расщеплении О-замещённых фенолов скоростьО-дезалкилирования снижается при увеличении длины неразветвлённой алкильной цепи, а электронодонорные группы около-углеродного атома увеличивают скорость реакции. Значительное влияние на скорость реакции оказывают и заместители в ароматическом цикле, однако не менее существенна и роль пространственных факторов.
п-Бензохинон, как и все хиноны, — сильный окислитель. Окислительно-восстановительные свойства системы хинон–гидрохинон играют важную роль в организме. По отношению к большинству органических субстратов эта система играет роль окислителя, участвуя в переносе электронов от субстрата к кислороду.
Анилин и многие ароматические амины довольно токсичны. Они являются нервными и кровяными ядами.
Анилин обладает жаропонижающим действием, однако не применяется в медицине вследствие своей токсичности.
Большое значение в химии лекарственных соединений имеют аминокислоты ароматического ряда, которые участвуют во многих жизненно важных процессах в качестве промежуточных веществ. Это п-аминобензойная кислота (витаминH1).
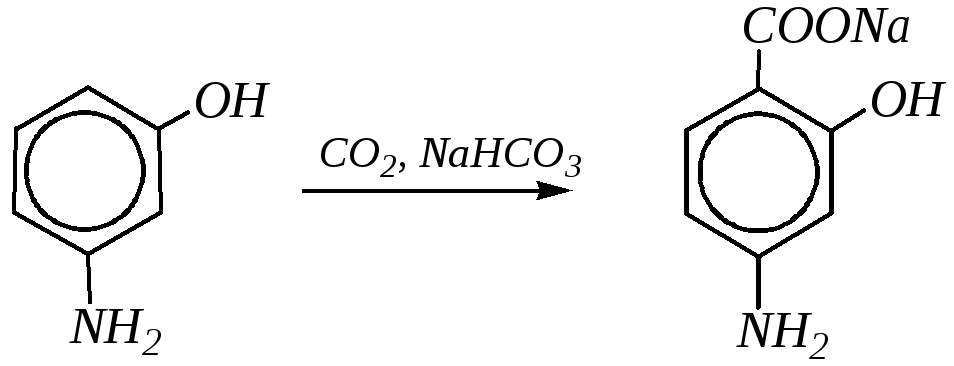
Если п-аминобензойная кислота является необходимым фактором для нормальной деятельности микроорганизмов, то п-аминосалициловая кислота, участвуя в обмене веществ, подавляет рост микроорганизмов. Таким образом, п-аминосалициловая кислота является антагонистом п-аминобензойной кислоты. п-Аминосалициловая кислота и её натриевая соль обладают бактериостатической активностью в отношении микобактерий туберкулёза и относятся к основным противотуберкулёзным препаратам. При приёме внутрь п-аминосалициловая кислота хорошо всасывается и проникает в сыворотку крови и ткани внутренних органов. п-Аминосалициловую кислоту и её соль часто применяют в комбинации с другими противотуберкулёзными препаратами.
Получают п-аминосалициловую кислоту из м-аминофенола карбоксилированием: