
- •Глава 10. Функциональные производные углеводородов ряда бензола
- •10.1. Общность строения и свойств монозамещённых бензолов
- •10.1.1. Электронные эффекты заместителей
- •10.1.2. Реакции электрофильного замещения
- •10.1.3. Реакции нуклеофильного замещения
- •10.2. Галогенарены
- •10.2.1. Классификация, номенклатура
- •10.2.2. Строение арилгалогенидов
- •10.2.3. Физические свойства
- •10.2.4. Химические свойства
- •10.2.5. Способы получения
- •10.2.6. Важнейшие представители
- •10.3. Ароматические сульфокислоты
- •10.3.1. Номенклатура
- •10.3.2. Строение
- •10.3.3. Физические и химические свойства
- •10.3.4. Способы получения
- •10.3.5. Производные сульфокислот
- •10.3.6. Медико-биологическое значение и Важнейшие представители
- •10.4. Ароматические нитросоединения
- •10.4.1. Строение нитробензола
- •10.4.2. Физические свойства
- •10.4.3. Химические свойства
- •10.4.4. Способы получения
- •10.4.5. Физиологическое действие и Важнейшие представители
- •10.5. Фенолы. Ароматические спирты. Хиноны
- •10.5.1. Классификация, номенклатура, изомерия фенолов и ароматических спиртов
- •10.5.2. Строение фенола и бензилового спирта
- •Ароматические амины и продукты неполного восстановления нитросоединений
- •10.6.1. Классификация, номенклатура, изомерия ароматических аминов
- •10.6.2. Строение анилина
- •10.6.3. Физические и химические свойства ароматических аминов
- •10.6.4. Способы получения ароматических аминов
- •10.6.5. Важнейшие представители ароматических аминов
- •10.6.6. Продукты неполного восстановления нитросоединений
- •10.7. Ароматические диазосоединения
- •10.7.1. Номенклатура диазосоединений
- •10.7.2. Механизм образования солей арендиазония и строение катиона бензолдиазония
- •10.7.3. Амфотерность диазосоединений
- •10.7.4. Реакции солей арендиазония
- •10.8. Ароматические альдегиды и кетоны
- •10.8.1. Изомерия, номенклатура
- •10.8.2. Строение бензальдегида
- •10.8.3. Физические и химические свойства
- •10.8.4. Способы получения
- •10.8.5. Важнейшие представители
- •10.9. Ароматические карбоновые кислоты и их производные
- •10.9.1. Классификация, номенклатура
- •10.9.2. Строение бензойной кислоты
- •10.9.3. Физические и химические свойства
- •10.9.4. Способы получения
- •10.9.5. Важнейшие представители
- •10.10. Физиологическая роль функциональных производных бензола
- •Вопросы и упражнения
10.6.4. Способы получения ароматических аминов
Существует несколько способов получения первичных, вторичных и третичных ароматических аминов. Бóльшая часть этих способов рассматривалась ранее в свойствах соответствующих классов соединений.
Первичные амины могут быть получены следующими способами.
Восстановление нитросоединений (гл. 10.4.3.3);
Аминирование арилгалогенидов (гл. 10.2.4.2). Этим же способом могут быть получены вторичные и третичные амины, если в качестве нуклеофильного агента вместо аммиака в реакции использовать амины (первичные или вторичные);
Перегруппировка амидов по Гофману (гл. 6.4.4.5).
Для получения вторичных и третичных аминов используются также:
Реакции алкилирования и арилирования первичных аминов (гл. 10.6.3.3);
Восстановление оснований Шиффа:
![]()
10.6.5. Важнейшие представители ароматических аминов
Анилин — бесцветная жидкость со своеобразным запахом; температура плавления 267К; малорастворим в воде.
В промышленности
анилин получают главным образом
каталитическим восстановлением
нитробензола водородом над
![]() или
или![]() .
.
Его применяют для получения полиуретанов, производных бензотиазола (ускорителей вулканизации), для синтеза антиоксидантов, красителей, лекарственных веществ.
N,N-Диметиланилин — бесцветная жидкость со своеобразным запахом; температура плавления 275.6 К, кипения — 466 К; малорастворим в воде.
Его получают алкилированием анилина метанолом в присутствии серной кислоты. Используют для синтеза красителей и взрывчатых веществ.
Сульфаниловая кислота (п-аминобензолсульфоновая кислота) — белое кристаллическое вещество; температура разложения 450 К; малорастворима в воде.
Её получают сульфированием анилина серной кислотой. Применяется в синтезе азокрасителей.
Важное практическое значение имеет амид сульфаниловой кислоты (сульфаниламид)
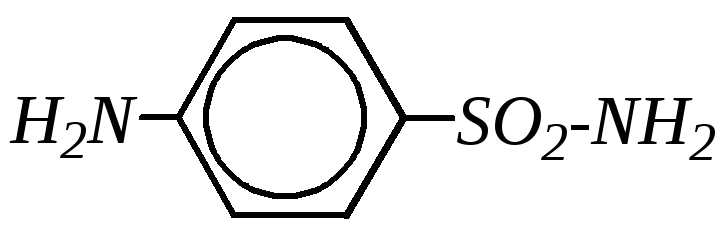 ,
,
производные которого используют в медицине как эффективные антибактериальные средства для лечения инфекционных заболеваний.
10.6.6. Продукты неполного восстановления нитросоединений
К производным ароматических аминов и одновременно к производным нитросоединений могут быть отнесены такие классы веществ, как нитрозоарены, N-арилгидроксиламин, гидразоарены, азо- и азоксисоединения, диазосоединения. Некоторые из этих соединений могут быть получены при неполном (частичном) восстановлении нитросоединений или при неполном окислении ариламинов, причём, возможно, только в качестве промежуточных продуктов, а для других существуют свои способы получения. Здесь приводится краткая характеристика этих веществ.
10.6.6.1. Нитрозобензол
Нитрозоарены — производные ароматических углеводородов, в которых атом водорода замещён нитрозогруппой. Номенклатура нитрозоаренов аналогична номенклатуре нитроаренов.
Нитрозобензол — бесцветное кристаллическое вещество, существующее в виде димера (цис- и транс-изомеры):

Мономер существует только в жидком состоянии и в парах, он окрашен в зелёный цвет.
Для нитрозобензола характерны многие реакции конденсации, он может вступать в реакции диенового синтеза в качестве диенофила:
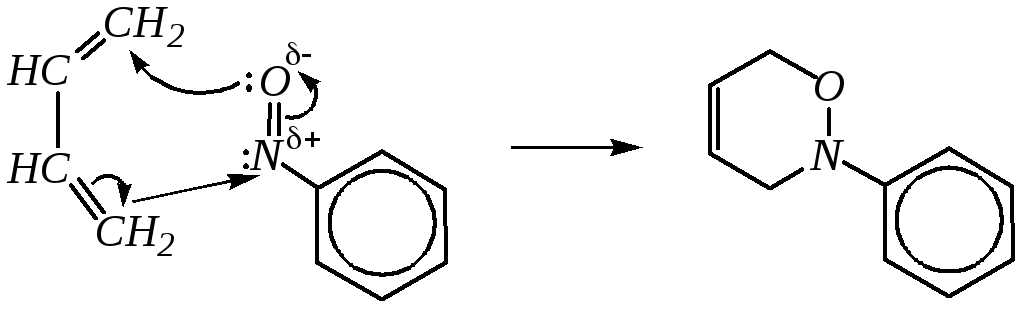
Получить чистые нитрозосоединения восстановлением нитросоединений по схеме
![]()
весьма трудно, поэтому используют реакции нитрозирования ароматических аминов (гл. 10.6.3.3) или фенолов (гл. 10.5.3.3). Нитрозобензол получают окислением фенилгидроксиламина хромовой кислотой:

10.6.6.2. Фенилгидроксиламин
N-Арилгидроксиламины обычно получаются как промежуточные соединения при восстановлении нитроаренов в нейтральной среде (гл. 10.4.3.3):
Ar-NO2
![]() Ar-NH-OH
Ar-NH-OH
N-Арилгидроксиламины, в частности фенилгидроксиламин, обладают как кислотными, так и основными свойствами, легко восстанавливаются дальше до ариламинов и гидразоаренов и окисляются до нитрозоаренов, дают реакцию «серебряного зеркала». В кислой среде фенилгидроксиламин перегруппировывается в п-аминофенол:
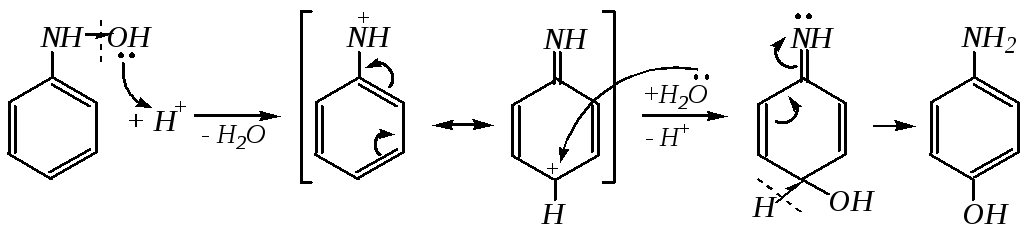
10.6.6.3. Гидразобензол
Гидразобензол — продукт восстановления нитробензола в щелочной среде (гл. 10.4.3.3). Это бесцветное кристаллическое вещество, легко окисляющееся кислородом воздуха. Окисление гидразобензола приводит к азобензолу, а при восстановлении образуется анилин:
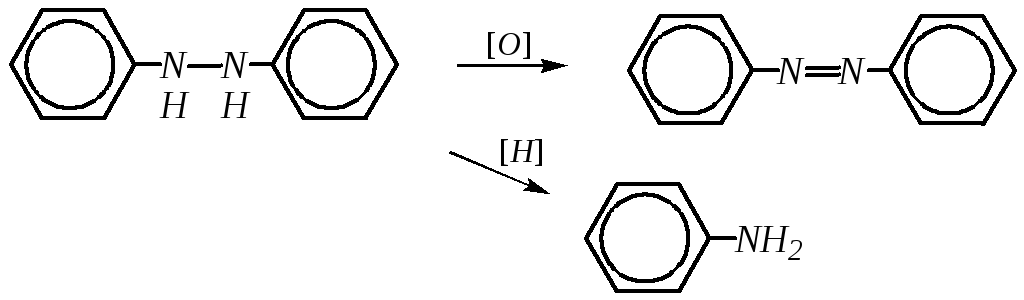
В кислой среде гидразобензол быстро подвергается бензидиновой перегруппировке:
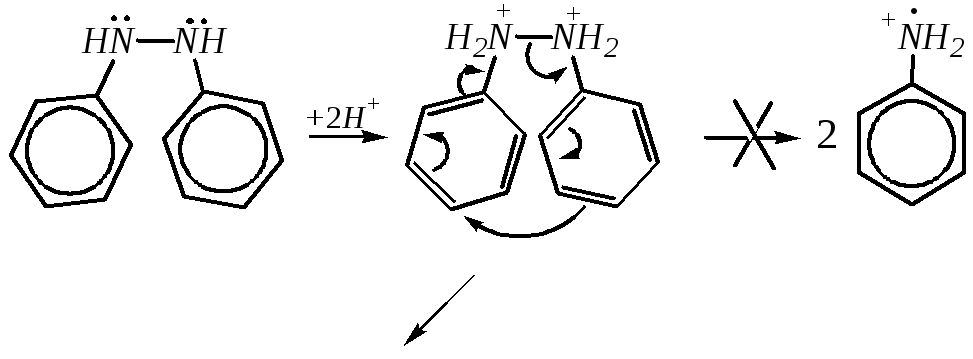
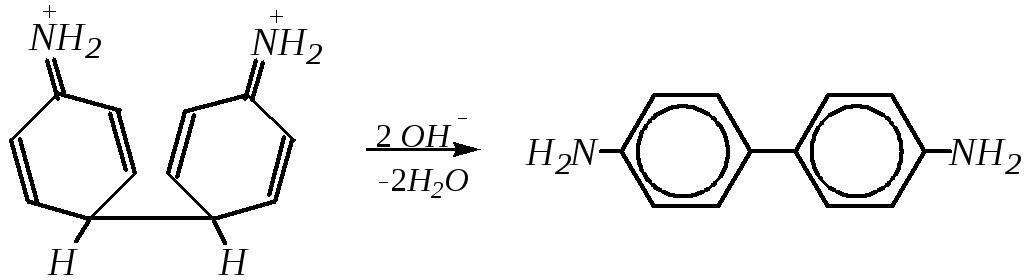
бензидин
Как установлено в настоящее время, в ходе протекания этой реакции катион-радикалы не образуются, а осуществляется перегруппировка в рамках внутримолекулярного синхронного элементарного процесса.
В общем случае, для гидразоаренов, если заняты п-положения в одном или обоих бензольных кольцах, протекает семидиновая (неполная) перегруппировка:
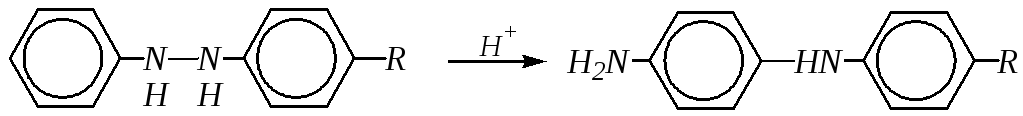
или
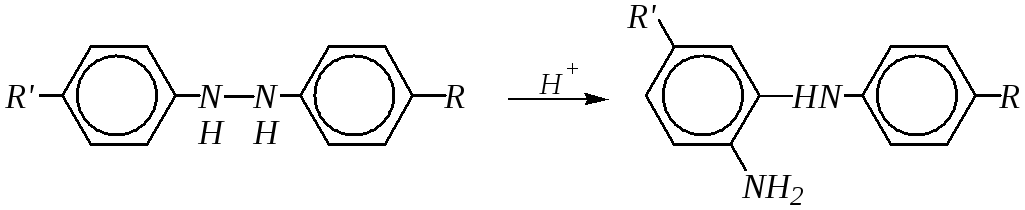
10.6.6.4. Азобензол и азоксибензол
Азобензол существует в виде двух геометрических изомеров:
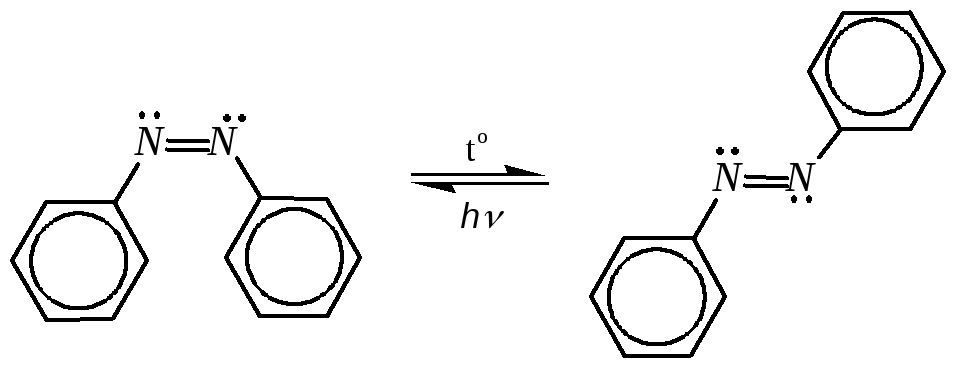
Цис-азобензол непланарен из-за пространственных затруднений (отталкивание орто-водородных атомов), поэтому он неустойчив и при нагревании легко превращается в транс-изомер. При освещении ультрафиолетом транс-изомер частично превращается в цис-изомер.
Азобензол является очень слабым основанием, но введение электронодонорных заместителей в одно из ароматических колец резко увеличивает основность -атома азота:
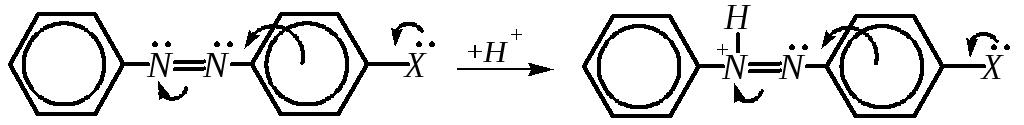
Азобензол может быть получен восстановлением нитробензола в щелочной среде. В общем случае азоарены получают разными способами, в частности, одним из распространённых способов получения азосоединений является реакция азосочетания, которая рассмотрена далее (гл. 10.7.4.3); там же будут рассмотрены и некоторые особенности номенклатуры азосоединений, связанной с этим способом получения.
Азоксибензол — продукт окисления азобензола и также может быть получен восстановлением нитробензола метилатом натрия:
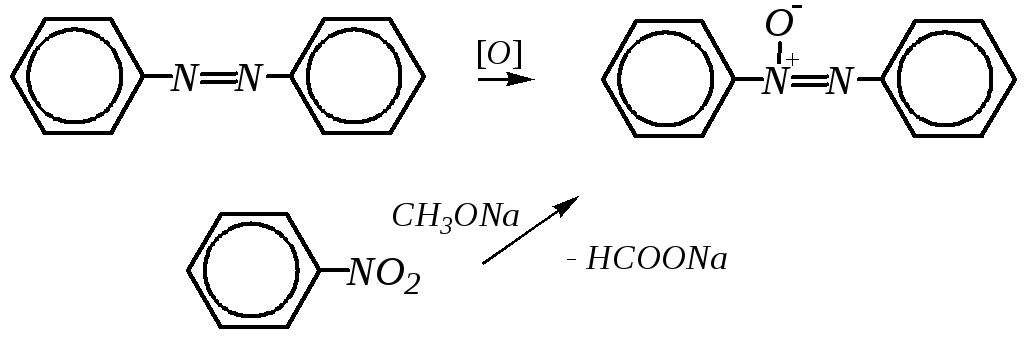
Производные азоксибензола проявляют жидкокристаллические свойства. Они обладают свойствами жидкости (текучестью) и некоторыми свойствами твёрдых кристаллов. При незначительном изменении температуры жидкие кристаллы могут изменять цвет. Это свойство используется в жидкокристаллической термографии.
