
- •Глава 10. Функциональные производные углеводородов ряда бензола
- •10.1. Общность строения и свойств монозамещённых бензолов
- •10.1.1. Электронные эффекты заместителей
- •10.1.2. Реакции электрофильного замещения
- •10.1.3. Реакции нуклеофильного замещения
- •10.2. Галогенарены
- •10.2.1. Классификация, номенклатура
- •10.2.2. Строение арилгалогенидов
- •10.2.3. Физические свойства
- •10.2.4. Химические свойства
- •10.2.5. Способы получения
- •10.2.6. Важнейшие представители
- •10.3. Ароматические сульфокислоты
- •10.3.1. Номенклатура
- •10.3.2. Строение
- •10.3.3. Физические и химические свойства
- •10.3.4. Способы получения
- •10.3.5. Производные сульфокислот
- •10.3.6. Медико-биологическое значение и Важнейшие представители
- •10.4. Ароматические нитросоединения
- •10.4.1. Строение нитробензола
- •10.4.2. Физические свойства
- •10.4.3. Химические свойства
- •10.4.4. Способы получения
- •10.4.5. Физиологическое действие и Важнейшие представители
- •10.5. Фенолы. Ароматические спирты. Хиноны
- •10.5.1. Классификация, номенклатура, изомерия фенолов и ароматических спиртов
- •10.5.2. Строение фенола и бензилового спирта
- •Ароматические амины и продукты неполного восстановления нитросоединений
- •10.6.1. Классификация, номенклатура, изомерия ароматических аминов
- •10.6.2. Строение анилина
- •10.6.3. Физические и химические свойства ароматических аминов
- •10.6.4. Способы получения ароматических аминов
- •10.6.5. Важнейшие представители ароматических аминов
- •10.6.6. Продукты неполного восстановления нитросоединений
- •10.7. Ароматические диазосоединения
- •10.7.1. Номенклатура диазосоединений
- •10.7.2. Механизм образования солей арендиазония и строение катиона бензолдиазония
- •10.7.3. Амфотерность диазосоединений
- •10.7.4. Реакции солей арендиазония
- •10.8. Ароматические альдегиды и кетоны
- •10.8.1. Изомерия, номенклатура
- •10.8.2. Строение бензальдегида
- •10.8.3. Физические и химические свойства
- •10.8.4. Способы получения
- •10.8.5. Важнейшие представители
- •10.9. Ароматические карбоновые кислоты и их производные
- •10.9.1. Классификация, номенклатура
- •10.9.2. Строение бензойной кислоты
- •10.9.3. Физические и химические свойства
- •10.9.4. Способы получения
- •10.9.5. Важнейшие представители
- •10.10. Физиологическая роль функциональных производных бензола
- •Вопросы и упражнения
10.3.2. Строение
А том
серы в сульфогруппе образует четыре-
и две -связи.
-Связи
образованы sp3-гибридными
орбиталями, и сера, таким образом, имеет
тетраэдрическое строение. -Связи
образованы за счёт d-орбиталей
атома серы.
том
серы в сульфогруппе образует четыре-
и две -связи.
-Связи
образованы sp3-гибридными
орбиталями, и сера, таким образом, имеет
тетраэдрическое строение. -Связи
образованы за счёт d-орбиталей
атома серы.
Сульфогруппа по отношению к бензольному кольцу оказывает –I- и –M-эффекты. Сильный электроноакцепторный индуктивный эффект вызван влиянием электроотрицательных атомов кислорода, с которыми связана сера. Мезомерный эффект должен быть обусловлен сопряжением -связи S=O с -электронной системой ароматического кольца. Но такое сопряжение невозможно, так как d-орбитали атома серы, участвующие в образовании -связей, непараллельны p-орбиталям атома углерода. Сопряжение возможно при перекрывании p-орбиталей атома углерода с вакантными d-орбиталями атома серы.
Результатом проявления сульфогруппой –I- и –M-эффектов является сильное понижение электронной плотности ароматического кольца, особенно в о- и п-положениях. Распределение электронов в системе вследствие проявления сульфогруппой –M-эффекта можно описать следующими граничными структурами:
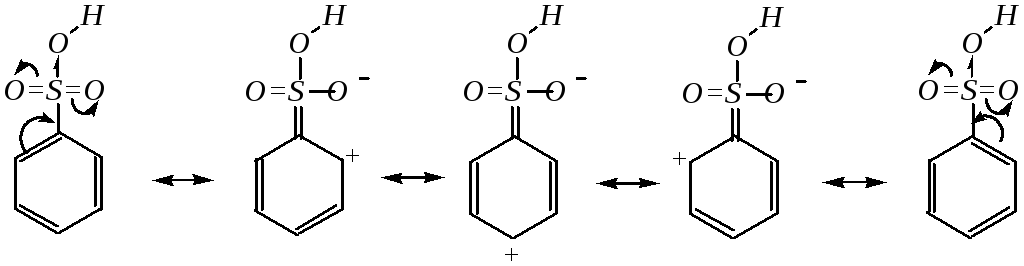
Поэтому реакционная способность аренсульфокислот по отношению к электрофильным реагентам в значительной степени понижена по сравнению с незамещённым бензолом, причём вступление электрофила в молекулу сульфокислоты возможно только в мета-положение, где влияние мезомерного эффекта не ощущается.
Кроме того, присутствие у серы электроотрицательных атомов кислорода, связанных с ней кратными связями, сильно повышает кислотные свойства гидроксильной группы.
10.3.3. Физические и химические свойства
Аренсульфоновые кислоты — бесцветные кристаллические гигроскопичные вещества, растворимые в воде. Большинство производных сульфокислот являются также кристаллическими веществами (соли, амиды, эфиры), в воде растворимы амиды и хорошо растворимы соли (в том числе кальциевые и магниевые).
Химические свойства ароматических сульфокислот весьма разнообразны. Сульфогруппа — это сложная функциональная группа, поэтому возможны и реакции, протекающие по бензольному кольцу, и реакции замещения сульфогруппы, и реакции с участием самой сульфогруппы.
10.3.3.1. Электрофильное замещение атома водорода в ароматическом кольце
Аренсульфокислотам, как и любым ароматическим соединениям, должны быть свойственны реакции электрофильного замещения атома водорода в бензольном кольце. Однако за счёт –I- и –M-эффектов электронная плотность на бензольном кольце сульфокислот сильно понижена по сравнению с незамещённым бензолом, и поэтому электрофильные реакции протекают, как правило, только с сильными электрофилами и в жёстких условиях. Наиболее значительно электронная плотность понижена во- ип-положениях (из-за действия акцепторного мезомерного эффекта). Поэтому электрофильное замещение направляется вм-положение к сульфогруппе. Например:
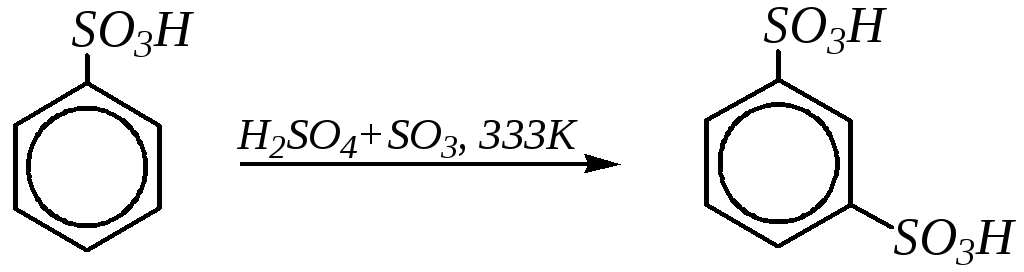
С другой стороны, мета-ориентирующее действие сульфогруппы может быть объяснено и динамическим подходом, то есть сравнением устойчивости образующихся-комплексов (гл. 10.1.2).
10.3.3.2. Электрофильное замещение сульфогруппы
Взаимодействие с электрофилами может привести не только к замещению атома водорода в бензольном кольце, но и самой сульфогруппы. Наиболее важными такими реакциями являются замещение её на водород, на нитрогруппу и на галоген.
Замещение сульфогруппы на водород — это реакция гидролиза аренсульфокислот (или десульфирования), общую схему которой можно представить следующим образом:
Ar-SO3Н + Н-OH Ar-H + H2SО4
Реакцию проводят при нагревании сульфокислот с водными растворами серной или соляной кислоты (обычно используют 60—70%-ю H2SO4при температуре около 400К). Сульфокислоты в присутствии воды диссоциированы, и в реакцию с электрофилом вступает, скорее всего, не молекула, а анион аренсульфокислоты. Электрофильной частицей является катион водорода, а отщепление сульфонатной группы происходит при участии молекул воды:

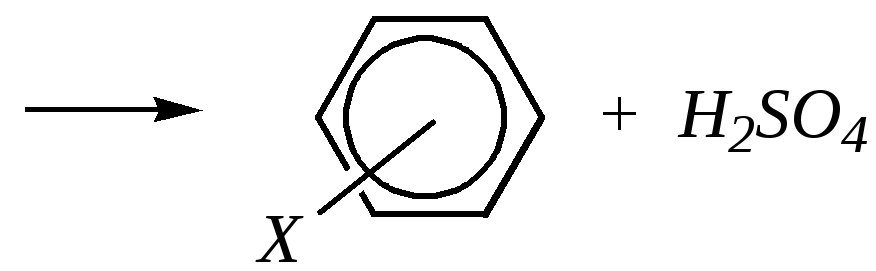
Замещение на нитрогруппу и на галоген происходит при электрофильном нитровании или галогенировании ароматических субстратов, если в бензольном кольце помимо сульфогруппы имеется сильный электронодонор (X). Тогда первоначально произойдёт замещение атомов водорода на нитрогруппы (или на атомы галогена), а затем может заместиться и сульфогруппа:
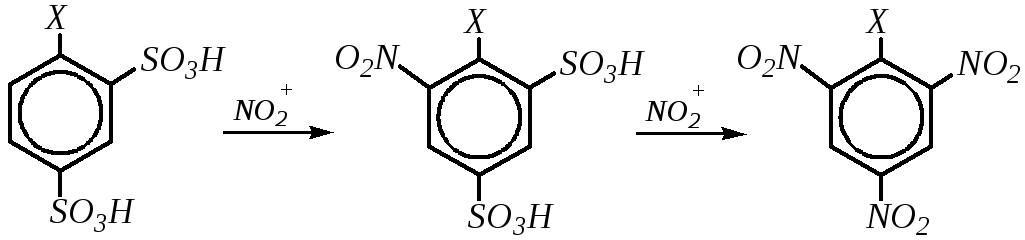
При нитровании отщепление сульфогруппы будет происходить при участии молекул азотной кислоты:
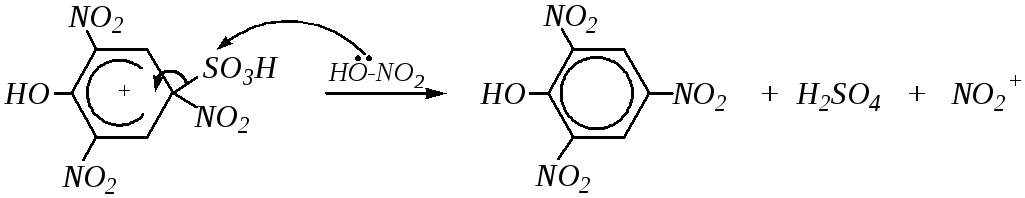 ,
,
а при бромировании — под действием бромид-ионов:

10.3.3.3. Нуклеофильное замещение сульфогруппы в ароматическом кольце
Сульфогруппа в бензольном кольце является сильным электроноакцептором, в том числе и за счёт индуктивного эффекта. Поэтому в молекулах аренсульфокислот связь C–S сильно полярна, и на атоме углерода, связанном с серой, имеется значительный частичный положительный заряд. Это делает возможным нуклеофильную атаку по данному атому углерода и, как следствие, протекание реакции нуклеофильного замещения сульфогруппы по механизмуSN2ароманалогично рассмотренному в главе 10.1.3.
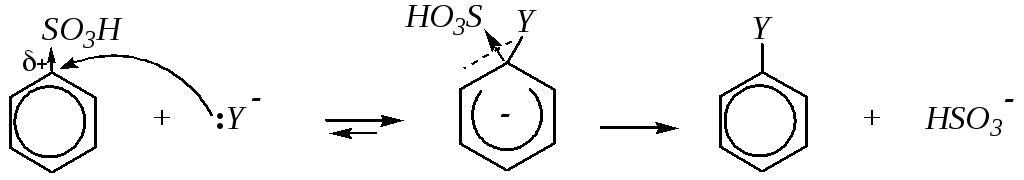
Реакцию проводят при сплавлении сульфокислоты с реагентом.
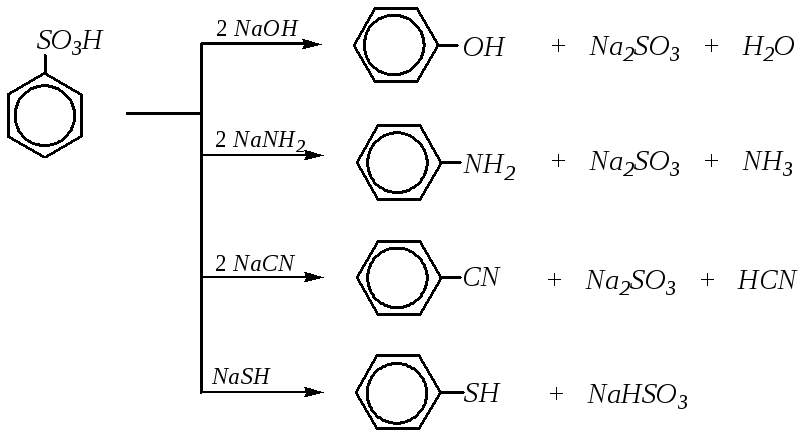
Наиболее распространённым здесь является сплавление со щёлочью (называемое щелочным плавлением) при температуре 530—570 К. В общем случае, при использовании аренсульфоновых кислот Ar-SO3H температура может достигать 610 К. Однако активированная сульфогруппа обменивается на гидроксильную группу в более мягких условиях.
При использовании других нуклеофильных реагентов может быть осуществлено замещение и на амино-, циано-, меркаптогруппы. Эта реакция может применяться для получения разнообразных функциональных производных аренов, но наиболее широкое применение этот способ нашёл для получения резорцина:
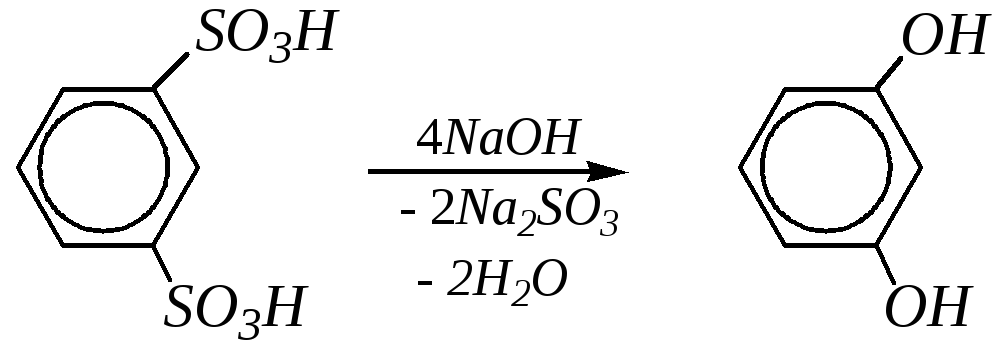
резорцин
10.3.3.4. Кислотные свойства
Аренсульфоновые кислоты — очень сильные кислоты, в водных растворах они полностью диссоциированы:
Ar-SO3Н + Н2O Ar-SO3¯ + H3О+
и, как типичные кислоты, образуют соли, например:
2Ar-SO3Н + Са(ОН)2 (Ar-SO3)2Са + 2H2О
аренсульфонат кальция
Кислотные свойства для большинства этих соединений выражены сильнее, чем для серной кислоты. Причиной столь высокой кислотности аренсульфокислот является большая устойчивость аренсульфонатного иона, который образуется при диссоциации кислоты (сравните с гидросульфат-ионом):
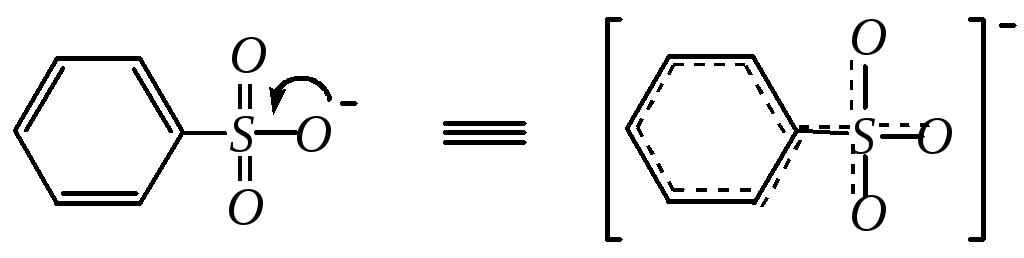
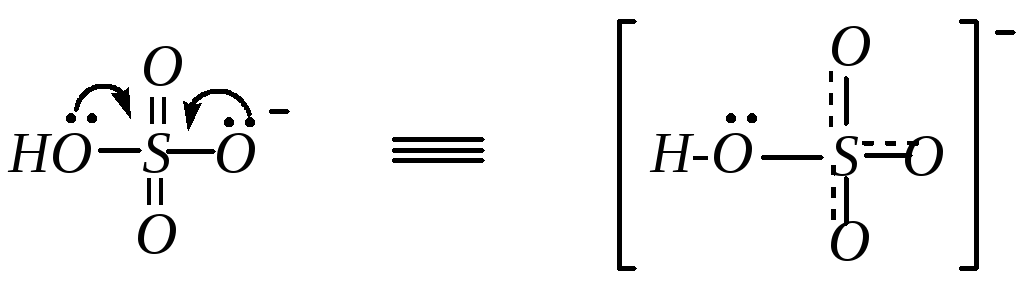
В анионе бензолсульфокислоты в делокализации отрицательного заряда принимает участие -электронная система ароматического кольца.
Электроноакцепторные заместители в ароматическом кольце бензолсульфокислоты увеличивают кислотные свойства за счёт более полной делокализации отрицательного заряда в анионе; электронодонорные заместители, наоборот, уменьшают кислотные свойства, так как в этом случае их электронный эффект препятствует делокализации заряда аниона:
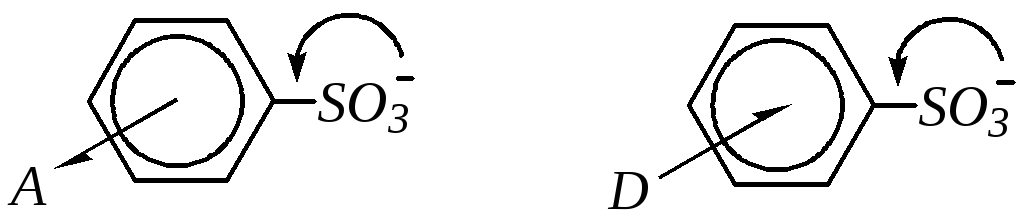
10.3.3.5. Нуклеофильное замещение в сульфогруппе
Нуклеофильное замещение в сульфогруппе — это замещение гидроксогруппы, и для него можно было бы привести такую схему:
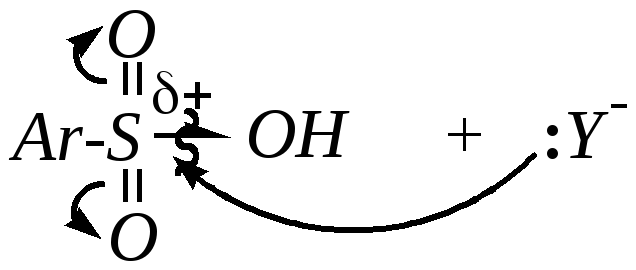
Однако аренсульфокислоты не вступают в такие реакции ни со спиртами, ни с аммиаком и аминами (в отличие от карбоновых кислот).
![]()
![]()
Причинами такого отличия реакционной способности сульфокислот от карбоновых кислот являются: 1) стерический фактор — невозможность подхода нуклеофильных частиц к тетраэдрическому атому серы, окружённому электроотрицательными атомами кислорода; 2) высокие кислотные свойства сульфокислот, за счёт чего легко происходит отрыв протона от сульфогруппы и присоединение его к нуклеофильной частице, но при этом она дезактивируется, и дальнейшая нуклеофильная атака становится невозможной.
Непосредственно из сульфокислот могут быть получены только галогенангидриды (сульфохлориды):
Ar-SO2-OH
![]() Ar-SO2-Cl
Ar-SO2-Cl
Реакция с участием пентахлорида фосфора, например, начинается с атаки атомом кислорода сульфогруппы по атому фосфора катиона [PCl4]+ (вследствие димеризации пентахлорида фосфора его можно представить в виде ионной пары [PCl4]+ [PCl6]¯):
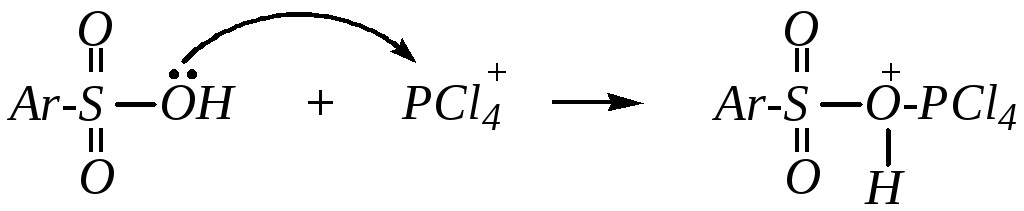
Дальнейшее превращение (при участии аниона [PCl6]¯) протекает по механизму, близкому к SN1:
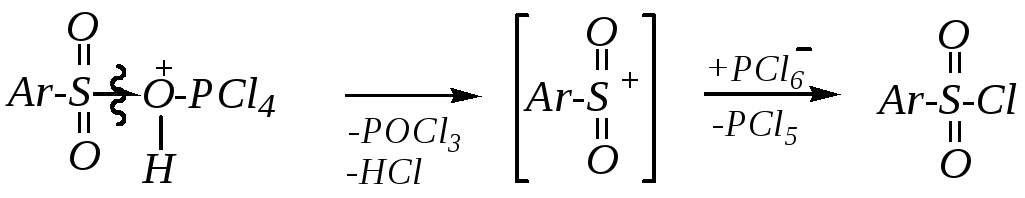
10.3.3.6. Реакции восстановления
Под действием сильных восстановителей сульфогруппа в ароматическом кольце может восстанавливаться до меркаптогруппы. При этом образуются тиофенолы:
Ar-SO3Н
![]() Ar-SH
Ar-SH
Одним из таких восстановителей может служить тетрагидроалюминат лития Li[AlН4]. Некоторые производные ароматических сульфокислот также могут быть восстановлены до арентиолов, например, аренсульфохлориды — под действием цинка в серной кислоте или водородом на металлических катализаторах:
Ar-SO2Сl
![]() Ar-SH
Ar-SH
