
Акушерство для студентов / Запоражан том 1
.pdf
Розділ 5. Репродуктивна генетика...
Тератогенну дію має непрямий антикоагулянт варфарин, на відміну від прямого антикоагулянту гепарину. Антигіпертензивні препарати — інгібітори ангіотензин? конвертуючого ензиму (АСЕ) — спричинюють затримку росту, ниркові порушення, маловоддя і внутрішньоутробну смерть плода.
Такі препарати, як пропілтіоурацил і йодид калію провокують зоб і розумову відсталість у плода, стрептоміцин — глухоту, сульфонаміди — жовтяницю, тетра? циклін — аномалії кісток і зубів плода, амфетамін — аномалії ротової щілини і сер цево судинної системи, квінін — глухоту. Аспірин у великих дозах також є тератоге ном.
Наркотичні препарати — діетиламід лізергінової кислоти (LSD), фенциклідин, або янгольський порошок (PCP), маріхуана, алкоголь, кокаїн також можуть бути тератогенами. Кокаїн спричинює природжені вади внаслідок судинозвужуючого ефек ту, що призводить до гіпоксії. Алкоголь у великих дозах спричинює низку аномалій
— «алкогольний синдром плода», може бути причиною алкогольного порушення нервового розвитку (ARND). Алкоголь є основною причиною розумової відсталості. Вживання тютюну під час вагітності не спричинює аномалій розвитку, але може сприяти передчасним пологам, низькій масі тіла при народженні та порушенням поведінки в подальшому житті. Вітамін А (пороговий рівень тератогенності 25 000 МО) спричинює А вітамінну ембріопатію, яка характеризується різноманітними ано маліями (табл. 5.4).
Гормони. Андрогенні агенти (синтетичні прогестини) раніше використовувалися для профілактики мимовільних викиднів. Прогестини етистерон і норетистерон ма ють значну андрогенну активність й інколи призводять до маскулінізації геніталій плодів жіночої статі — збільшення клітора, злиття губно мошонкових складок різно го ступеня вираженості.
Ендокринні дизруптори (дезінтегратори) — екзогенні чинники, які втручаються в нормальну регуляторну дію гормонів, що контролюють процеси розвитку. Найчас тіше ці агенти втручаються у дію естрогенів завдяки дії рецепторів і спричинюють аномалії розвитку ЦНС та репродуктивного тракту. Раніше при використанні ді етилстильбестролу (для попередження мимовільних викиднів) у народжених дівча ток зростала частота вад розвитку матки, маткових труб, верхньої частини піхви і раку піхви, у хлопчиків — природжених вад яєчок і аномалій сперматозоїдів.
Вивчається ембріотоксичність естрогенів навколишнього середовища, які містять ся у пестицидах та промислових речовинах, а також фітоестрогенів.
Оральні контрацептиви. Естроген гестагенні оральні контрацептиви мають низь кий тератогенний потенціал. При підозрі на вагітність слід припинити застосування цих препаратів.
Кортизон. В експерименті ін’єкції кортизону спричинювали щілини піднебіння у кролів і мишей, але у людини тератогенні властивості кортизону не доведені.
Материнські захворювання
Цукровий діабет. Ризик природжених аномалій розвитку у потомства матерів із цукровим діабетом в 3–4 рази вищий, ніж у здорових і охоплює 80 % новонародже них у матерів із тривалим недостатньо компенсованим діабетом. Вади розвитку вклю чають таку тяжку аномалію, як каудальний дисгенез (сиреномелія).
Доведено, що інсулін не має тератогенної дії, а навпаки, лікування інсуліном з метою компенсації вуглеводного обміну ще до запліднення сприяє зменшенню ри зику патології потомства. Але гіпоглікемія матері є тератогенним фактором. Навіть нетривале зниження рівня глюкози в крові під час органогенезу дає тератогенний ефект. Оральні гіпоглікемічні препарати (похідні сульфонілсечовини і бігуаніди) вважаються тератогенними, хоча останні дослідження свідчать про відсутність сер йозного ризику для плода.
169

Акушерство і гінекологія. Том 1
Фенілкетонурія. Матері з фенілкетонурією, які мають дефіцит ферменту феніл аланінг гідроксилази, що призводить до підвищення вмісту фенілаланіну у сиро ватці крові, мають підвищений ризик народження дітей з розумовою відсталістю, мікроцефалією і вадами серця. Дотримання дієти з низьким рівнем фенілаланіну перед зачаттям зменшує ризик аномалій до фонового рівня.
Нестача харчових компонентів. Доведеним фактором є те, що дефіцит йоду спри чинює ендемічний кретинізм. Доказів про те, що дефіцит харчових компонентів і вітамінів є тератогеном, немає, хоча недостатнє харчування матері є фактором ризи ку передчасних пологів і низької маси тіла плода при народженні.
Гіпоксія. Гіпоксія спричинює природжені вади у багатьох видів експерименталь них тварин. У людини таких даних не зареєстровано, хоча доведено зменшення маси тіла дітей, народжених жінками, які мешкають на значній висоті над рівнем моря.
Важкі метали. Вживання вагітною харчових продуктів (зерно, м’ясо, риба), за бруднених ртуттю (у складі фунгіцидів або промислових відходів), призводить до множинних неврологічних вад у плода, які нагадують церебральний параліч. Сви нець призводить до збільшення частоти мимовільних викиднів, затримки росту і неврологічних розладів.
Тератогенез, пов’язаний з чоловічим фактором. Вплив хімічних і фізичних чин ників, таких як етилнітрозосечовина і радіація, може спричинювати мутації в чоловічих статевих клітинах. Існує зв’язок між тератогенним впливом на батька (професійним чи оточуючого середовища) ртуті, свинцю, хімічних розчинників, алкоголю, тютюну і мимовільними абортами, низькою масою тіла плода при на родженні та природженими вадами. Похилий вік батька є фактором ризику де фектів кінцівок і нервової трубки, а також синдрому Дауна у плода. Юний вік батька (до 20 років) також є фактором ризику зачаття дітей з аномаліями розвит ку. Механізми токсичного впливу включають: 1) передачу токсичних агентів че рез сперму; 2) забруднення житла хімічними речовинами; 3) мутації статевих клітин і геномний імпринтинг (відносне змішування материнських і батьківських генів).
Клінічні кореляції
Багато випадків природжених вад можна попередити. Так, вживання йодованої солі запобігає розвитку кретинізму, що проявляється розумовою відсталістю і де формаціями кісток. Суворий метаболічний контроль за пацієнтками з цукровим діа бетом і фенілкетонурією дозволяє зменшити ризик природжених вад розвитку. До давання у харчовий раціон фолатів до запліднення і протягом вагітності зменшує ризик розвитку дефектів нервової трубки (щілина хребта, аненцефалія).
Критичні періоди розвитку ембріона і плода
Отже, у розвитку ембріона і плода можна виділити три основні періоди:
1)перший період, преембріональний, який триває після запліднення протягом першого тижня вагітності. Критичними моментами цього періоду є запліднення і імплантація. Дія несприятливих факторів у цей період спричинює ембріотоксичний ефект або відсутність будь якого впливу, закон «все або нічого»;
2)другий період — ембріональний, триває з 3 до 8 го тижня після запліднення (протягом 5–10 тиж гестаційного віку) (період органогенезу). Це найбільш чутливий
інебезпечний період (критичний) для дії агресивних факторів зовнішнього се редовища. Дія несприятливих факторів у цей період спричинює тератогенний ефект;
3)третій, фетальний (плодовий) період, триває з 9 го тижня вагітності до наро дження дитини. Під час плодового періоду агресивні чинники зазвичай не спричи
170

Розділ 5. Репродуктивна генетика...
нюють значних вад розвитку, але можуть бути причиною розумових порушень і ано? мальних поведінкових реакцій у постнатальному періоді.
Плодові оболонки і плацента
Трофобласт
На початку другого місяця ембріогенезу трофобласт має велику кількість вто ринних і третинних ворсинок, які надають йому променистого вигляду. Ворсинки занурені у мезодерму хоріонічної пластинки, а на периферії прикріплюються до ма теринської децидуальної оболонки за допомогою зовнішнього шару цитотрофоблас? та. Поверхня ворсинки вкрита синцитієм, що лежить на одному шарі клітин цито трофобласта, який вкриває серцевину ворсинки, утворену васкуляризованою мезо дермою. Капілярна система серцевини стовбурових ворсинок вступає в контакт із капілярами хоріонічної пластинки та сполучної ніжки, даючи початок позазарод ковій судинній системі.
Протягом наступних місяців від стовбурових ворсинок відростають численні дрібні гілочки в оточуючі лакунарні та міжворсинчасті простори. Спочатку ці вор синки примітивні, але до початку четвертого місяця клітини цитотофобласта і деякі сполучнотканинні клітини зникають. Таким чином, материнську і плодову судинну систему розмежовують лише синцитій і ендотеліальна стінка кровоносних судин ворсинок хоріона. Синцитій може потоншуватись, і великі його сегменти з кількома ядрами відриваються, потрапляють у міжворсинчасті кров’яні лакуни. Такі уламки
— синцитіальні вузли — потрапляють у материнську судинну систему і звичайно дегенерують, не спричинюючи жодних симптомів. Зникнення клітин цитотрофо бласта починається від менших ворсинок і переходить на більші. Хоча деякі елемен ти цитотрофобласта залишаються у великих ворсинках, вони не беруть участі в обміні речовин між материнською і плодовою системами кровообігу.
Ворсинчастий хоріон і основна децидуальна
(відпадна) оболонка
У перші тижні розвитку ворсинки вкривають усю поверхню хоріона. Протягом вагітності ворсинки на ембріональному полюсі продовжують рости і поширювати ся, даючи початок ворсинчастому хоріону. Ворсинки на протилежному полюсі деге нерують, і до третього місяця ембріогенезу утворюється гладкий хоріон. Різниця у будові ембріонального і протиембріонального полюсів хоріона позначається також і на структурі відпадної (децидуальної) оболонки, яка є функціональним шаром ен дометрія і відторгнення якої відбувається при пологах (рис. 5.10). Частина відпад ної оболонки над ворсинчастим хоріоном — основна відпадна оболонка (базальна децидуальна оболонка, decidua basalis) складається з компактного шару великих де цидуальних клітин, які наповнені ліпідами і глікогеном. Децидуальний шар над протиембріональним полюсом має назву сумкової відпадної оболонки (капсулярної децидуальної оболонки, decidua capsularis). При збільшенні розмірів хоріонічного міхура цей шар розтягується і дегенерує. У зв’язку з цим гладкий хоріон вступає в контакт зі стінкою матки і утворюється пристінкова відпадна оболонка (парієтальна децидуальна оболонка, decidua parietalis), з якою він зливається, облітеруючи по рожнину матки. Отже, єдиною частиною хоріона, яка бере участь у процесі обміну
171
Акушерство і гінекологія. Том 1
7
8
|
5 |
4 |
6 |
3 |
9 |
|
10 |
2 |
|
11 |
|
|
|
|
1 |
12 |
|
|
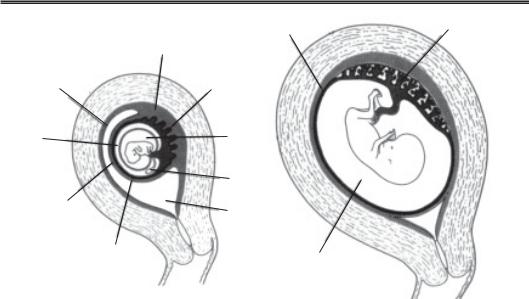
Рис. 5.10. Співвідношення плодових оболонок і стінки матки:
1 — гладкий хоріон; 2 — капсулярна децидуальна оболонка; 3 — хоріонічна по рожнина; 4 — парієтальна децидуальна оболонка; 5 — базальна децидуальна обо лонка; 6 — злиття парієтальної децидуальної оболонки, гладкого хоріона й амніо на; 7 — плацента; 8 — ворсинчастий хоріон; 9 —амніотична порожнина; 10 — жовт ковий мішок; 11 — порожнина матки; 12 — амніотична порожнина
речовин, є ворсинчастий хоріон, що разом із відпадною оболонкою утворює плацен ту. При злитті амніона і хоріона утворюється амніохоріальна оболонка, яка обліте рує хоріонічну порожнину. Саме ця оболонка і розривається під час пологів (при відходженні навколоплідних вод).
Структура плаценти
На початку четвертого місяця розвитку плацента є сформованою і складається з двох частин: плодової частини, утвореної ворсинчастим хоріоном, і материнської частини, утвореної основною відпадною оболонкою. З боку плода плацента обме жена хоріонічною пластинкою, а з материнського боку — основною відпадною обо лонкою, децидуальна пластинка якої найглибше вростає в плаценту. У ділянці з’єднання трофобласт і децидуальні клітини змішуються. Ця ділянка характеризуєть ся наявністю децидуальних і гігантських синцитіальних клітин і багата на міжклітин ну аморфну речовину. До цього часу більшість клітин цитотрофобласта дегенерує. Між хоріонічною і децидуальною пластинками розташовані заповнені материнсь кою кров’ю міжворсинчасті простори. Вони розвиваються з лакун синцитіотрофоб ласта і вистелені синцитієм ембріонального походження. Гілки ворсинок знаходять ся у міжворсинчастих кров’яних лакунах.
Протягом 4–5 міс відпадна оболонка утворює численні перегородки — дециду? альні септи, які виступають у міжворсинчасті простори, але не досягають хоріоніч ної пластинки. Такі септи мають серцевину з материнської тканини. Але їхня поверх
172

Розділ 5. Репродуктивна генетика...
ня вкрита шаром синцитію, який відмежовує материнську кров у міжворсинчастих лакунах від плодової тканини ворсинок. Завдяки розвитку септ плацента розділяється на відділи — котиледони. Внаслідок того, що децидуальні септи не досягають хоріо нічної пластинки, міжворсинчасті простори різних котиледонів зберігають між со бою контакт.
Разом з ростом плода і розширенням матки має місце ріст плаценти. Збільшення площі поверхні плаценти відбувається відповідно до збільшення матки, наприкінці вагітності плацента займає близько 15–30 % внутрішньої поверхні матки. Зростан ня товщини плаценти зумовлене розгалуженням існуючих ворсинок, а не їх подаль шою пенетрацією в материнські тканини.
Плацента при доношеній вагітності
Наприкінці вагітності плацента має дископодібну форму, діаметром 15–25 см, товщиною близько 3 см, масою 500–600 г. Під час третього періоду пологів вона відривається від стінки матки і приблизно через 30 хв після народження дитини виштовхується з порожнини матки. Якщо розглянути плаценту після народження, з материнського боку можна розрізнити 15–20 злегка виступаючих ділянок — котиле донів, укритих тонким шаром основної відпадної оболонки. Борозни між котиледо нами утворені децидуальними септами. Значна частина децидуальних оболонок тим часово залишається в матці і виштовхується з подальшою матковою кровотечею.
Плодова поверхня плаценти повністю |
|
|
вкрита хоріонічною пластинкою. Чис |
|
|
ленні великі артерії і вени (хоріонічні |
|
|
судини) сходяться до пупкового канати |
|
|
ка. Хоріон вкритий амніоном. Прикріп |
5 |
|
лення пупкового канатика є переважно |
6 |
|
ексцентричним, може мати місце крайо |
||
ве і оболонкове прикріплення (рис. 5.11). |
|
|
Зміни плаценти наприкінці вагітності |
4 |
|
обумовлені зменшенням обміну між дво |
||
7 |
||
ма системами кровообігу і включають: |
||
1) збільшення кількості фіброзної ткани |
3 |
|
ни у ворсинках; 2) потовщення базаль |
|
|
них мембран у капілярах плода; 3) обліте |
8 |
|
рацію малих капілярів ворсинок; |
||
2 |
||
4) відкладання фібриноїду на поверхні |
|
|
ворсинок у зоні з’єднання і на хоріонічній |
9 |
|
пластинці. Посилене утворення фібриної |
|
|
ду може зумовити інфаркти лакун і ко |
|
тиледонів плаценти (котиледон набуває |
1 |
|
білого кольору). |
||
|
Клінічні кореляції
Аномалії плаценти. У нормі плацента імплантується на передній або задній стінці матки. Під передлежанням плацен ти (placenta previa) розуміють її аномаль ну імплантацію над внутрішнім зівом
Рис. 5.11. Плацента наприкінці вагітності: 1 — судини ендометрія; 2 — ворсинки хорі она; 3 — базальна децидуальна оболонка; 4 — плацентарна перетинка; 5 — амніон; 6 — гладкий хоріон; 7 — ворсинчастий хоріон; 8 —
пуповинні артерії; 9 — пуповинна вена
173

Акушерство і гінекологія. Том 1
шийки матки: 1) повне передлежання плаценти — плацента повністю перекриває внутрішній зів; 2) часткове передлежання плаценти — плацента частково перекри ває внутрішній зів; 3) крайове передлежання плаценти — край плаценти досягає краю внутрішнього зіва; 4) низьке прикріплення плаценти (низька плацентація) — плацента розміщується в нижньому матковому сегменті, але не досягає краю внут рішнього зіва.
Аномалії прикріплення плаценти включають такі стани: приросла плацента (placenta accreta) — патологічна інвазія плаценти у поверхневий шар міометрія з повною або частковою відсутністю базальної децидуальної оболонки; вросла пла? цента (placenta increta) — патологічна інвазія плаценти у всю товщу міометрія; про? росла плацента (placenta percreta) — патологічна інвазія плаценти з наскрізним про никненням у міометрій і периметрій, іноді з проникненням у прилеглі структури.
Приросла плацента призводить до неможливого відокремлення плаценти від стінки матки при народженні плода, що може призвести до масивної кровотечі, шоку і смерті матері. Інші аномалії плаценти включають більш рідкісні стани: 1) валопо? дібна плацента (placenta circumvallata) — оболонки подвоюються позаду її краю, утворюючи щільне кільце навкруги периферії плаценти; 2) плацента у формі покри? вала (placenta velamentous); 3) резервна плацента (placenta suсcenturiata) — додаткова частка плаценти, яка імплантується на деякій відстані від решти плаценти; 4) пере? длежання судин пупкового канатика (vasa previa) — оболонкове прикріплення пуп кового канатика, коли судини плода проходять над внутрішнім зівом. Такий стан може спостерігатися при placenta velamentous і placenta suсcenturiata.
Кровопостачання плаценти
Котиледони отримують кров з 80–100 спіральних артерій, що пронизують деци дуальну пластинку і входять у міжворсинчасті простори з майже регулярними про міжками. Просвіт спіральних артерій є вузьким, тому тиск крові у міжворсинчасто му просторі високий. Завдяки цьому кров потрапляє на значну глибину у міжвор синчасті простори і омиває численні ворсинки хоріона оксигенованою кров’ю. Коли тиск зменшується, кров повертається з хоріонічної пластинки в децидуальну обо лонку і звідти — у вени ендометрія. Таким чином, кров із міжворсинчастих лакун повертається у материнську циркуляцію через вени ендометрія.
Міжворсинчастий простір зрілої плаценти вміщує близько 150 мл крові, яка онов люється 3–4 рази за хвилину і омиває ворсинки хоріона, площа поверхні яких коли вається від 4 до 14 м2. Але плацентарний обмін відбувається не в усіх ворсинках, а лише в тих, де судини плода тісно контактують із синцитіальним покривом. У цих ворсинках синцитій утворює додаткові мікроворсинки, які збільшують площу кон такту, а отже, швидкість обміну між кров’ю матері та плода.
Плацентарний бар’єр, що відокремлює кров матері від крові плода, спочатку скла дається із чотирьох шарів:
1)ендотелію судин плода;
2)сполучної тканини серцевини ворсинки;
3)цитотрофобластичного шару;
4)синцитію.
З четвертого місяця плацентарна мембрана стоншується завдяки тому, що ендо телій судин вступає у тісний контакт із синцитіальною мембраною, чим досягається збільшення швидкості обміну. Але плацентарний бар’єр може пропускати багато речовин. Враховуючи, що материнська кров у міжворсинчастому просторі відокрем лена від крові плода похідними хоріона, плаценту людини відносять до гемохоріаль?
ного типу.
174

Розділ 5. Репродуктивна генетика...
Функції плаценти
Основні функції плаценти включають:
1)газообмін між кров’ю матері та плода;
2)живильну функцію (обмін метаболітів та електролітів між матір’ю і плодом);
3)гормональну функцію (продукція гормонів);
4)передачу материнських антитіл, які забезпечують пасивний імунітет плода;
5)детоксикаційну функцію (детоксикація деяких речовин).
Обмін газами. Обмін газів у плаценті (кисень, вуглекислий газ, окис вуглецю) відбувається шляхом простої дифузії. Але кількість кисню, що досягає плода у складі материнської крові, первинно залежить від швидкості кровотоку, а не від дифузії. Враховуючи, що плід поглинає з материнської крові 20–30 мл кисню щохвилини, навіть коротка перерва у постачанні кисню є смертельною для плода.
Обмін живильними речовинами та електролітами також є інтенсивним і збільшується при прогресуванні вагітності.
Передача материнських антитіл. Материнські антитіла поглинаються синцитіо трофобластом шляхом піноцитозу з подальшим транспортуванням у капіляри пло да. У такий спосіб плід отримує материнські антитіла, які належать до імуногло булінів класу G (Ig G), класу 7S, і набуває пасивного імунітету проти дифтерії, віспи, кору, але не отримує імунітету проти вітряної віспи, коклюшу та ін. Пасив ний імунітет є дуже важливим, оскільки до народження плід має обмежену здатність продукування власних антитіл.
Гормональна функція. Основними гормонами, що синтезуються в плаценті, є про гестерон, естріол, хоріонічний гонадотропін і соматомамотропін (плацентарний лак тоген). Плацента продукує деяку кількість інших гормонів: хоріонічний адренокор тикотропін, хоріонічний тиротропін, релаксин, рилізинг гормони, нейропептид Y, інгібін і активін та ін.
Наприкінці четвертого місяця плацента продукує достатню кількість прогесте? рону для збереження вагітності у разі видалення жовтого тіла або недостатності його функції. Плацентарні гормони, ймовірно, синтезуються синцитіотрофобластом. Окрім прогестерону, плацента протягом вагітності продукує естрогени (переважно естріол), кількість яких досягає максимуму в кінці вагітності. Високі концентрації естрогенів стимулюють ріст матки і молочних залоз.
Синцитіотрофобласт також продукує хоріонічний гонадотропін людини (ХГЛ), дія якого подібна до лютеїнізуючого гормону передньої частки гіпофіза (ЛГ). Хоріоніч ний гонадотропін людини екскретується з сечею матері; за його рівнем у крові та сечі проводять діагностику і моніторинг вагітності ранніх термінів.
Соматомамотропін (плацентарний лактоген) є подібним до гормону росту і за безпечує плоду пріоритет у використанні глюкози з материнської крові, отже він має до певної міри діабетогенну (контрінсулярну) дію.
Клінічні кореляції
Передача антитіл. Якщо плід є Rh позитивним, а мати — Rh негативною (резус? конфліктна вагітність), еритроцити плода при потраплянні у материнську кров мо жуть викликати утворення антирезусних антитіл. Материнські антитіла проти анти генів плода повертаються до нього і спричинюють гемоліз еритроцитів плода. При чиною реакції антиген — антитіло можуть бути невеликі кровотечі з поверхні вор синок. Гемоліз еритроцитів плода призводить до розвитку гемолітичної хвороби, або еритробластозу плода. Своєчасне профілактичне введення антирезусного анти D імуноглобуліну матері може попередити або зменшити ризик гемолітичної хвороби плода.
175

Акушерство і гінекологія. Том 1
Плацентарний бар’єр. Більшість материнських гормонів не проходить через пла центу. Ступінь проникності через плаценту інших гормонів (тироксин тощо) є не значним. Небезпеку можуть становити синтетичні прогестини (похідні андрогенів), які спроможні спричинювати маскулінізацію плода жіночої статі. Синтетичний ест роген діетилстильбестрол легко проходить через плаценту і спричинює аномалії роз витку матки, маткових труб, верхньої третини піхви, рак піхви, а також аномалії розвитку яєчок у індивідів, які підлягали впливу діетилстильбестролу in utero.
Віруси краснухи, цитомегаловірус, Коксакі, віспи, вітряної віспи, кору, поліоміє літу та інші легко проходять через плацентарний бар’єр і зумовлюють розвиток внут рішньоутробних інфекцій, а також можуть спричинити загибель клітин і природжені вади розвитку. Більшість ліків і метаболітів проникають через плаценту і можуть спричинити ураження ембріона. Вживання матір’ю наркотиків та їх проходження через плаценту може спричинювати у плода звикання до цих речовин і тяжкий абстинентний синдром після народження.
Плацентарна недостатність — клінічний синдром, обумовлений морфологічни ми і функціональними змінами в плаценті, що проявляється порушенням стану, ро сту і розвитку плода. Виділяють три форми плацентарної недостатності: 1) гемоди намічну, зумовлену порушенням матково плацентарного і плодово плацентарного кровотоку; 2) плацентарно мембранну, яка характеризується зниженням можливос тей плацентарної мембрани до транспорту метаболітів; 3) клітинно паренхіматозну, що пов’язана з клітинною активністю трофобласта і плаценти. Первинна плацентар на недостатність розвивається до 16 го тижня вагітності внаслідок анатомічних по рушень будови матки, васкуляризації і розвитку хоріона, захворювань вагітної (ав тоімунні, діабет та ін.) або дії несприятливих чинників зовнішнього середовища (інфекції, мутагени та ін.). Вторинна плацентарна недостатність розвивається в більш пізні терміни вагітності і є наслідком порушення матково плацентарного кровотоку (гіпертензивні хвороби матері, автоімунні захворювання, прееклампсія та ін.). Ви являють гостру плацентарну недостатність (інфаркт, тромбоз, передчасне відшару вання плаценти) і хронічну плацентарну недостатність (при хронічній недостат ності матково плацентарного кровотоку). Гостра плацентарна недостатність призво дить до гострої гіпоксії і, нерідко, смерті плода; хронічна плацентарна недостатність спричинює хронічну гіпоксію і затримку внутрішньоутробного росту (ЗВУР) плода. Профілактика плацентарної недостатності включає лікування захворювань та інфекцій матері до вагітності. Лікування плацентарної недостатності полягає у по кращанні матково плацентарного кровотоку та оксигенації плода, лікуванні мате ринських захворювань і ускладнень, що призвели до розвитку плацентарної недо статності.
Амніон, пупковий канатик і амніотична рідина
Зона контакту між амніоном і зародковою ектодермою (амніоектодермальне спо лучення) має овальну форму і отримала назву первинного пупкового кільця. На п’ятому тижні розвитку через це кільце проходять такі структури: 1) сполучне сте? бельце, що містить алантоїс і пупкові судини, які представлені двома артеріями і однією веною; 2) жовткове стебельце (жовткова протока), яка супроводжується жовтковими судинами; 3) канал, що сполучає внутрішньозародкову та позазародко ву порожнину. Жовтковий мішок локалізується у хоріонічній порожнині, тобто про сторі між амніоном і хоріонічною пластинкою.
Протягом подальшого розвитку амніотична порожнина швидко збільшується за рахунок хоріонічної порожнини й амніон оточує сполучну ніжку і протоку жовтко вого мішка, з’єднуючи їх і утворюючи первинний пупковий канатик. У дистальній
176

Розділ 5. Репродуктивна генетика...
частині первинний пупковий канатик містить жовткову протоку і пупкові судини, а у проксимальній — петлі кишки і залишки алантоїса. Жовтковий мішок міститься у хоріонічній порожнині та сполучається з пупковим канатиком своєю протокою. В кінці третього місяця амніон розширюється так, що вступає у контакт з хоріоном, і хоріонічна порожнина облітерується. Жовтковий мішок також облітерується. Че ревна порожнина тимчасом стає замалою для кишкових петель, які розвиваються і деякі з них у складі пупкового канатика виштовхуються у позазародковий простір. Ці виштовхнуті петлі кишки формують фізіологічну пупкову грижу. Наприкінці 3 го місяця розвитку кишкові петлі втягуються в тіло плода, а порожнина в пупко вому канатику заростає. Після облітерації жовткової протоки й алантоїса в пупко вому канатику залишаються тільки пупкові судини, оточені вартоновими драглями
— спеціалізованим типом сполучної тканини з високим вмістом протеогліканів, яка функціонує як захисне оточення для судин пупкового канатика. Стінки пупкових артерій мають багато м’язових та еластичних волокон, які сприяють швидкому зву женню і скороченню пупкових судин після перев’язування пупкового канатика.
Амніотична порожнина заповнена прозорою водянистою рідиною (амніотичною рідиною), яку частково продукують амніотичні клітини і яка первинно походить з материнської крові. Кількість рідини зростає з 30 мл на 10 му тижні вагітності до 350 мл — на 20 му і 800–1000 мл — на 37 му тижні. Амніотична рідина дозволяє ембріону рухатися та пом’якшує поштовхи, відокремлює плід від амніона. Повний об’єм амніотичної рідини поновлюється кожні 3 год. З початку 5 го місяця плід починає заковтувати амніотичну рідину: він випиває близько 400 мл амніотичної рідини за добу, що становить половину її загальної кількості. З 5 го місяця до скла ду амніотичної рідини приєднується сеча плода, яка містить переважно воду (кінцеві продукти метаболізму видаляються плацентою). Під час пологів амніотична обо лонка формує гідростатичний клин, який сприяє розширенню цервікального кана лу.
Клінічні кореляції
Аномалії пупкового канатика. При народженні дитини пупковий канатик має діа метр близько 2 см і довжину 50–60 см. Він має покручену форму і може утворювати псевдовузли. При збільшенні своєї довжини пупковий канатик може охоплювати шию плода, переважно без несприятливих наслідків, а дуже короткий пупковий канатик може спричинити передчасне відшарування плаценти під час пологів. У нормі пупковий канатик має 2 артерії й 1 вену. В 1 з 200 новонароджених присутня лише 1 артерія, причому 20 % таких дітей можуть мати вади серцево судинної сис теми. Артерія пупкового канатика або не утворюється (агенезія), або дегенерує на ранніх стадіях розвитку.
Амніотичні перетяжки. Рідко розриви амніона в ранні терміни вагітності можуть призвести до утворення амніотичних перетяжок, які охоплюють частини плода — кінцівки, пальці рук. Це спричинює ампутації, кільцеві звуження, черепно лицьові деформації.
Кровообіг плода
Перед народженням плода кров від плаценти, приблизно на 80 % насичена кис нем, повертається до плода через пуповинну вену. Основна маса цієї крові прохо дить через венозну протоку в нижню порожнисту вену, минаючи печінку. Невелика
177

Акушерство і гінекологія. Том 1
частина крові надходить у синусоїди печінки і змішується з кров’ю ворітної системи кровообігу. Сфінктерний механізм у венозній протоці регулює надходження пупо винної крові у синусоїди печінки. Якщо при скороченнях матки венозний приплив зростає, цей сфінктер закривається, що попереджує перевантаження серця плода.
Після короткого шляху через нижню порожнисту вену, де плацентарна кров змішується з деоксигенованою кров’ю, що повертається з нижніх кінцівок таза і нирок, вона потрапляє у праве передсердя. З правого передсердя кров потрапляє в овальний отвір завдяки дії клапана нижньої порожнистої вени, і основна маса крові переходить у ліве передсердя. Невелика частина крові залишається у правому пе редсерді задяки затриманню її нижнім краєм вторинної перегородки — роздільного гребеня. Тут ця кров змішується з десатурованою кров’ю, яка повертається від голо ви та верхніх кінцівок через верхню порожнисту вену.
З лівого передсердя кров, яка змішується з невеликою кількістю десатурованої крові з легенів, потрапляє у лівий шлуночок і висхідну аорту. Оскільки вінцеві та сонні артерії є першими гілками висхідної аорти, міокард та мозок постачаються добре оксигенованою кров’ю. Десатурована кров із верхньої порожнистої вени че рез правий шлуночок потрапляє у легеневий стовбур. Внаслідок того, що опір у легеневих судинах під час внутрішньоутробного життя високий, основна маса крові проходить безпосередньо в артеріальну протоку та низхідну аорту, де вона змішується з кров’ю із проксимальної аорти. З низхідної аорти кров прямує до плаценти двома пуповинними артеріями. Насичення крові киснем у пуповинних артеріях становить близько 58 %. На шляху від плаценти до органів плода кров у пуповинній вені поступово втрачає високу насиченість киснем через змішування з десатурованою кров’ю. Змішування крові може відбуватись у кількох місцях: 1) у печінці (злиття з кров’ю, що повертається з ворітної системи); 2) у нижній порожнистій вені (з кро в’ю від нижніх кінцівок, таза та нирок); 3) у правому передсерді — з кров’ю від голови та верхніх кінцівок; 4) змішування з кров’ю від легенів; 5) змішування у місці входження артеріальної протоки у низхідну аорту.
Зміни кровообігу плода при народженні спричинюються припиненням плацен тарного кровотоку і початком дихання. В цей час артеріальна (боталова) протока закривається завдяки м’язовим скороченням її стінки і кількість крові, яка прохо дить через легені, зростає. Це призводить до збільшення тиску у лівому передсерді. В цей час тиск у правому передсерді зменшується внаслідок припинення плацен тарного кровотоку. Тоді первинна перегородка накладається на вторинну, і оваль ний отвір закривається функціонально. В судинній системі плода після народження відбуваються виражені зміни:
1.Закриття пуповинних артерій завдяки м’язовим скороченням їх стінок, терміч ним і механічним подразникам, змінам у насиченні киснем. Повна анатомічна об літерація може тривати 2–3 міс. Дистальні частини пуповинних артерій утворю ють медіальні пупкові зв’язки, а проксимальні частини залишаються відкритими і утворюють верхні міхурові артерії.
2.Закриття пуповинної вени і венозної протоки відбувається відразу після за криття пуповинних артерій. Кров із плаценти ще деякий час після народження може надходити до плода. Після облітерації пуповинна вена утворює круглу зв’язку печін ки у нижньому краї серпоподібної зв’язки. Венозна протока, яка проходить від круг лої зв’язки до нижньої порожнистої вени, також облітерується і формує венозну зв’язку.
3.Закриття артеріальної протоки внаслідок скорочення м’язової стінки настає майже відразу після народження та регулюється брадикініном та речовиною, яка вивільняється в легенях під час початкового вдиху. Повна анатомічна облітерація триває 1–3 міс. Облітерована артеріальна протока утворює артеріальну зв’язку.
178
