
- •ОГЛАВЛЕНИЕ
- •1. Способы получения
- •1.1. Способы получения алкилгалогенидов
- •а) галогенирование алканов
- •б) аллильное хлорирование алкенов
- •г) гидрогалогенирование алкенов
- •д) гидрогалогенирование сопряженных диенов
- •е) замещение гидроксильной группы в спиртах на галоген
- •1.2. Способы получения винил- и арилгалогенидов
- •1.3. Способы получения дигалогенпроизводных
- •2. Химические свойства
- •2.1. Реакции нуклеофильного замещения (SN) в алкилгалогенидах
- •А) Механизм мономолекулярного нуклеофильного замещения (SN1)
- •Б) Механизм бимолекулярного нуклеофильного замещения (SN2)
- •2.2. Особенности нуклеофильного замещения галогена в арилгалогенидах
- •А) Нуклеофильное замещение в неактивированных арилгалогенидах
- •Б) Нуклеофильное замещение в активированных арилгалогенидах
- •2.3. Реакция дегидрогалогенирования
- •2.4. Восстановление галогенпроизводных
- •2.5. Реакции галогенпроизводных с металлами
- •3. Задачи и упражнения
- •СПИРТЫ
- •1. Способы получения
- •1.1. Гидратация алкенов
- •1.2. Гидролиз галогенпроизводных
- •1.3. Восстановление карбонильных соединений
- •1.4. Получение спиртов реакцией Гриньяра
- •1.5. Получение диолов и триолов
- •2. Химические свойства
- •2.1. Кислотно-основные свойства
- •2.2. Реакции спиртов с разрывом связи О-Н
- •2.2.1. Алкилирование спиртов
- •2.2.2. Ацилирование спиртов
- •2.3. Реакции спиртов с разрывом связи С-О
- •2.3.1. Замещение гидроксильной группы на галоген
- •2.3.2. Образование простых эфиров (межмолекулярная дегидратация)
- •2.3.3. Внутримолекулярная дегидратация спиртов до алкенов
- •2.4. Окисление и дегидрирование спиртов
- •3. Задачи и упражнения
- •ФЕНОЛЫ
- •1. Способы получения
- •1.1. Щелочной гидролиз арилгалогенидов
- •1.2. Щелочное плавление солей ароматических сульфокислот
- •1.3. «Кумольный» метод получения фенола
- •2. Химические свойства
- •2.1. Кислотно-основные свойства фенолов
- •2.2. Фенолы как нуклеофилы
- •2.2.1. Алкилирование и ацилирование фенолов по атому кислорода
- •2.2.2. Реакции электрофильного замещения
- •3. Задачи и упражнения
- •АЛЬДЕГИДЫ И КЕТОНЫ
- •1. Способы получения
- •1.1. Окисление алкенов
- •а) озонолиз алкенов
- •б) окисление алкенов в присутствии хлорида палладия
- •1.2. Гидратация алкинов
- •1.3. Получение ароматических альдегидов и кетонов ацилированием аренов
- •1.4. Гидролиз геминальных дигалогенидов
- •1.5. Окисление и дегидрирование спиртов
- •1.6. Получение альдегидов и кетонов из карбоновых кислот и их производных
- •а) восстановление ацилгалогенидов до альдегидов (реакция Розенмунда)
- •б) пиролиз кальциевых солей карбоновых кислот
- •в) синтез кетонов реакцией Гриньяра из нитрилов карбоновых кислот
- •2. Химические свойства
- •2.1. Кислотно-основные свойства и кето-енольная таутомерия
- •2.2. Реакции нуклеофильного присоединения
- •а) Реакции с О-нуклеофилами
- •б) Реакции с S-нуклеофилами
- •в) Реакции с N-нуклеофилами
- •г) Реакции с С-нуклеофилами
- •2.3. Реакции енолизующихся альдегидов и кетонов с галогенами
- •2.4. Окисление и восстановление альдегидов и кетонов
- •2.4.1. Окисление альдегидов и кетонов
- •2.4.2. Восстановление альдегидов и кетонов
- •2.4.3. Реакция Канниццаро
- •3. Задачи и упражнения

В качестве примеров приведем получение бензальдегида дегидрированием бензилового спирта и получение ацетона окислением дихроматом калия в серной кислоте изопропилового спирта.
|
|
|
|
CH2OH Cu, t |
|
|
|
|
|
CH=O |
||||
|
|
|
|
|||||||||||
|
|
|
|
|
|
|
|
|
||||||
|
|
|
|
|
|
_H2 |
|
|
|
|
|
|
||
|
|
|
|
|
|
|
|
|
|
|
||||
|
|
|
|
|
|
|
|
|
|
|
|
|||
CH3CHCH3 |
K2Cr2O7 |
|
CH3CCH3 |
|||||||||||
H2SO4 |
||||||||||||||
|
|
|
|
|
|
|
|
|
|
|
||||
|
OH |
|
|
|
O |
|||||||||
|
|
|
|
|
|
|
||||||||
1.6. Получение альдегидов и кетонов из карбоновых кислот и их производных
а) восстановление ацилгалогенидов до альдегидов (реакция Розенмунда)
Альдегиды получают гидрированием галогенангидридов карбоновых кислот (ацилгалогенидов) на частично дезактивированном («отравленном») палладии.
R |
|
C |
|
O |
H2 |
R |
|
C |
|
O |
||
|
|
Pd, S |
|
|
||||||||
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Cl |
|
|
|
H |
||||||
б) пиролиз кальциевых солей карбоновых кислот
При нагревании кальциевых солей карбоновых кислот образуются кетоны симметричного строения.
R C=O |
t |
|
|
|
O Ca2 |
R |
C=O |
||
_ |
||||
O |
|
R |
||
R C=O |
CaCO3 |
|
||
|
|
|
Если пиролизу подвергнуть смешанную кальциевую соль двух различных карбоновых кислот, то продуктом реакции окажется несимметричный кетон. Например, смешанная кальциевая соль уксусной и фенилуксусной кислот при пиролизе превращается в бензилметилкетон, а из соли муравьиной и бензойной кислот можно получить бензальдегид.
53
http://mitht.ru/e-library
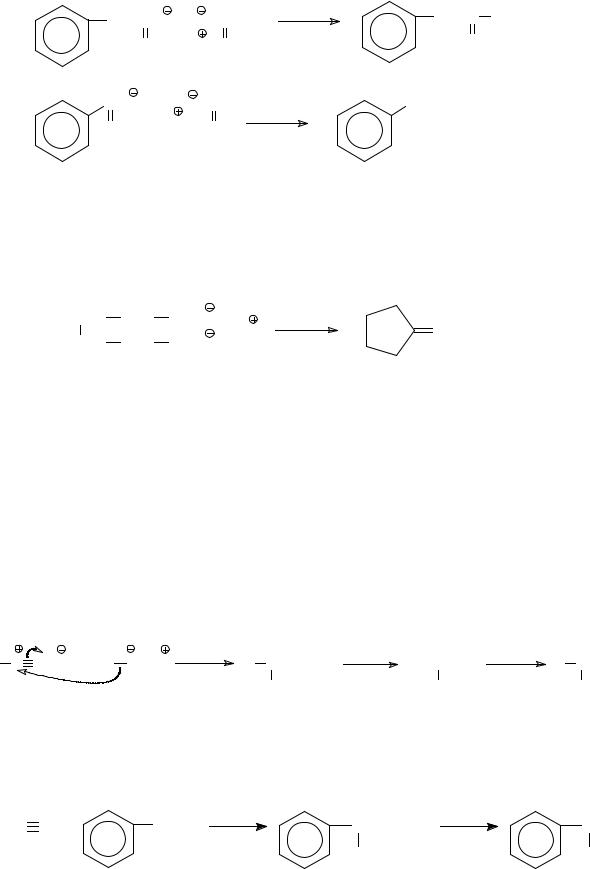
CH2CO |
|
OCCH3 |
t |
CH2C CH3 |
||
|
_ CaCO3 |
|||||
|
O Ca2 |
O |
|
O |
||
CO |
Ca2 |
OCH |
|
t |
CH=O |
|
O |
|
|
O |
_ CaCO3 |
|
|
Этим методом удобно получать циклические кетоны с размером цикла от 5 до 7 атомов углерода. Они образуются при пиролизе кальциевых солей подходящих дикарбоновых кислот. Например, циклопентанон образуется из адипината кальция:
CH2 |
CH2 |
COO |
Ca2 |
t |
O |
|
_ CaCO3 |
||||||
CH2 |
CH2 |
COO |
|
|
адипинат кальция
в) синтез кетонов реакцией Гриньяра из нитрилов карбоновых кислот
В нитрилах карбоновых кислот атом углерода цианогруппы является электрофильным центром, к которому могут присоединяться нуклеофильные реактивы Гриньяра. Продукт этого присоединения при гидролизе превращается в так называемый имин, который далее гидролизуется до кетона.
δ |
δ |
+ |
R' |
δ |
δ |
R C=NMgX H2O |
R C=NH |
H2O |
R C=O |
R C N |
|
|
MgX |
||||||
|
|
|
|
|
|
R' |
R' |
_ NH3 |
R' |
|
|
|
|
|
|
|
Так, например, ацетофенон (метилфенилкетон) можно получить взаимодействием нитрила уксусной кислоты и фенилмагнийбромида с последующим гидролизом.
CH3C N + |
MgBr |
C=NMgBr |
2H2O |
C=O |
|
||||
|
|
CH3 |
|
CH3 |
Возможен и другой вариант синтеза ацетофенона реакцией Гриньяра: из нитрила бензойной кислоты и метилмагниййодида.
54
http://mitht.ru/e-library
