
- •Часть I. Теоретическая химия
- •Глава 1. Основные понятия и законы химии
- •§ 1.1. Задачи с решениями
- •§ 1.2. Задачи для самостоятельного решения
- •1.2.1. Задачи на расчет числа молей
- •1.2.2. Задачи на определение формул веществ
- •1.2.3. Расчеты по химическим уравнениям
- •1.2.4. Задачи на смеси
- •1.2.5. Задачи на газовые законы
- •Глава 2. Строение атома и периодический закон
- •§ 2.1. Задачи с решениями
- •§ 2.2. Задачи для самостоятельного решения
- •2.2.1. Электронные конфигурации и Периодическая система
- •2.2.2. Изотопы и радиоактивные превращения
- •Глава 3. Химическая связь
- •§ 3.1. Задачи с решениями
- •§ 3.2. Задачи для самостоятельного решения
- •3.2.1. Типы химической связи и их характеристики
- •3.2.2. Валентность. Степени окисления элементов. Геометрическая структура молекул.
- •3.2.3. Строение и свойства вещества
- •Глава 4. Закономерности протекания химических реакций
- •§ 4.1. Задачи с решениями
- •§ 4.2. Задачи для самостоятельного решения
- •4.2.1. Энергетика химических превращений
- •4.2.2. Химическая кинетика и катализ
- •4.2.3. Обратимые и необратимые реакции. Состояние химического равновесия.
- •Глава 5. Растворы электролитов и неэлектролитов
- •§ 5.1. Задачи с решениями
- •§ 5.2. Задачи для самостоятельного решения
- •5.2.1. Способы выражения концентрации растворов
- •5.2.2. Ионные реакции в растворах
- •Глава 6. Окислительно-восстановительные процессы. Ряд напряжений. Электролиз растворов и расплавов.
- •§ 6.1. Задачи с решениями
- •§ 6.2. Задачи для самостоятельного решения
- •6.2.1. Окислители и восстановители
- •6.2.2. Составление уравнений овр и подбор коэффициентов
- •6.2.3. Влияние pH среды на характер протекания овр
- •6.2.4. Электрохимический ряд напряжений
- •6.2.5. Электролиз растворов и расплавов
- •Часть II. Неорганическая химия
- •Глава 7. Номенклатура, классификация, свойства и способы получения неорганических веществ
- •§ 7.1. Задачи с решениями
- •§ 7.2. Задачи для самостоятельного решения
- •7.2.1. Важнейшие классы неорганических соединений
- •7.2.2. Классификация химических реакций
- •7.2.3. Гидролиз солей
- •Глава 8. Водород. Галогены.
- •§ 8.1. Задачи с решениями
- •§ 8.2. Задачи для самостоятельного решения
- •8.2.1. Водород
- •8.2.2. Галогены и их соединения
- •Глава 9. Элементы подгруппы кислорода
- •§ 9.1. Задачи с решениями
- •§ 9.2. Задачи для самостоятельного решения
- •9.2.1. Кислород и его соединения
- •9.2.2. Сера и ее соединения
- •Глава 10. Подгруппа азота и фосфора
- •§ 10.1. Задачи с решениями
- •§ 10.2. Задачи для самостоятельного решения
- •10.2.1. Азот и его соединения
- •10.2.2. Фосфор и его соединения
- •Глава 11. Подгруппа углерода и кремния
- •§ 11.1. Задачи с решениями
- •§ 11.2. Задачи для самостоятельного решения
- •11.2.1. Углерод и его соединения
- •11.2.2. Кремний и его соединения
- •Глава 12. Металлы главных подгрупп (щелочные, щелочноземельные, алюминий)
- •§ 12.1. Задачи с решениями
- •§ 12.2. Задачи для самостоятельного решения
- •12.2.1. Щелочные металлы
- •12.2.2. Щелочноземельные металлы
- •12.2.3. Алюминий и его соединения
- •Глава 13. Главные переходные металлы
- •§ 13.1. Задачи с решениями
- •§ 13.2. Задачи для самостоятельного решения
- •13.2.1. Железо и его соединения
- •13.2.2. Медь и ее соединения
- •13.2.3. Серебро и его соединения
- •13.2.4. Хром и его соединения
- •13.2.5. Марганец и его соединения
- •Часть III. Органическая химия
- •Глава 14. Общая характеристика органических соединений
- •§ 14.1. Задачи с решениями
- •§ 14.2. Задачи для самостоятельного решения
- •Глава 15. Предельные углеводороды
- •§ 15.1. Задачи с решениями
- •§ 15.2. Задачи для самостоятельного решения
- •15.2.1. Строение, номенклатура, изомерия
- •15.2.2. Получение
- •15.2.3. Химические свойства
- •Глава 16. Углеводороды с двойной связью
- •§ 16.1. Задачи с решениями
- •§ 16.2. Задачи для самостоятельного решения
- •16.2.1. Строение, номенклатура, изомерия
- •16.2.2. Получение
- •16.2.3. Химические свойства
- •Глава 17. Алкины
- •§ 17.1. Задачи с решениями
- •§ 17.2. Задачи для самостоятельного решения
- •17.2.1. Строение, номенклатура, изомерия
- •17.2.2. Получение
- •17.2.3. Химические свойства
- •Глава 18. Ароматические углеводороды (арены)
- •§ 18.1. Задачи с решениями
- •§ 18.2. Задачи для самостоятельного решения
- •18.2.1. Строение, номенклатура, изомерия
- •18.2.2. Получение
- •18.2.3. Химические свойства
- •Глава 19. Спирты. Фенолы
- •§ 19.1. Задачи с решениями
- •§ 19.2. Задачи для самостоятельного решения
- •19.2.1. Строение, номенклатура, изомерия
- •19.2.2. Получение
- •19.2.3. Химические свойства
- •Глава 20. Альдегиды. Кетоны
- •§ 20.1. Задачи с решениями
- •§ 20.2. Задачи для самостоятельного решения
- •20.2.1. Строение, номенклатура, изомерия
- •20.2.2. Получение
- •20.2.3. Химические свойства
- •Глава 21. Карбоновые кислоты и их производные
- •§ 21.1. Задачи с решениями
- •§ 21.2. Задачи для самостоятельного решения
- •21.2.1. Строение, номенклатура, изомерия карбоновых кислот
- •21.2.2. Получение карбоновых кислот
- •21.2.3. Химические свойства карбоновых кислот
- •21.2.4. Сложные эфиры
- •21.2.5. Жиры
- •Глава 22. Углеводы
- •§ 22.1. Задачи с решениями
- •§ 22.2. Задачи для самостоятельного решения
- •22.2.1. Моносахариды
- •Глава 23. Амины
- •§ 23.1. Задачи с решениями
- •§ 23.2. Задачи для самостоятельного решения
- •23.2.1. Строение, номенклатура, изомерия
- •23.2.2. Получение
- •23.2.3. Химические свойства
- •Глава 24. Аминокислоты и пептиды
- •§ 24.1. Задачи с решениями
- •§ 24.2. Задачи для самостоятельного решения
- •24.2.1. Строение и изомерия
- •24.2.2. Получение и химические свойства
- •Глава 25. Азотсодержащие гетероциклические соединения
- •§ 25.1. Задачи с решениями
- •§ 25.2. Задачи для самостоятельного решения
- •25.2.1. Гетероциклические основания
- •25.2.2. Нуклеиновые кислоты
- •Часть IV варианты вступительных экзаменов
- •Глава 26. Вступительные экзамены в Московском государственном университете
- •Глава 27. Вступительные экзамены в Московской медицинской академии
- •Глава 28. Решения избранных вариантов вступительных экзаменов
Глава 24. Аминокислоты и пептиды
Аминокислоты — это бифункциональные органические соединения, в молекуле которых имеются аминогруппа и карбоксильная группа. По их взаимному расположению различают -, -, -аминокислоты. Среди них особое место занимают -аминокислоты, поскольку в них имеется по меньшей мере один асимметрический атом углерода:
![]()
Аминокислоты называют обычно как замещенные производные соответствующих карбоновых кислот, обозначая положение аминогруппы буквами греческого алфавита.
Изомерия аминокислот связана с положением функциональных групп и со строением углеродного скелета.
Функциональные группы в аминокислотах реагируют между собой. Поэтому молекулы аминокислот представляют собой биполярные ионы (внутренние соли), например, H3N+CH2COO-.
Аминокислоты — амфотерные соединения, они реагируют с кислотами и основаниями. Им свойственны обычные реакции по карбоксильной группе и аминогруппе. Однако, кислотные и основные свойства выражены очень слабо. В результате межмолекулярного взаимодействия амино- и карбоксильной групп аминокислоты вступают в реакции поликонденсации с образованием пептидов различного строения.
§ 24.1. Задачи с решениями
Задача 237. Определите строение сложного эфира -аминокислоты, если известно, что он содержит 15,73% азота по массе.
Решение. Сложные эфиры -аминокислот описываются общей формулой:
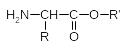
где R — водород или углеводородный радикал, R' — углеводородный радикал. В одном моле этого вещества содержится один моль N массой 14 г, что составляет 15,73% от общей (молярной) массы; следовательно молярная масса эфира равна: M(H2NCH(R)COOR') = 14/0,1573 = 89 г/моль. На долю двух радикалов приходится M(R+R') = 89 – M(H2N+CH+COO) = 16 г/моль. Это возможно только в том случае, если R = H, R' = CH3. Таким образом, искомый эфир — метилглицинат, т.е. метиловый эфир аминоуксусной кислоты:
H2NCH2COOCH3.
Ответ. Метиловый эфир аминоуксусной кислоты.
Задача 238. Какой объем 10%-ного раствора гидроксида натрия (плотность 1,1 г/мл) может прореагировать с глицином, полученным из 32 г карбида кальция?
Решение. Глицин можно получить из карбида кальция по схеме:
CaC2 C2H2 CH3CHO CH3COOH ClCH2COOH H2NCH2COOH.
Согласно этой схеме, число молей глицина равно числу молей карбида кальция: (H2NCH2COOH) = (CaC2) = 32 / 64 = 0,5 моль. Количество щелочи, необходимой для реакции с глицином по уравнению
H2NCH2COOH + NaOH = H2NCH2COONa + H2O,
также равно 0,5 моль. m(NaOH) = 0,540 = 20 г;
m(р-ра NaOH) = 20 / 0,1 = 200 г;
V(р-ра NaOH) = 200 / 1,1 = 182 мл.
Ответ. 182 мл.
Задача 239. Этиловый эфир глицина массой 2,06 г прокипятили с раствором, содержащим 1,50 г гидроксида калия, и полученный раствор выпарили. Рассчитайте массу сухого остатка.
Решение. При кипячении происходит щелочной гидролиз сложного эфира с образованием калиевой соли глицина:
H2NCH2COOC2H5 + KOH H2NCH2COOK + C2H5OH.
(H2NCH2COOC2H5) = 2,06 / 103 = 0,02 моль, (KOH) = 1,50 / 56 = 0,0268 моль — избыток. В результате реакции образуется 0,02 моль глицината калия H2NCH2COOK массой 0,02113 = 2,26 г, и остается неизрасходованным гидроксид калия массой 1,5 – 0,0256 = 0,38 г. Этанол и вода улетучиваются из раствора при выпаривании. Масса сухого остатка равна 2,26 + 0,38 = 2,64 г.
Ответ. 2,64 г.
Задача 240. Напишите структурную формулу одного из природных трипептидов, в молекуле которого на четыре атома кислорода приходится три атома серы.
Решение. Общая формула природных трипептидов:
![]()
где R, R’, R’’ — остатки -аминокислот. Мы видим, что эти остатки не содержат атомов кислорода, но содержат три атома серы. Среди природных аминокислот нет ни одной, которая бы содержала более одного атома серы, поэтому каждый остаток в данном пептиде содержит ровно один атом серы. Простейший вариант — пептид, образованный тремя остатками серосодержащей аминокислоты цистеина:
 .
.
Ответ. Трипептид, состоящий из трех остатков цистеина.
Задача 241. Определите строение вещества, имеющего состав C6H12O3S2N2, если известно, что из него можно получить соединение состава C3H9O6S2N.
Решение. Конечное соединение содержит в два раза меньше атомов углерода, чем исходное, поэтому можно предположить, что схема реакций включала гидролиз и что исходное вещество — дипептид. Конечное соединение содержит азот и серу, поэтому вероятно, что это — сернокислая соль аминокислоты. Если из формулы C3H9O6S2N вычесть H2SO4, то получим C3H7O2SN. Это — молекулярная формула аминокислоты цистеина. Если эту формулу умножить на 2 и вычесть H2O, то получим C6H12O3S2N2 — формулу исходного соединения.
Таким образом, исходное соединение C6H12O3S2N2 — дипептид цистеина, конечное соединение C3H7O2SN — сульфат цистеина, HSCH2CH(NH3HSO4)COOH.
Сульфат цистеина можно получить из дипептида цистеина в одну стадию путем гидролиза дипептида при нагревании с избытком серной кислоты:

Процесс можно провести в две стадии, если сначала гидролизовать дипептид в щелочной среде, а затем добавить избыток серной кислоты.
Ответ. C6H12O3S2N2 — дипептид цистеина.
Задача 242. При полном гидролизе 14,6 г природного дипептида раствором гидроксида натрия (массовая доля щелочи 12%, плотность раствора 1,2 г/мл) из раствора выделено 11,1 г соли, массовая доля натрия в которой равна 20,72%. Установите возможную структурную формулу исходного дипептида и вычислите объем раствора щелочи, израсходованный на гидролиз.
Решение. Запишем уравнение гидролиза в общем виде:

Одна из солей содержит 20,72% Na, следовательно, ее молярная масса равна 23/0,2072 = 111 г/моль, и ее количество составляет 11,1/111 = 0,1 моль. Молярная масса углеводородного радикала, входящего в состав этой соли (это может быть как R1, так и R2) равна: M(R) = 111M(H2N)M(CH)M(COONa) = 111161367 = 15. Этот радикал — CH3.
Найдем другой радикал. Количество дипептида равно 0,1 моль, следовательно его молярная масса равна 14,6/0,1 = 146 г/моль. Молярная масса второго радикала равна: 146M(H2N)M(CHCH3)M(CONH)M(CH)M(COOH) = 1461628431345 = 1, этот радикал — H.
Таким образом, одна из кислот, образовавших дипептид, — аминопропионовая, а другая — аминоуксусная. Каждая из этих аминокислот может находиться либо в "голове" дипептида (со стороны группы COOH), либо в "хвосте" (со стороны группы NH2), поэтому для пептида возможны 2 формулы:
1) H2NCH(CH3)CONHCH2COOH (аланилглицин);
2) H2NCH2CONHCH(CH3)COOH (глицилаланин).
Ответ. Аланилглицин или глицилаланин.
