
- •Раздел 1. Введение. Лекция 1. Требования, предъявляемые к современным металлургическим процессам.
- •Вопрос 1. Комплекснгость использования сырья (кис)
- •Вопрос 2. Экологическая безопасность технологий.
- •Вопрос 3. Удельная производительность оборудования
- •Вопрос 1. Способы получения порошков.
- •Вопрос 2. Механическое изельчение
- •Вопрос 3. Распыление расплава
- •Вопрос 1. Твердофазное восстановление
- •Вопрос 2. Электролиз.
- •Вопрос 3. Цементация
- •Вопрос 4. Карбонильный метод
- •Вопрос 5. Термолиз
- •Вопрос 6. Автоклавный способ
- •Вопрос 7. Специальные способы
- •Вопрос 1. Химические свойства
- •Вопрос 2. Физические свойства
- •Вопрос 3. Технологические свойства
- •Вопрос 4. Производство изделий из порошков
- •Раздел 3. Автогенные процессы в металлургии меди. Лекция 5. Некоторые теоретические аспекты автогенных процессов
- •Вопрос 1. . Физико-химические принципы автогенности, методы достижения.
- •Вопрос 2.Особенногсти тепловых балансов.
- •Вопрос 3. Влияние различных факторов на тб ап в общем случае автогенный режим автогенных процессов зависит от следующих факторов:
- •Вопрос 4. Оксисульфидные системы.
- •Лекция 3. Практика автогенных процессов (ап)
- •Вопрос 1. Классификация ап и преимущества ап
- •Совмещенная плавка-конвертирование (спк)
- •Технологические преимущества автогенных процессов.
- •Вопрос 2. Кислородно-факельная плавка, аппаратурное оформление
- •Технологическая схема приведена на рис. 1. Вопрос 2. Особенности ф-х процессов технологии
- •Вопрос 3. Технологическая схема производства с использованием кфп следующая
- •Вопрос 3. Т-э показатели процессса, преимущества, недостатки, перспективы.
- •Недостатки:
- •Лекция 7. Плавка во взвешенном состоянии.
- •Вопрос 2. Практика процесса.
- •Недостатки ап первой группы (классификация):
- •Лекция 8. Плавка в печах Ванюкова.
- •Вопрос 2. Конструкция печи. Печь представляет собой шахту, кессонированную в средней части и футерованную ниже оси фурм.
- •Вопрос 7. Показатели и перспективы процесса пв:
- •Вопрос 1. Спк на уральских предприятиях(оао «ммск»)
- •Вопрос 2. Практика спк на оао «Святогор». Технологическая схема спк на оао «Святогор» включает (рис.2.) плавку концент-
- •Вопрос 3. Технология «Эльтениенте» (Чили).
- •Вопрос 2. Технология «Мицубиси»
- •Вопрос 3. Практика работы завода «Гресик» Индонезия
- •Лекция 11. Ап с погружной фурмой. Аусмелт
- •Вопрос 1. Классификация процессов.
- •Особенность фурмы аусмелт
- •Вертикальная фурма многоцелевого назначения.
- •Вопрос 2. Оосбенности технологии « кивцэт»
- •Вопрос 3. Схема кифцэт:
- •Показатели
- •Вопрос 3. Факельно-барботажная плавка фбп.
- •Технико-экономические показатели факельно-барбатажной плавки:
- •Раздел 4. Современное состояние и пути модернизации существующих процессов.
- •Вопрос 2. Характеристика шахтной плавки.
- •Вопрос 1. Характеристика современного состояния
- •Вопрос 2. Пути совершенствования оп и ее перспективы
- •Лекция 14. Современное состояние процесса конвертирования медных штейнов и перспективы развития производства.
- •Вопрос 1. Теория конвертирования
- •Вопрос 1. Распределение основных спутников меди
- •Лекция 16 Современная практика конвертирования и направление совершенствования процесса.
- •Вопрос 1. Характеристика конвертеров и технологии
- •Вопрос 2. Прогресс в области конвертирования:
- •Вопрос 3. Повышение качества флюса.
- •Часть 5.Современное состояние и перспективы технологии рафинирования черновой меди.
- •Вопрос 1. Термодинамика реакций окисления меди и примесей
- •Вопрос 2. Анализ системы Cu-п-о
- •Вопрос 5. Термодинамика дегазации и раскисления
- •Вопрос 1. Типы печей.
- •Стационарная отражательная печь
- •Технические характеристики пламенных печей
- •Наклоняющиеся печи, по сравнению с отражательными печами, имеют преимущества:
- •Вопрос 2. Характеристика печи «Мерц»
- •Вопрос 3. Оборудование для разливки анодов
- •Вопрос 4. Разливочная машина.
- •Технические характеристики
- •Лекция 20. Технология рафинирования. Режимные параметры операций
- •Вопрос 1. Основные операции рафинрвания
- •Вопрос 3. Виды восстановителя
- •Вопрос 4.Особенности восстановления в печи Мерц
- •Вопрос 5. Реагентное рафинирование.
- •Вопрос 2. Поведение примесей на аноде и катоде
- •Вопрос 4. Образование медеэлектролитного шлама
- •Вопрос 5. Пассивация анода
- •Вопрос 6. Структура катодных осадков
- •Вопрос 7. Добавки в электролит
- •Вопрос 8. Влияние температуры электролита
- •Вопрос 3. Принцип работы автоматической линии для сборки и расстановки стартерных катодов
- •Вопрос 4. Работа «Стрипп-машины».
- •Вопрос 5. Конструкции электролизных ванн
- •Вопрос 6. Системы включения электродов
Лекция 14. Современное состояние процесса конвертирования медных штейнов и перспективы развития производства.
Вопрос 1. Теория конвертирования
Плавка сульфидных медных руд и концентратов за исключением способов прямого производства черновой меди (Direkt-To-Blister Flach smelting) заканчивается получением промежуточного продукта - медного штейна, который направляют на конвертирование.
Целью конвертирования является удаление из штейна железа, серы и получение черновой меди, в которую также концентрируют благородные металлы. Попутными продуктами являются конвертерный шлак, пыль и серусодержащие газы.
Процесс получения черновой меди состоит из двух периодов, продолжительность которых зависит от содержания меди в штейне и количества подаваемого воздуха. Так, при работе на богатые штейны (более 40-45 % Cu) первый период длиться 6-9 ч, а при бедном (менее 20% Сu) 16-24 ч. Продолжительность второго периода составляет 2-3 ч.
Химизм первого и второго периодов конвертирования может быть в первом приближении соответственно, представлен схемами
[Cu-Fe-S] + {O2}+ [SiO2] → [Cu-S] + (FeO-SiO2-Fe3O4) + SO2,
[Сu-S] + {O2} → [Cu] + SO2
Расслоение фаз и разрыв областей гомогенности расплавов разных периодов конвертирования схематично иллюстрирует развертка диаграммы Cu-Fe-S-O (рис. 1), построенная в общем виде.
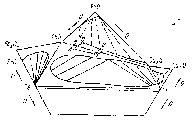
Рис.1. Развертка диаграммы состояния системы Сu-Fе-S-О
На боковых сторонах диаграммы показаны широкие области разрыва смесимости псевдобинарных систем Fe-FeO; Cu-Cu2O; FeO-Cu2S относительно составов промышленных штейнов АВСDEF. Введение кислорода приводит к достижению расплавом предела насыщения по кислороду, на что указывают почти смыкающиеся области расслаивания. Линия, соединяющая состав бедных медных штейнов (АВС) и FeO-Fe3O4 неглубоко проникает в область расслаивания, поэтому образуется сравнительно небольшое количество металлизированной фазы, растворяющейся в штейне. Получается более высокий выход первичного шлака, чем металлизированной фазы. Избыточное сверх стехиометрии металлическое железо, взаимодействует с кислородом дутья
2Fe + O2 = 2FeO
В результате образуются первичный шлак и, насыщенный кислородом штейновый расплав с растворенным металлическим железом, выгорающим по мере конвертирования.
Введение флюса (SiO2), как отмечалось ранее, существенно расширяет области расслаивания системы Cu-Fe-S-O и способствует шлакообразованию. Однако окисление сульфидов газообразным кислородом преимущественно осуществляется в фурменной зоне, а кварц, имея меньшую плотность, рассредоточен по поверхности расплава. Поскольку скорость окисления сульфидов в условиях барботажа высокая, о чем свидетельствует практически полное усвоения кислорода в области фурм, то общая скорость шлакообразования лимитируется скоростью растворения кремнезема. В этом случае целесообразна подача тонкоизмельченного флюса непосредственно в зону реакции например, с использованием известных в инжекционной металлургии , методов ввода в расплав газопорошковых струй (ПГС).
Роль кремнезема, заключается еще и в снижении активности закиси железа в шлаке, что способствует протеканию реакции
3Fe3O4+FeS+5SiO2=5(2FeO*SiO2)+SO2
и уменьшает содержание магнетита. В реальных условиях кислотность шлака определяется скоростью образования FeO (расходом дутья) и скоростью растворения SiO2 в шлаке, которая возрастает с увеличением температуры . В связи с необходимостью увеличения срока службы футеровки, температурный режим конвертирования ограничен величиной t =1300-1350 оС., что способствует высокой концентрации магнетита в шлаке (до 25-28%).
Оптимальная концентрация кремнезема составляет ~ 25 %. Более низкая повышает содержание Fe3O4 в шлаке, а более высокая ( ~ 30%), приводит к нецелесообразному расходу флюса и увеличивает выход шлака.
Крупность кварца, способствующая его быстрому усвоению ванной и соответствующая наименьшим механическим потерям с пылью находится в пределах 10-20 мм. Предпочтительно использовать кремнезем с высоким содержанием SiO2 (95-96 %) и минимальным количеством тугоплавких составляющих (MgO, CaO, Al2O3). Последние уменьшают скорость его растворения, увеличивают выход шлака и снижают кислотность. В этой связи, применение золотосодержащих кварцевых флюсов с повышенным количеством примесей, должно быть экономически обосновано с учетом способа обеднения конвертерных шлаков и оценки общего извлечения меди. Флюсы наиболее полно усваиваются ванной при горячем ходе конвертера.
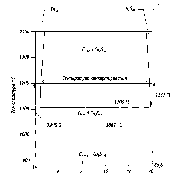
Общую картину фазового состояния второго периода конвертирования можно также проследить по стороне развертки стороны диаграммы Cu2S-Cu2O-Cu или более наглядно на схеме диаграммы Cu-S (рис. 2). Предположим, что продувку белого матта (Сu2S) осуществляем при температуре 1200оС. Фигуративная точка, показывающая изменение массы расплава перемещается влево и на участке ab (рис. 5.31), конвертерная масса представляет однородный раствор меди в
Рис.2. Диаграммма равновесий в системе Cu-S
Cu2S. На последующем участке bc процесс осуществляется в двухфазной области, где в контакте находятся сульфидная фаза состава b и металлическая с. Точка b соответствует содержанию Сu2S 19.6 % ( 1200oC), а точка с- отвечает концентрации серы в металлической меди ~ 1 % S. После точки с сульфидная фаза исчезает и остается только металлическая, насыщенная сульфидами.
В связи с тем, что белый матт находится в контакте с остатками конвертерного шлака, то парциальное давление серы в газовой фазе и концентрация серы в меди определяются условиями равновесия реакции взаимодействия Cu2S с Cu2O. Содержание меди в последних сливах шлака составляет 20-25% и низкая активность кислорода (Cu2O) в шлаке и Cu, являются причинами, что при конвертировании получают черновую медь с концентрацией не более 0.01% S. Направление конод, сходящихся в медном углу диаграммы указывает, что окисление полусернистой меди протекает с образованием металлической фазы Cu.
В ходе первого периода осуществляют постепенное накопление в конвертере богатой сульфидной массы, чередуя порционную заливку штейна c его продувкой и слива шлака. Эти операции повторяют несколько раз до появления в конвертере достаточного количества обогащенной массы. Изменение содержания меди в штейне носит циклический характер, увеличивается при сливе шлака и снижается при заливке штейна (рис. 3).
Соответственно изменяются физико-химические свойства расплава. По мере продувки штейна и выгорания поверхностно активного железа, образования шлака и обогащения массы, возрастает величина межфазного натяжения на границе штейн-шлак, что способствует разделению расплавов. Более высокая температура в первом периоде снижает вязкость и плотность шлака по сравнению со вторым периодом.
Теоретическое
содержание сернистого ангидрида в
атмосфере конвертера также различается
по периодам конвертирования. Например,
для воздушного дутья и при степени
использовании кислорода 95-99 % (без учета
образования магнетита и SO3,)
концентрация SO2
составляет, %, об: 14.2-14.8 SO2
(первый) и 19.5-20.8 SO2
(второй)
периоды. Полученные значения в целом,
соответствуют практическим данным
первого (12.1-13.7 SO2;
0.91-1.2 SO3;
0.09-0.33 )
и второго (15.38-15,62SO2;
1.55-2.38 SO3;
0.23-0.3
)
и второго (15.38-15,62SO2;
1.55-2.38 SO3;
0.23-0.3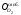 )
периодов конвертирования, если
рассматривать суммарную концентрациюSO2
и SO3
[89].
)
периодов конвертирования, если
рассматривать суммарную концентрациюSO2
и SO3
[89].

Наличие SO3 в отходящих газах, направляемых в сернокислотное производство, необходимо учитывать в связи со следующим обстоятельствами.
При совместном присутствии серного ангидрида и влаги, возможна коррозия оборудования конвертеров и газового тракта, изготовленного из металла, особенно на участках газового тракта с низкой температурой, где высока вероятность выпадение росы. Такими местами могут быть газоход перед электрофильтрами, электрофильтры, участок тракта после электрофильтров и пр. В частности, содержание SO3 в газоходе после электрофильтров может составлять 0.01-0.1 % , а концентрация влаги до 2 %. ( без подачи воды на охлаждение) и 7-10 % ( при системе искусственного орошения газохода). В этих условиях температура точки, согласно диаграмме ( рис. 5.33.), составляет без добавок воды 167 и 180 оС при ее впрыскивании. Наличие оксидов цинка и свинца в газах в какой-то мере, нейтрализует воздействие SO3 за счет связывания серного ангидрида в форму сульфатов, однако на практике коррозия газоходов и оборудования происходит. Одним из мероприятий снижающих износ оборудования может являться тщательный контроль температуры газового поток, не допуская его охлаждения ниже точки выпадения росы.
Лекция 15. Поведение примесей .
