
- •Вопрос 4. Структурная классификация полиморфизма
- •Вопрос 6. Твердые растворы
- •Вопрос 9. Признаком краевой дислокации является наличие в одной части кристалла лишней («оборванной» или «недостроенной») атомной плоскости, не имеющей продолжения в другой части кристалла.
- •Вопрос 11. Свойства дислокаций:
- •Вопрос 12. Гипотезы строения жидкостей .
- •Вопрос 14. Фх особенности стеклообразного сост-я:
- •Вопрос 15. Процесс стеклообразования определяется следующими факторами:
- •Вопрос 16.
- •Вопрос 17. Устойчивость и коагуляция коллоидных силикатных систем
- •Вопрос 18. Структуры, образующиеся в высокодисперсных системах, п. А. Ребиндер предложил классифицировать:
- •Вопрос 22. Общий вид диаграммы состояния однокомпонентной системы
- •Вопрос 23.
- •Вопрос 24.
- •Вопрос 25. Двухкомпонентные диаграммы состояния
- •Вопрос 26. Диаграмма состояния двухкомпонентной системы с химическим соединением, плавящимся без разложения (конгруэнтно).
- •Вопрос 27.
- •Вопрос 28. Диаграмма состояния двухкомпонентной системы с непрерывным рядом твердых растворов.
- •Вопрос 29. Динамический и статический методы построения диаграмм состояния.
- •Вопрос 30.
- •Вопрос 31.
- •Вопрос 32. Система MgO—SiO2
- •Вопрос 33. Система а12o3— SiO2
- •Вопрос 34. Трехкомпонентные диаграммы состояния
- •Вопрос 36. Диагр.Сост. Трехкомп.Сист. С эвтектикой.
- •Вопрос 37.
- •Вопрос 39.
- •Вопрос 40. Диаграмма состояния трехкомпонентной системы с тройным химическим соединением, плавящимся конгруэнтно, полиморфными превращениями и ликвацией.
- •Вопрос 42. Система Na2o-CaO-SiO2
- •Вопрос 43. Система CaO-Al2o3-SiO2
- •Вопрос 44. Система MgO- Al2o3- SiO2
- •Вопрос 45. Система СаО—MgO — SiO2
- •Вопрос 46. Диссоциация –химический процесс распада молекул, радикалов, ионов на несколько частиц, имеющих меньшую молекулярную массу.
- •Вопрос 47. Дегидратация.
- •Вопрос 49.
- •Вопрос 50. Особенности твердофазовых реакций:
- •Вопрос 51. Кинетика твердофазовых реакций
- •Вопрос 52. Факторы, влияющие на скорость твердофазовых реакций:
- •Вопрос 54. Жидкостное спекание.
- •Вопрос 55. Твердофазовое спекание. Осуществляется под действием температуры за счет переноса вещества в твердой фазе в отсутствие жидкости и без участия газовой фазы.
- •Вопрос 56. Кинетика твердофазового спекания.
- •Вопрос 57. Спекание за счет процесса “испарние — конденсация”
- •Вопрос 58. Первичная Рекристаллизация.
- •Вопрос 59. Вторичная рекристаллизация.
- •Вопрос 61. Кристаллизация.
- •Вопрос 62. Гомогенное образование центров кристаллизации
- •Вопрос 63. Гетерогенное образование центров кристаллизации.
- •Вопрос 66. Структура и классиф полимеров
- •Вопрос 67. Химическое строение макромолекул
- •Вопрос 68. Особенности линейных, разветвленных и сетчатых полимеров
- •Вопрос 69. Способы получения полимеров.
- •Вопрос 70. Карбоцепные полимеры
- •Вопрос 72. Старение и стабилизация полимеров.
- •Вопрос 73. Физическая Структура Полимеров.
- •Вопрос 74.Агрегатные и фазовые состояния полимеров
- •Вопрос 75. Аморфное состояние полимеров.
- •Вопрос 78. Химический состав древесины.
- •Вопрос 79. Под макроскопическим строением (макроструктурой) древесины понимают детали структуры, которые можно исследовать невооруженным глазом и с помощью лупы.
- •Вопрос 80. Анатомическое строение древесины
Вопрос 29. Динамический и статический методы построения диаграмм состояния.
Сущность динамич методапостроения диа состояния состоит в построении методом термического анализа кривых охлаждения(или наревания) образцов в координатах температура- время. Получают эти кривые термическим анализом, при котором фиксируются температурные области протекания процессов, идущих с поглощением или выделением тепла (изменением энтальпии системы). Поскольку практически все фазовые превращения сопровождаются изменением теплосодержания системы, на кривых нагревания или охлаждения должны проявляться все процессы, происходящие в системе при изменении температуры: плавление, кристаллизация, разложение, полиморфные превращения и т.п. Кривые, получаемые при постоянной скорости изменения температуры печи, в которой находится исследуемая смесь, показывают ускорение или замедление скорости изменения температуры вещества в зависимости от того, выделяется или поглощается тепло при фазовых превращениях. Установленные таким путем температурные точки фазовых переходов переносят на диаграмму “концентрация – температура”, соединяя общей линией соответственно температуры ликвидуса, солидуса и т.д. К сожалению, несмотря на простоту этого метода,его не всегда можно применять к силикатнымсистемам из-за замедленности фазовых превращений и склонности к переохлаждению.
Статический метод, или метод закалки, наиболее точный и надежный применительно к большинству силикатных систем. Заключается он в следующем. Смесь заданного состава предварительно многократно спекают или плавят и измельчают для обеспечения высокой степени гомогенности. Затем небольшую навеску приготовленной смеси (обычно 0,2-0,5 г) заворачивают в платиную фольгу и помещают в печь, нагретую до заданной температуры. При длительной выдержке в печи в пробе устанавливается равновесное для данной температуры состояние, которое контролируется повторным нагревом пробы при больших длительностях выдержки и сохранением фазового состава образца. Потом пробу подвергают резкой закалке, сбрасывая ее в холодную инертную жидкость. При таком охлаждении жидкая фаза, содержащаяся в образце при исследуемой температуре, застывает в виде стекла, а кристаллические фазы фиксируются в том же состоянии, в каком они были во время выдержки. Исследуя закаленную пробу с помощью поляризационного микроскопа и рентгенофазового анализа, определяют количество и природу фаз, сосуществовавших при температуре опыта.
Последовательно повышая или понижая температуру, при которой образец выдерживается в печи, можно достаточно точно установить момент исчезновения жидкой фазы или температуру полного плавления смеси. Найденные для разных составов температуры дают серию точек, соответствующих кривым ликвидуса, солидуса и полиморфных превращений.
Вопрос 30.
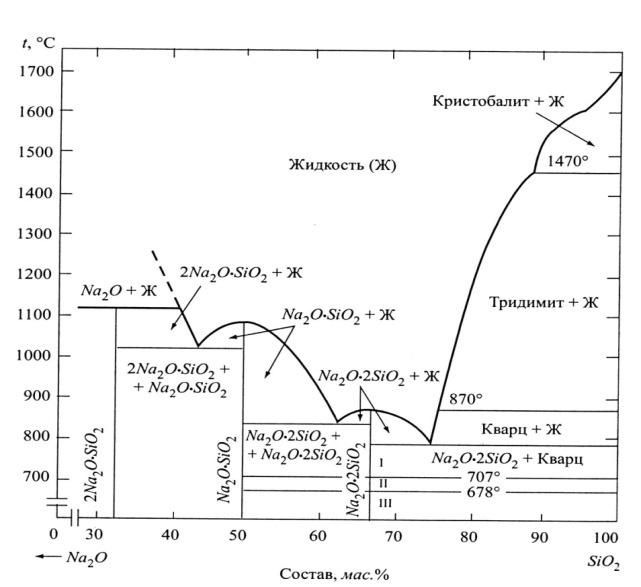
В этой части системы существуют следующие двойные соединения: ортосиликат натрия 2Na2O·SiO2,метасиликат натрияNa2O·SiO2 идисиликат натрия Na2O·2SiO2.
Ортосиликат натрия плавится инконгруэнтно при 1118°С, разлагаясь на жидкость состава 59,3% (маc.) Na2Oи 40,7% (маc.) SiO2и кристаллы Na2O, мета- и дисиликаты натрия плавятся конгруэнтно: первый при 1089°С и второй при 874°С.
Дисиликат натрия имеет несколько полиморфных разновидностей: на диаграмме состояния они обозначены I,IIиIII. Соединения системы Na2O-SiO2 по сравнению с большинством других силикатных соединений весьма легкоплавкие. Диаграмма Na2O-SiO2 является ярким примером того, насколько сильно может понижаться температура плавления смесей за счет образования эвтектик. Например, температура ликвидуса снижается от 1728°С для чистого SiO2до 790 °С. Это позволяет получать в этой системе различные легкоплавкие стекла. Диаграмма состояния системы
имеет специальное значение для технологии изготовления натриевых растворимых (жидких) стекол, представляющих собой стеклообразные силикаты натрия переменного состава с общей формулой Na2O·mSiO2.
Жидкое стекло используется для различных целей: как связующее (клеящее) вещество, как компонент кислотостойких цементов, как основа для силикатных красок, как ПАВ для разжижения глинистых суспензий, для укрепления грунтов, как вяжущее в формовочных смесях в литейном производстве и т.д.
