
- •Вопрос 4. Структурная классификация полиморфизма
- •Вопрос 6. Твердые растворы
- •Вопрос 9. Признаком краевой дислокации является наличие в одной части кристалла лишней («оборванной» или «недостроенной») атомной плоскости, не имеющей продолжения в другой части кристалла.
- •Вопрос 11. Свойства дислокаций:
- •Вопрос 12. Гипотезы строения жидкостей .
- •Вопрос 14. Фх особенности стеклообразного сост-я:
- •Вопрос 15. Процесс стеклообразования определяется следующими факторами:
- •Вопрос 16.
- •Вопрос 17. Устойчивость и коагуляция коллоидных силикатных систем
- •Вопрос 18. Структуры, образующиеся в высокодисперсных системах, п. А. Ребиндер предложил классифицировать:
- •Вопрос 22. Общий вид диаграммы состояния однокомпонентной системы
- •Вопрос 23.
- •Вопрос 24.
- •Вопрос 25. Двухкомпонентные диаграммы состояния
- •Вопрос 26. Диаграмма состояния двухкомпонентной системы с химическим соединением, плавящимся без разложения (конгруэнтно).
- •Вопрос 27.
- •Вопрос 28. Диаграмма состояния двухкомпонентной системы с непрерывным рядом твердых растворов.
- •Вопрос 29. Динамический и статический методы построения диаграмм состояния.
- •Вопрос 30.
- •Вопрос 31.
- •Вопрос 32. Система MgO—SiO2
- •Вопрос 33. Система а12o3— SiO2
- •Вопрос 34. Трехкомпонентные диаграммы состояния
- •Вопрос 36. Диагр.Сост. Трехкомп.Сист. С эвтектикой.
- •Вопрос 37.
- •Вопрос 39.
- •Вопрос 40. Диаграмма состояния трехкомпонентной системы с тройным химическим соединением, плавящимся конгруэнтно, полиморфными превращениями и ликвацией.
- •Вопрос 42. Система Na2o-CaO-SiO2
- •Вопрос 43. Система CaO-Al2o3-SiO2
- •Вопрос 44. Система MgO- Al2o3- SiO2
- •Вопрос 45. Система СаО—MgO — SiO2
- •Вопрос 46. Диссоциация –химический процесс распада молекул, радикалов, ионов на несколько частиц, имеющих меньшую молекулярную массу.
- •Вопрос 47. Дегидратация.
- •Вопрос 49.
- •Вопрос 50. Особенности твердофазовых реакций:
- •Вопрос 51. Кинетика твердофазовых реакций
- •Вопрос 52. Факторы, влияющие на скорость твердофазовых реакций:
- •Вопрос 54. Жидкостное спекание.
- •Вопрос 55. Твердофазовое спекание. Осуществляется под действием температуры за счет переноса вещества в твердой фазе в отсутствие жидкости и без участия газовой фазы.
- •Вопрос 56. Кинетика твердофазового спекания.
- •Вопрос 57. Спекание за счет процесса “испарние — конденсация”
- •Вопрос 58. Первичная Рекристаллизация.
- •Вопрос 59. Вторичная рекристаллизация.
- •Вопрос 61. Кристаллизация.
- •Вопрос 62. Гомогенное образование центров кристаллизации
- •Вопрос 63. Гетерогенное образование центров кристаллизации.
- •Вопрос 66. Структура и классиф полимеров
- •Вопрос 67. Химическое строение макромолекул
- •Вопрос 68. Особенности линейных, разветвленных и сетчатых полимеров
- •Вопрос 69. Способы получения полимеров.
- •Вопрос 70. Карбоцепные полимеры
- •Вопрос 72. Старение и стабилизация полимеров.
- •Вопрос 73. Физическая Структура Полимеров.
- •Вопрос 74.Агрегатные и фазовые состояния полимеров
- •Вопрос 75. Аморфное состояние полимеров.
- •Вопрос 78. Химический состав древесины.
- •Вопрос 79. Под макроскопическим строением (макроструктурой) древесины понимают детали структуры, которые можно исследовать невооруженным глазом и с помощью лупы.
- •Вопрос 80. Анатомическое строение древесины
Вопрос 63. Гетерогенное образование центров кристаллизации.
Образование центров кристаллизации значительно облегчается, если в переохлажденной жидкости присутствует другая фаза (твердые частицы, пылинки, капельки несмешивающейся жидкости другого состава и т.д.), образующая поверхности раздела с жидкой фазой. Наличие в жидкости готовой поверхности раздела существенно уменьшает энергию активации процесса зародышеобразования — при непременном, однако, условии, что жидкость смачивает поверхность посторонней фазы. По Фольмеру, энергию активации ΔG''mах процесса гетерогенного зародышеобразования можно выразить в виде:
ΔG''mах = ΔG'mах.·f(θ),
где ΔG'mах— энергия активации процесса гомогенного зародышеобразования;
f(θ)— функция от краевого угла смачивания.
Если зародыш представляет собой шаровой сегмент, то f(θ).—(функция Фольмера) равна:
![]()
Соответственно:
![]()
Если жидкость абсолютно не смачивает поверхность посторонней фазы, то θ = 180°, cosθ = -1 и ΔG''mах=ΔG'max, т.е. в этом случае присутствие посторонней фазы не оказывает никакого влияния на образование центров кристаллизации, которое будет происходить точно так же, как и при гомогенном зародышеобразовании. При любом значении θ >180° (т.е. при наличии какой-то степени смачивания) ΔG''mахвсегда будет меньшеΔG'max, т.е. энергия активации процесса гетерогенного зародышеобразования всегда меньше, чем гомогенного. Например, при θ= 60° величина ΔG''mахбудет составлять около 1/6 ΔG'mах,а при абсолютном смачивании (θ= 0°,cos0 = 1) ΔG''mахбудет равна нулю, т.е. системе вообще не надо затрачивать никакой энергии на зародышеобразование и этот процесс может начаться уже при ничтожно малом пересыщении.
Все это связано с тем, что при гетерогенном зароды преобразовании не нужно тратить энергию на образование новой поверхности раздела фаз, она уже существует в системе в виде какой-то посторонней фазы. Весьма важным является вопрос о влиянии природы посторонней фазы(затравки) на гетерогенное зародышеобразование.
наиболее эффективными затравками, выполняющими роль центров кристаллизации, могут служить:
1) частицы кристаллизующегося вещества;
2) частицы другого вещества, изоморфного с кристаллизующимся;
3) частицы, дающие с кристаллизующимся веществом закономерно ориентированные сростки (эпитаксии);
4) частицы вещества, которые легко адсорбируют на своей поверхности атомы кристаллизующегося вещества.
Искусственное введение в жидкость или расплав примесей облегчает зародышеобразование и кристаллизацию и позволяет изменять структуру закристаллизованного материала.
Вопрос 64. В последние годы способ введения примесей — искусственных зародышеобразователей — нашел применение в технологии новых стеклокристаллических материалов— ситаллов, применительно к которым эти примеси условно называются катализаторами кристаллизации. Исследование механизма действия катализаторов кристаллизации показало, что вопрос о требованиях, которым должен отвечать катализатор, достаточно сложен и далеко не всегда эффективность действия затравки связана с описанными выше требованиями. Обнаружено, в частности, что действие катализатора кристаллизации при получении ситаллов может быть весьма разнообразным: металлы, например, сами образуют зародыши будущей кристаллической фазы, а действие катализаторов оксидного типа часто связано с микроликвацией жидкости (расслоением на две несмешивающиеся жидкости), что обеспечивает появление поверхности раздела фаз и облегчает появление центров кристаллизации.
Вопрос 65. Кристаллизация представляет собой фазовое превращение, в результате которого из структурно неупорядоченной фазы — газа, раствора, расплава, аморфного твердого тела образуется структурно упорядоченная кристаллическая фаза.
Например,при обжиге портландцементного клинкера образование основного минерала цемента —алита, происходит путем его кристаллизации из расплава. Процесс кристаллизации силикатных расплавов имеет решающее значение и в технологии производства стеклоизделий (позволяет получать эффективные стеклокристаллические материалы —ситаллы).
Кристаллизация может происходитьтолькоиз пересыщенных растворов или переохлажденных расплавов. Расплав, охлажденный нижетемпературы ликвидусабез образования кристаллической фазы, называется переохлажденным и представляет собой, в сущности, пересыщенную при данной температуре жидкость.Степень переохлаждения определяется величинойТ0 —T, гдеТ0 — температура ликвидуса,Т— температура, при которой при данных условиях начинается кристаллизация расплава. Переохлажденный расплав является неустойчивой системой, так как обладает по сравнению с кристаллическим состоянием избытком свободной энергии. Тенденция к уменьшению этой энергии проявляется в самопроизвольномпереходе системы в стабильное кристаллическое состояние.
Кристаллизация начинается из центров кристаллизации — зародышей новой фазы, рост которых в дальнейшем приводит к образованию кристаллического тела.
Образование центров кристаллизации: сущность процесса заключается в возникновении в переохлажденной жидкости микрообластей (микрообъемов) с более упорядоченным, чем в жидкости, и определенным образом ориентированным по отношению друг к другу расположением частиц.
Зародыш еще не является кристаллом. Это квазикристаллические образования в виде динамичных ассоциаций частиц кристаллизующегося вещества, которые под воздействием теплового движения могут распадаться в одних микрообъемах и возникать в других. Собственно центрами кристаллизации будут являтьсятакие зародышис определенным минимальным (критическим) размером, которые в дальнейшем могут самопроизвольно расти, образуя кристалл.
Различают два процесса образования центров кристаллизации: гомогенный (спонтанный)(без раздела фаз. Зародыши того же состава, что и кристаллы) игетерогенный (в этом случае зародыш может иметь другой состав, чем состав выпадающих кристаллов).
Рост кристаллов. После образования в переохлажденной жидкости устойчивого зародыша начинается его рост за счет постепенного отложения (адсорбции) на его поверхности частиц растворенного вещества с последующим их встраиванием в структуру растущего кристалла.
Дворик кристаллизации— пограничная зона пересыщенного раствора, питающая растущий кристалл.
Молекулярно-кинетическая теория послойного роста кристаллов: Для роста какой-либо грани кристалла необходимо последовательное наращивание на ней отдельных атомных слоев. Для образования нового слоя на грани должен возникнуть двухмерный (толщиной в один атомный слой) зародыш этого слоя в виде группы определенным образом ориентированных атомов, который образует на грани кристалла атомную ступеньку роста.
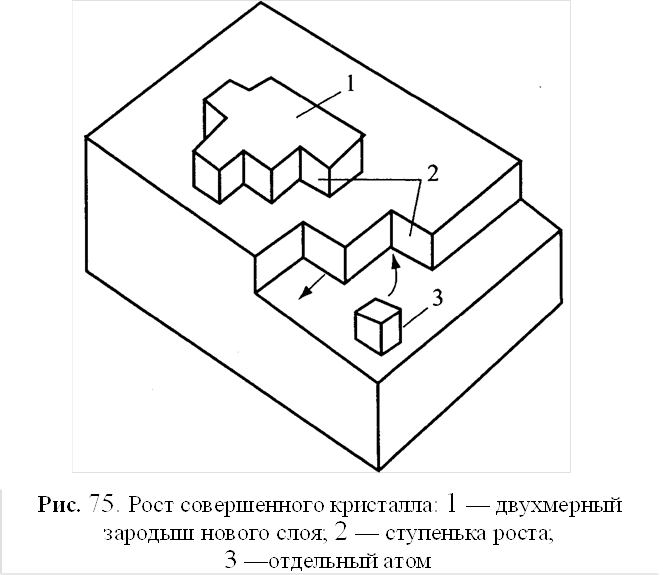
После этого атомы, адсорбированные гранью из окружающей жидкости, мигрируют (диффундируют) по ней и пристраиваются к этой ступеньке, за счет чего она разрастается и заполняет всю грань, образуя новый атомный слой. Затем процесс повторяется, т.е. на этом слое должен возникнуть новый зародыш, который, разрастаясь, образует новый атомный слой, и т.д. Следует подчеркнуть, что если второй процесс — миграция атомов по грани и пристраивание к ступеньке протекает сравнительно легко, то процесс образования зародыша нового слоя требует очень большой энергии активации, поэтому процесс может происходить только в очень сильно пересыщенных или переохлажденных растворах и расплавах.
При наличии в кристалле дефекта решетки — винтовой дислокации — ее выход на поверхность грани кристалла образует на ней атомную ступеньку, которая играет при росте кристалла роль зародыша нового слоя. Атомы, попадающие на грань кристалла, мигрируют к этой ступеньке и пристраиваются к ней, за счет чего происходит ее перемещение в плоскости грани. Ступенька «закреплена» на грани кристалла в месте выхода линии дислокации, проходящей через ее основание перпендикулярно плоскости грани, поэтому при достраивании атомами она начинает вращаться вокруг линии дислокации, наращивая (навивая) на грань кристалла все новые и новые атомные слои.
Большое значение для кинетики и характера кристаллизации имеет соотношение между скоростью образования центров кристаллизации и линейной скоростью роста кристаллов.
МОДУЛЬ 4
