
- •Вопрос 4. Структурная классификация полиморфизма
- •Вопрос 6. Твердые растворы
- •Вопрос 9. Признаком краевой дислокации является наличие в одной части кристалла лишней («оборванной» или «недостроенной») атомной плоскости, не имеющей продолжения в другой части кристалла.
- •Вопрос 11. Свойства дислокаций:
- •Вопрос 12. Гипотезы строения жидкостей .
- •Вопрос 14. Фх особенности стеклообразного сост-я:
- •Вопрос 15. Процесс стеклообразования определяется следующими факторами:
- •Вопрос 16.
- •Вопрос 17. Устойчивость и коагуляция коллоидных силикатных систем
- •Вопрос 18. Структуры, образующиеся в высокодисперсных системах, п. А. Ребиндер предложил классифицировать:
- •Вопрос 22. Общий вид диаграммы состояния однокомпонентной системы
- •Вопрос 23.
- •Вопрос 24.
- •Вопрос 25. Двухкомпонентные диаграммы состояния
- •Вопрос 26. Диаграмма состояния двухкомпонентной системы с химическим соединением, плавящимся без разложения (конгруэнтно).
- •Вопрос 27.
- •Вопрос 28. Диаграмма состояния двухкомпонентной системы с непрерывным рядом твердых растворов.
- •Вопрос 29. Динамический и статический методы построения диаграмм состояния.
- •Вопрос 30.
- •Вопрос 31.
- •Вопрос 32. Система MgO—SiO2
- •Вопрос 33. Система а12o3— SiO2
- •Вопрос 34. Трехкомпонентные диаграммы состояния
- •Вопрос 36. Диагр.Сост. Трехкомп.Сист. С эвтектикой.
- •Вопрос 37.
- •Вопрос 39.
- •Вопрос 40. Диаграмма состояния трехкомпонентной системы с тройным химическим соединением, плавящимся конгруэнтно, полиморфными превращениями и ликвацией.
- •Вопрос 42. Система Na2o-CaO-SiO2
- •Вопрос 43. Система CaO-Al2o3-SiO2
- •Вопрос 44. Система MgO- Al2o3- SiO2
- •Вопрос 45. Система СаО—MgO — SiO2
- •Вопрос 46. Диссоциация –химический процесс распада молекул, радикалов, ионов на несколько частиц, имеющих меньшую молекулярную массу.
- •Вопрос 47. Дегидратация.
- •Вопрос 49.
- •Вопрос 50. Особенности твердофазовых реакций:
- •Вопрос 51. Кинетика твердофазовых реакций
- •Вопрос 52. Факторы, влияющие на скорость твердофазовых реакций:
- •Вопрос 54. Жидкостное спекание.
- •Вопрос 55. Твердофазовое спекание. Осуществляется под действием температуры за счет переноса вещества в твердой фазе в отсутствие жидкости и без участия газовой фазы.
- •Вопрос 56. Кинетика твердофазового спекания.
- •Вопрос 57. Спекание за счет процесса “испарние — конденсация”
- •Вопрос 58. Первичная Рекристаллизация.
- •Вопрос 59. Вторичная рекристаллизация.
- •Вопрос 61. Кристаллизация.
- •Вопрос 62. Гомогенное образование центров кристаллизации
- •Вопрос 63. Гетерогенное образование центров кристаллизации.
- •Вопрос 66. Структура и классиф полимеров
- •Вопрос 67. Химическое строение макромолекул
- •Вопрос 68. Особенности линейных, разветвленных и сетчатых полимеров
- •Вопрос 69. Способы получения полимеров.
- •Вопрос 70. Карбоцепные полимеры
- •Вопрос 72. Старение и стабилизация полимеров.
- •Вопрос 73. Физическая Структура Полимеров.
- •Вопрос 74.Агрегатные и фазовые состояния полимеров
- •Вопрос 75. Аморфное состояние полимеров.
- •Вопрос 78. Химический состав древесины.
- •Вопрос 79. Под макроскопическим строением (макроструктурой) древесины понимают детали структуры, которые можно исследовать невооруженным глазом и с помощью лупы.
- •Вопрос 80. Анатомическое строение древесины
Вопрос 50. Особенности твердофазовых реакций:
1. Направление химической реакциив смесях твердых веществ может не совпадать с направлением реакции в жидкой фазе. Например, в обычных условиях в водных растворах угольная кислота сильнее кремниевой, а при твердофазовом взаимодействии кремниевая кислота вытесняет угольную из ее солей.
2. Процесс взаимодействия твердых компонентов имеетступенчатый характер.
Например, в системе CaO—SiО2при любом молярном соотношении СаО/ SiО2в исходной смеси вначале всегда образуется ортосиликат кальция 2СаО·SiО2. На рис. 83 изображена, например, последовательность образования соединений в смеси СаО и SiО2с соотношенем СаО/ SiО2= 1:1 при 1200°С. Вначале образуется 2СаО·SiО2 количество которого на первой стадии реакции непрерывно увеличивается, достигая максимума, после чего начинает падать за счет взаимодействия с SiО2и образования конечного продукта реакции — метасиликата кальция СаО·SiО2. Кроме 2СаО·SiО2 в качестве промежуточного продукта в этой системе образуя также соединение 3СаО·2SiО2.
3.Твердофазовые реакциивсегда идут с выделением тепла,т.е. являются экзотермическими.
4. Если при твердофазовом взаимодействии не образуются твердые растворы и не возникает значительных количеств газовой и жидкий фаз, то термодинамическоое равновесие в реакции практически не может быть достигнуто, т.е. реакция идет в одном направлении до конца, пока не будет полностью израсходован по крайней мере один из реагирующих компонентов.
Вопрос 51. Кинетика твердофазовых реакций
Зависимость описывающая кинетику твердофазовых реакций, характеризуют изменение во времени количества веществ, участвующих в реакции. Получить какое-то общее уравнение для указанной зависимости, пригодное для всей реакции в целом, без ряда допущений и упрощений вряд ли возможно. Это связано с тем, что твердофазовые реакции складываются из ряда стадий, кинетика которых описывается различными закономерностями. Вначале скорость твердофазового взаимодействия может определяться скоростью химического взаимодействия между компонентами, а впоследствии — скоростью процесса диффузии.
Уравнение Яндера,
для стадии твердофазовой реакции, контролируемой процессом диффузии, имеет для изотермических условий вид:
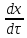 =D
=D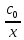
Где х — толщина слоя продукта реакции на покрываемом, менее подвижном компоненте;τ— время;D — коэффициент диффузии при данной температуре; с0— концентрация диффундирующего компонента на границе со слоем продукта реакции.
Принимая величины D и с0постоянными и обозначаяDc=kпосле интегрирования уравнения Яндера получаем:x2 = 2kτ
т.е. в изотермических условиях квадрат толщины слоя продукта реакции пропорционален времени.
Т.к. измерить толщину слоя трудно, Яндер изменил ур-ие:
![]() Гдеy-степень превращения
покрываемого компонента, т.е. его
количество, вошедшее в реакцию,мас.%;
k -постоянная.
Гдеy-степень превращения
покрываемого компонента, т.е. его
количество, вошедшее в реакцию,мас.%;
k -постоянная.
Применимость уравнения проверяется с
помощью графического построения
зависимости величины (l-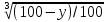 )2от τ, которая должна быть прямой,
проходящей через начало координат.
Линейный ход этой зависимости указывает
на правомерность. В ряде случаев, особенно
для больших значенийτ это уравнение
оказалось неприменимым, Т.к. вывод
исходного уравнения (1) был сделан исходя
из предположения о том, что диффузия
происходит через плоский слой продукта
реакции. Последующее распространение
этого положения на сферические частицы
является формальным и не совсем
правомерным. Оно справедливо на
начальных стадиях реакции при малых
(от 10 до 40%) степенях превращения
компонентов. Именно к таким случаям
относится большинство экспериментальных
данных Яндера.
)2от τ, которая должна быть прямой,
проходящей через начало координат.
Линейный ход этой зависимости указывает
на правомерность. В ряде случаев, особенно
для больших значенийτ это уравнение
оказалось неприменимым, Т.к. вывод
исходного уравнения (1) был сделан исходя
из предположения о том, что диффузия
происходит через плоский слой продукта
реакции. Последующее распространение
этого положения на сферические частицы
является формальным и не совсем
правомерным. Оно справедливо на
начальных стадиях реакции при малых
(от 10 до 40%) степенях превращения
компонентов. Именно к таким случаям
относится большинство экспериментальных
данных Яндера.
A.M. Гинстлинг и Б.И. Броунштейнучли сферичность реагирующих зерен в смеси, и предложили следующее уравнение:
1- 2/3G-(1-G)2/3 = k''τ,
где G — степень превращения покрываемого компонента в долях единицы;τ— время;kпостоянная.
Уравнение дает более точные результаты, особенно при больших степенях превращения компонентов и больших значениях τ.
Уравнения основанные на одном и том же исходном положении: скорость твердофазовой реакции обратно пропорциональна толщине слоя продукта реакции, были получены исходя из предположения об образовании продукта реакции путем односторонней диффузии покрывающего компонента в глубь зерен покрываемого компонента.
