
- •Вопрос 4. Структурная классификация полиморфизма
- •Вопрос 6. Твердые растворы
- •Вопрос 9. Признаком краевой дислокации является наличие в одной части кристалла лишней («оборванной» или «недостроенной») атомной плоскости, не имеющей продолжения в другой части кристалла.
- •Вопрос 11. Свойства дислокаций:
- •Вопрос 12. Гипотезы строения жидкостей .
- •Вопрос 14. Фх особенности стеклообразного сост-я:
- •Вопрос 15. Процесс стеклообразования определяется следующими факторами:
- •Вопрос 16.
- •Вопрос 17. Устойчивость и коагуляция коллоидных силикатных систем
- •Вопрос 18. Структуры, образующиеся в высокодисперсных системах, п. А. Ребиндер предложил классифицировать:
- •Вопрос 22. Общий вид диаграммы состояния однокомпонентной системы
- •Вопрос 23.
- •Вопрос 24.
- •Вопрос 25. Двухкомпонентные диаграммы состояния
- •Вопрос 26. Диаграмма состояния двухкомпонентной системы с химическим соединением, плавящимся без разложения (конгруэнтно).
- •Вопрос 27.
- •Вопрос 28. Диаграмма состояния двухкомпонентной системы с непрерывным рядом твердых растворов.
- •Вопрос 29. Динамический и статический методы построения диаграмм состояния.
- •Вопрос 30.
- •Вопрос 31.
- •Вопрос 32. Система MgO—SiO2
- •Вопрос 33. Система а12o3— SiO2
- •Вопрос 34. Трехкомпонентные диаграммы состояния
- •Вопрос 36. Диагр.Сост. Трехкомп.Сист. С эвтектикой.
- •Вопрос 37.
- •Вопрос 39.
- •Вопрос 40. Диаграмма состояния трехкомпонентной системы с тройным химическим соединением, плавящимся конгруэнтно, полиморфными превращениями и ликвацией.
- •Вопрос 42. Система Na2o-CaO-SiO2
- •Вопрос 43. Система CaO-Al2o3-SiO2
- •Вопрос 44. Система MgO- Al2o3- SiO2
- •Вопрос 45. Система СаО—MgO — SiO2
- •Вопрос 46. Диссоциация –химический процесс распада молекул, радикалов, ионов на несколько частиц, имеющих меньшую молекулярную массу.
- •Вопрос 47. Дегидратация.
- •Вопрос 49.
- •Вопрос 50. Особенности твердофазовых реакций:
- •Вопрос 51. Кинетика твердофазовых реакций
- •Вопрос 52. Факторы, влияющие на скорость твердофазовых реакций:
- •Вопрос 54. Жидкостное спекание.
- •Вопрос 55. Твердофазовое спекание. Осуществляется под действием температуры за счет переноса вещества в твердой фазе в отсутствие жидкости и без участия газовой фазы.
- •Вопрос 56. Кинетика твердофазового спекания.
- •Вопрос 57. Спекание за счет процесса “испарние — конденсация”
- •Вопрос 58. Первичная Рекристаллизация.
- •Вопрос 59. Вторичная рекристаллизация.
- •Вопрос 61. Кристаллизация.
- •Вопрос 62. Гомогенное образование центров кристаллизации
- •Вопрос 63. Гетерогенное образование центров кристаллизации.
- •Вопрос 66. Структура и классиф полимеров
- •Вопрос 67. Химическое строение макромолекул
- •Вопрос 68. Особенности линейных, разветвленных и сетчатых полимеров
- •Вопрос 69. Способы получения полимеров.
- •Вопрос 70. Карбоцепные полимеры
- •Вопрос 72. Старение и стабилизация полимеров.
- •Вопрос 73. Физическая Структура Полимеров.
- •Вопрос 74.Агрегатные и фазовые состояния полимеров
- •Вопрос 75. Аморфное состояние полимеров.
- •Вопрос 78. Химический состав древесины.
- •Вопрос 79. Под макроскопическим строением (макроструктурой) древесины понимают детали структуры, которые можно исследовать невооруженным глазом и с помощью лупы.
- •Вопрос 80. Анатомическое строение древесины
Вопрос 32. Система MgO—SiO2
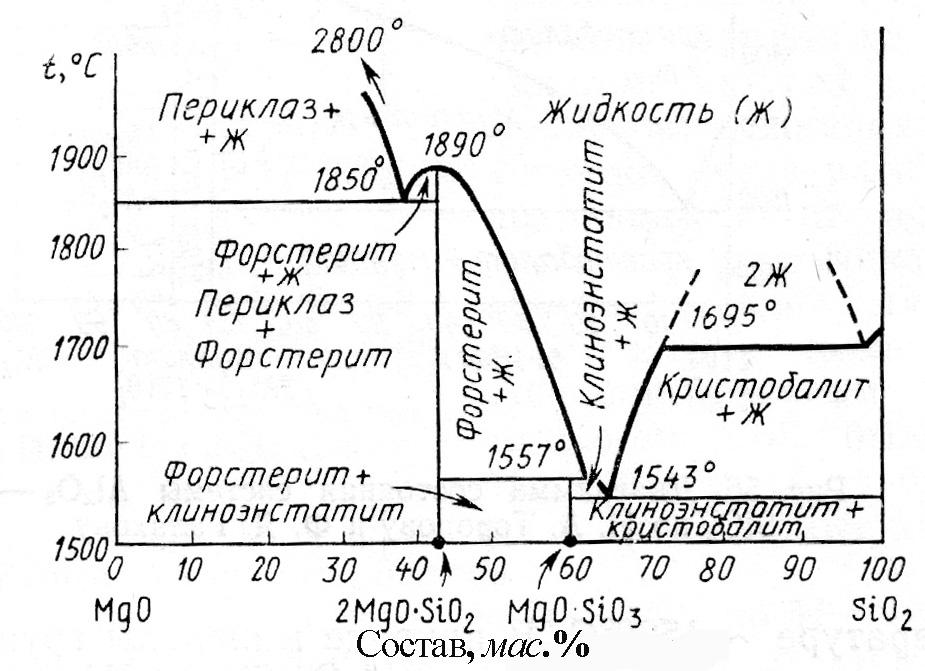
Ортосиликат магния 2MgO·SiO2 (форстерит) — соединение, не имеющее полиморфных разновидностей, плавится конгруэнтно при 1890°С (no другим данным при 1860°С). В природе форстерит встречается главным образом в виде твердых растворов с ортосиликатом оксида железа (II)—фаялитом 2FeO·SiO2, называемых оливинами, состав которых отвечает общей формуле (Mg, Fe)2SiO4. Форстерит с фаялитом образуют непрерывный ряд твердых растворов, в которых форстерит является одним из конечных членов оливинового ряда твердых растворов.
Метасиликат магния MgO·SiO2 плавится инконгруэнтно при1557°С, разлагаясь на жидкость состава 37,5% (мас.) MgO и 62,5% (мас.) ,SiO2и кристаллы 2MgOSiO2. В отличие от ортосиликата метасиликат магния имеет три полиморфные разновидности, называемыеэнстатитом, клиноэнстатитом и протоэнстатитом.
По этой схеме энстатит рассматривается как низкотемпературная форма метасиликата магния, необратимо переходящая при 1260°С в протоэнстатит, а последний при охлаждении превращается не в энстатит, а в клиноэнстатит, который может при соответствующих условиях перейти в энстатит.
По другим данным схема полиморфизма метасиликата магния имеет иной характер. Некоторые вообще отрицают существование протоэнстатита как самостоятельной модификации, рассматривая его как энстатит или клиноэнстатит с дефектной несовершенной решеткой. В природе метасиликат магния встречается чаще всего в виде твердого раствора с FeO-SiO2, входящего в состав распространенных минералов группы пироксенов.
В высококремнеземистых составах системы MgO—SiO2наблюдается явление ликвации, причем при температуре 1695°С в равновесии с кристаллами кристобалита находятся две жидкости: одна, содержащая 0,8% (мас.) MgO и 99,2% (мас.) SiO2, и вторая, содержащая 31,0% (мас.) MgO и 69,0% (мас.) SiO2.
Следует отметить высокую тугоплавкость составов в этой системе. Даже эвтектические составы имеют очень высокие температуры плавления, в частности, эвтектика между MgO и 2MgO·SiO21850°, а эвтектика между MgO·SiO2и SiO21543°С.
Система MgO—SiO2имеет большое значение в керамике для технологии производства различных видов магнезиальных огнеупоров и магнезиальных керамических материалов, в частности оливиновой, форстеритовой, магнезитовой, тальковой, стеатитовой керамики.
Вопрос 33. Система а12o3— SiO2
Система А12O3—SiO2впервые была детально изучена Н. Боуэном и Д. Грейгом, по данным которых, в системе существует только одно бинарное соединение —муллит, состав которого соответствует формуле 3Al2O3·2SiO2. По Н. Боуэну и Д. Грейгу, муллит плавится инконгруэнтно при 1810°С, разлагаясь на корунд α-А12O3и жидкость состава ~45% (мас.) SiO2 и 55% (мас.) А12O3.
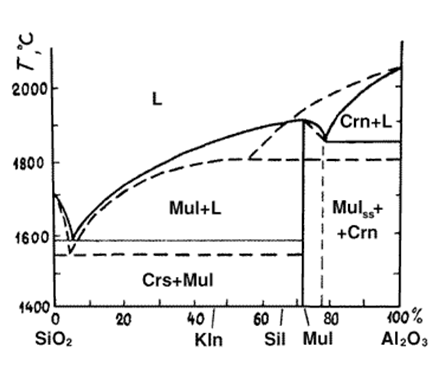 (рис. по Боуэнду и Грейгу)
(рис. по Боуэнду и Грейгу)
Более поздние исследования, проведенные советским учеными Н. А. Тороповым и Ф. Я. Галаховым. было показано, что выделение корунда при плавлении муллита (т. е. его инконгруэнтное плавление) наблюдается только в тех случаях, когда не принимается мер против улетучивания кремнезема при высоких температурах из расплава муллитового состава. В условиях же, когда расплавы предохраняются от возможного частичного улетучивания кремнезема,муллит плавится, не разлагаясь,т. е. характеризуется конгруэнтным плавлением. Кроме того, было обнаружено, что муллит образует с корундом твердые растворы и определена область их существования.
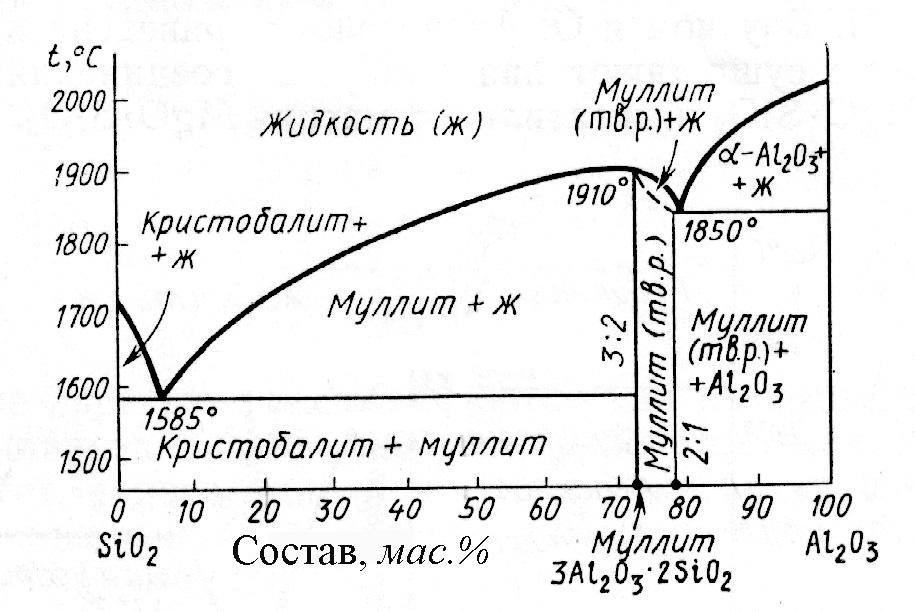 (рис.
по Торопову и Галахову)
(рис.
по Торопову и Галахову)
Согласно этой диаграмме муллит плавится конгруэнтно при 1910°С и образует две эвтектики: одну с SiO2 при 1585°С и вторую (в виде твердого раствора) с А12O3 при 1850°С. Область твердых растворов муллита с корундом простирается от состава муллита (3:2), соответствующего содержанию 71,8% (мас.) А12O3 и 28,2% (мас.) SiO2, до предельного состава (2: 1), соответствующего содержанию ~78% (мас.) Al2O3и 22% (мас.) SiO2.
Особенности системы Al2O3—SiO2:
Прежде всего, нужно обратить внимание на то, что на диаграмме состояния этой системы отсутствует какой-либо максимум на кривой ликвидуса, который бы соответствовал соединению Al2O3·SiO2распространенному в природе в видеминералов группы силлиманита(силлиманит и его разновидности — кианит и андалузит). Это объясняется тем, что при обычном давлении, при котором построены приведенные диаграммы, соединениеAl2O3·SiO2 не имеет области устойчивого равновесного состояния. Однако, как показывают некоторые исследования, при высоких давлениях такие области на диаграмме состояния системыAl2O3—SiO2 появляются.
Другая особенность состоит в весьма пологом характере кривой ликвидуса в области кристаллизации муллита, лежащей влево от его состава. Такой пологий ход кривой ликвидуса обусловливает очень быстрое нарастание содержания жидкой фазы при нагревании смесей, содержащих от 5,5% (мас.) (эвтектика при 1585°С) до ~72% (мас.) Al2O3. Отсюда следует, что при температурах выше 1600°С для составов, содержащих указанное количество AL2O3, содержание жидкой фазы в системе будет очень сильно зависеть от соотношения в образцахAl2O3 и SiO2.
Система Al2O3—SiO2имеет особенно большое значение для технологии производства различных алюмосиликатных огнеупоров и изделий тонкой керамики (фарфора) и интерпретации процессов, протекающих при их обжиге, а также для понимания явлений, происходящих при взаимодействии алюмосиликатных огнеупоров с различными агрессивными средами.
