
- •Вопрос 4. Структурная классификация полиморфизма
- •Вопрос 6. Твердые растворы
- •Вопрос 9. Признаком краевой дислокации является наличие в одной части кристалла лишней («оборванной» или «недостроенной») атомной плоскости, не имеющей продолжения в другой части кристалла.
- •Вопрос 11. Свойства дислокаций:
- •Вопрос 12. Гипотезы строения жидкостей .
- •Вопрос 14. Фх особенности стеклообразного сост-я:
- •Вопрос 15. Процесс стеклообразования определяется следующими факторами:
- •Вопрос 16.
- •Вопрос 17. Устойчивость и коагуляция коллоидных силикатных систем
- •Вопрос 18. Структуры, образующиеся в высокодисперсных системах, п. А. Ребиндер предложил классифицировать:
- •Вопрос 22. Общий вид диаграммы состояния однокомпонентной системы
- •Вопрос 23.
- •Вопрос 24.
- •Вопрос 25. Двухкомпонентные диаграммы состояния
- •Вопрос 26. Диаграмма состояния двухкомпонентной системы с химическим соединением, плавящимся без разложения (конгруэнтно).
- •Вопрос 27.
- •Вопрос 28. Диаграмма состояния двухкомпонентной системы с непрерывным рядом твердых растворов.
- •Вопрос 29. Динамический и статический методы построения диаграмм состояния.
- •Вопрос 30.
- •Вопрос 31.
- •Вопрос 32. Система MgO—SiO2
- •Вопрос 33. Система а12o3— SiO2
- •Вопрос 34. Трехкомпонентные диаграммы состояния
- •Вопрос 36. Диагр.Сост. Трехкомп.Сист. С эвтектикой.
- •Вопрос 37.
- •Вопрос 39.
- •Вопрос 40. Диаграмма состояния трехкомпонентной системы с тройным химическим соединением, плавящимся конгруэнтно, полиморфными превращениями и ликвацией.
- •Вопрос 42. Система Na2o-CaO-SiO2
- •Вопрос 43. Система CaO-Al2o3-SiO2
- •Вопрос 44. Система MgO- Al2o3- SiO2
- •Вопрос 45. Система СаО—MgO — SiO2
- •Вопрос 46. Диссоциация –химический процесс распада молекул, радикалов, ионов на несколько частиц, имеющих меньшую молекулярную массу.
- •Вопрос 47. Дегидратация.
- •Вопрос 49.
- •Вопрос 50. Особенности твердофазовых реакций:
- •Вопрос 51. Кинетика твердофазовых реакций
- •Вопрос 52. Факторы, влияющие на скорость твердофазовых реакций:
- •Вопрос 54. Жидкостное спекание.
- •Вопрос 55. Твердофазовое спекание. Осуществляется под действием температуры за счет переноса вещества в твердой фазе в отсутствие жидкости и без участия газовой фазы.
- •Вопрос 56. Кинетика твердофазового спекания.
- •Вопрос 57. Спекание за счет процесса “испарние — конденсация”
- •Вопрос 58. Первичная Рекристаллизация.
- •Вопрос 59. Вторичная рекристаллизация.
- •Вопрос 61. Кристаллизация.
- •Вопрос 62. Гомогенное образование центров кристаллизации
- •Вопрос 63. Гетерогенное образование центров кристаллизации.
- •Вопрос 66. Структура и классиф полимеров
- •Вопрос 67. Химическое строение макромолекул
- •Вопрос 68. Особенности линейных, разветвленных и сетчатых полимеров
- •Вопрос 69. Способы получения полимеров.
- •Вопрос 70. Карбоцепные полимеры
- •Вопрос 72. Старение и стабилизация полимеров.
- •Вопрос 73. Физическая Структура Полимеров.
- •Вопрос 74.Агрегатные и фазовые состояния полимеров
- •Вопрос 75. Аморфное состояние полимеров.
- •Вопрос 78. Химический состав древесины.
- •Вопрос 79. Под макроскопическим строением (макроструктурой) древесины понимают детали структуры, которые можно исследовать невооруженным глазом и с помощью лупы.
- •Вопрос 80. Анатомическое строение древесины
Вопрос 22. Общий вид диаграммы состояния однокомпонентной системы

правило фаз однокомпонентных систем в виде f = К+2—Р=3-P.
Основным элементом строения однокомпонентных диаграмм состояния являются линии упругости пара (линии АВ, ВС, CD,BE,CF).ОбластиABE, FCD, EBCF являются однофазными и согласно правилу фаз для однокомпонентных систем дивариантны,т. е. в границах этих областей можно произвольно менять температуру и давление, не нарушая равновесие в системе, т. е. не изменяя число и состав фаз.
Вдоль линий упругости пара АВ, ВС, CD,BEиCF, разделяющих области существования отдельных фаз, в равновесии находятся соответственно по две фазы: твердая фазаK1—пар (АВ), твердая фаза К2— пар (ВС), жидкость — пар (CD), твердая фазаK1— твердая фаза К2(BE) и твердая фаза Кг— жидкость (CF). Точкам этих линий соответствуетмоновариантное состояние системы, т. е. можно изменять произвольно без нарушения равновесия только какой-либо один параметр системы, например температуру, при этом второй зависимый параметр системы (давление) в соответствии с изменением температуры будет принимать строго определенное значение. Фигуративная точка, выражающая состояние системы, будет перемещаться при этом вдоль линий упругости пара. Каждая полиморфная модификация имеетсвоюобласть температур и давлений, в которой она существует в стабильном (равновесном) состоянии и никакая другая модификация этого же вещества в той же области стабильной быть не может. Это следует из того, что стабильная равновесная форма кристаллического вещества должна иметь минимальную энергию Гиббса. Однако в области стабильности какой-либо полиморфной формы кристаллического вещества другие модификации могут существовать в метастабильном состоянии. КриваяGBбудет являться линией упругости пара модификации К2, существующей в метастабильном состоянии в области стабильного существования формы К1.
В тройных точках В и С в равновесии находятся три фазы (К1К2и газообразная фаза в точке В; К2, жидкая и газообразная фазы в точке С), поэтому в соответствии с правилом фаз при параметрах, соответствующих этим точкам, система инвариантна, т. е. для сохранения состояния равновесия все параметры системы (в данном случае температура и давление) должны быть строго фиксированы.Все точки линий упругости пара, включая инвариантные точки В и С,характеризуют собой параметры (температуру и давление), при изменении которых одна фаза превращается в другую. Например, линияBEопределяет температуру и соответствующее ей давление, при изменении которых происходит энантиотропный переход К1↔К2, линияCFсоответствует переходу К2↔жидкость (расплав), т. е. определяет собой при данном давлении температуру плавления твердой фазы К2.
Угол наклона линий упругости параBEиCFк оси температур зависит от характера изменения удельного объема и, следовательно, плотности при фазовых превращениях. Тангенс угла наклона этих линий к оси температур равенdp/dT. В соответствии с уравнением Клаузиуса—Клапейрона
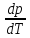 =
=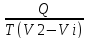
Отсюда следует, что если высокотемпературная фаза имеет меньший удельный объем, т. е. большую плотность, то с повышением давления температура фазового перехода падает, т. е. увеличение давления ускоряет фазовое превращение (угол наклона соответствующей линии упругости пара тупой). Это, например, имеет место при фазовом переходе «лед ↔вода».
Тройная точка Схарактеризует температуруT3 плавления в трехфазной системе (твердая, жидкая и газообразная фазы) кристаллической модификации К2Температура плавления Т2низкотемпературной модификации К1будет определяться точкой Н пересечения продолжения линии АВ упругости пара этой модификации с линиейCDупругости пара жидкости. Однако это будет температураметастабильного плавления. Перевести модификациюK1непосредственно в расплав в неравновесных условиях иногда можно, например, за счет очень быстрого нагревания, при котором структура низкотемпературной формыK1не успевает перейти в структуру высокотемпературной формы К2 .Температура метастабильного плавления всегда ниже температуры плавления этого вещества в равновесных условиях.
