
- •О. А. Голубчиков
- •Органический практикум
- •Санкт-Петербург
- •Нии химии сПбГу – 2012
- •Оглавление
- •Предисловие
- •1. Общие правила и методы работы
- •1.1. Планирование работ и ведение рабочего журнала
- •1.1.1. Форма ведения записей в лабораторном журнале
- •1.1.2. Пояснения к составлению таблиц
- •1.1.3. План экспериментальной работы. Отчет о выполнении работы
- •1.2. Правила техники безопасности в лаборатории органического синтеза
- •1.2.1. Общие правила работы
- •1.2.2. Правила обращения с ядовитыми и едкими веществами
- •1.2.3. Правила при работе с огнеопасными веществами
- •1.2.4. Правила при работах, которые могут сопровождаться взрывами или выбросами веществ
- •1.2.5. Правила обращения со стеклом
- •1.3. Основные методы выделения и очистки органических соединений
- •1.3.1 Перекристаллизация Принцип метода
- •Подбор растворителя
- •Практика проведения перекристаллизации
- •Обесцвечивание горячих насыщенных растворов
- •Фильтрование с отсасыванием
- •Сушка органических веществ
- •Определение температуры плавления вещества
- •Контрольные вопросы
- •1.3.2. Перегонка органических жидкостей
- •1.3.2. Простая перегонка при атмосферном давлении
- •Перегонка при уменьшенном давлении (под вакуумом)
- •Перегонка с водяным паром
- •Фракционная перегонка и перегонка с дефлегматором
- •Контрольные вопросы
- •1.3.3. Хроматография
- •Газо-жидкостная хроматография
- •Тонкослойная и бумажная хроматография
- •Нуклеофильное замещение у sp3-гибридизованного атома углерода
- •Нуклеофильное замещение у sp2-гибридизованного карбонильного углерода
- •Контрольные вопросы
- •2.1.2. Бромистый изопропил
- •Примечания:
- •Пояснения к синтезу
- •Контрольные вопросы
- •2.1.3. Ацетанилид (метод а)
- •2.1.4. Ацетанилид (метод б)
- •Пояснения к синтезу
- •Контрольные вопросы
- •2.1.5. Ацетилсалициловая кислота (аспирин)
- •Пояснения к синтезу
- •Контрольные вопросы
- •Пояснения к синтезу
- •2.2. Электрофильное замещение в ароматическом ряду
- •2.2.1. Основные теоретические положения
- •2.2.2. Нитротолуолы (смесь изомеров)
- •Хроматографическое определение изомерного состава нитротолуолов
- •Пояснения к синтезу
- •Контрольные вопросы
- •Пояснения к синтезу
- •Контрольные вопросы
- •2.2.4. Cульфаниловая кислота
- •Пояснения к синтезу
- •Контрольные вопросы
- •2.3. Восстановление нитросоединений
- •2.3.1. Основные теоретические положения
- •Восстановление металлами в присутствии растворов электролитов
- •Восстановление в кислой среде металлами
- •Пути восстановления нитросоединений в зависимости от pH среды Восстановление в кислой среде
- •Восстановление в щелочной среде
- •Восстановление в щелочной среде растворами сульфидов. Селективное восстановление полинитросоединений
- •Определение конца реакции
- •Выделение продуктов реакции
- •Меры предосторожности при работе с ароматическими аминами
- •2.3.2. Анилин
- •Выделение анилина из реакционной смеси
- •2.3.3. Выделение и идентификация аминов
- •Пояснения к синтезу
- •Экстракция органических веществ из водных растворов
- •Контрольные вопросы
- •2.3.4. Мета-Нитроанилин
- •Пояснения к синтезу
- •Контрольные вопросы
- •2.4. Получение и превращения диазосоединений
- •2.4.1. Основные теоретические положения
- •Получение ароматических диазосоединений
- •Механизм диазотирования
- •Факторы, влияющие на скорость диазотирования
- •Контроль диазотирования
- •Формы диазосоединений
- •Превращения диазосоединений Азосочетание
- •Реакции солей диазония с выделением азота
- •2.4.2. Йодбензол
- •Пояснения к синтезу
- •Пояснения к синтезу
- •Пояснения к синтезу
- •Контрольные вопросы
- •2.4.5. Метилоранж
- •Примечания к синтезу
- •Метиловый оранжевый:
- •2.4.6. Кислотный оранжевый (-нафтолоранж)
- •Азосочетание
- •2.4.7. Резорциновый желтый (тропеолин)
- •Азосочетание
- •2.4.8. Спектрофотометрическое определение содержания красителя в растворе
- •2.4.9. Пояснения к синтезам азокрасителей
- •Контрольные вопросы
- •2.5. Окисление
- •2.5.1. Основные теоретические положения
- •2.5.2. Бензойная кислота (из толуола)
- •Примечание
- •2.5.3. Бензойная кислота (из бензилового спирта)
- •Пояснения к синтезам бензойной кислоты (2.5.2 и 2.5.3)
- •Контрольные вопросы
- •2.5.4. Масляный альдегид (бутаналь)
- •Пояснения к синтезу
- •Контрольные вопросы
- •2.5.5. Бензальдегид
- •Пояснения к синтезу
- •Контрольные вопросы
- •3. Синтез гетероциклических соединений
- •Пояснения к синтезу
- •Пояснения к синтезу
- •Пояснения к синтезу
- •Пояснения к синтезу
- •Бензимидазол
- •Пояснения к синтезу
- •Пояснения к синтезу
- •Хинолин (синтез Скраупа)
- •Пояснения к синтезу
- •Фенилизоиндолизин
- •Пояснения к синтезу
- •Фенотиазин
- •Пояснения к синтезу
- •5,10,15,20-Тетрафенилпорфирины
- •5,10,15,20-Тетрафенилпорфирин
- •Пояснения к синтезу
- •Хроматографическая очистка тетрафенилпорфирина
- •5,10,15, 20-Тетракис(4-нитрофенил)порфирин
- •Пояснения к синтезу
- •5,10,15,20-Тетракис(4-бромфенил)порфирин
- •Приложение
- •Список рекомендуемой литературы
Пояснения к синтезу
При повышенной температуре серная кислота дегидратирует глицерин, образуя непредельный спирт НОСН2СН=СНОН, который перегруппировывается в β-гидроксипропаналь НОСН2СН2СНО и вновь подвергается дегидратации, образуя акролеин СН2=СН-СНО. II
Акролеин, как и другие α,β-ненасыщенные альдегиды, вступает в реакции присоединения против правила Марковникова. Взаимодействуя с анилином, он образует 1-фениламинопропаналь I. Его аминогруппа активирует о-положение бензольного ядра по отношению к действию электрофильного атома углерода альдегидной группы. По отношению к бензольному ядру реакция образования промежуточного соединения II является электрофильным замещением. Под каталитическим и водоотнимающим действием серной кислоты II подвергается дегидратации, образуя III. Наконец, III окисляется до хинолина действием нитробензола, который в свою очередь восстанавливается до анилина, вновь вступает в реакцию с акролеином.
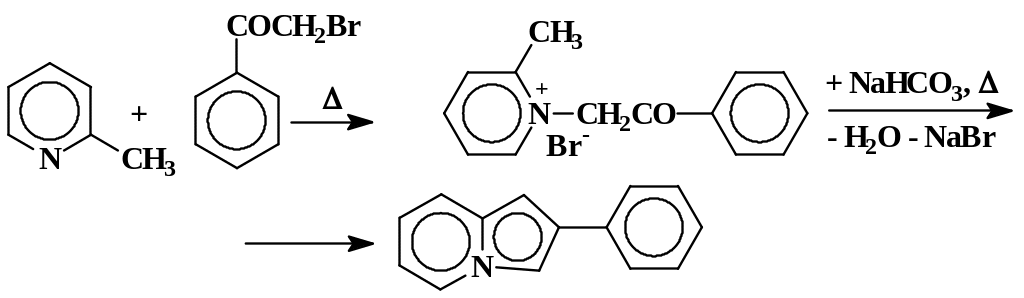
Фенилизоиндолизин
При взаимодействии α-пиколина с фенацилбромидом образуется 2-метил-1-фенацилпиридиний бромид, который при кипячении в воде в присутствии гидрокарбоната натрия превращается в фенилизоиндолизин:
2-Метил-1-фенацилпиридиний бромид. В трехгорлую колбу, снабженную обратным холодильником и мешалкой, вносят 9,3 мл (0,1 моль) α-пиколина и раствор 19,9 г (0,1 моль) фенацилбромида (лакриматор, работать под тягой!) в 20 мл ацетона. Смесь при перемешивании кипятят на водяной бане в течение 2-х часов, и выпавший при охлаждении осадок четвертичной соли отфильтровывают, дважды промывают ацетона и дважды – эфиром, порциями по 10 мл.
Выход 25,7 – 26,8 г (88 – 92 %), tпл 211 °С (с разложением).
Фенилизоиндолизин. Раствор 14,6 г (0,05 моль) 2-метил-1-фенацилпиридиний бромида в 250 мл воды кипятят при перемешивании в присутствии 6,3 г (0,075 моль) гидрокарбоната натрия 40 – 50 минут. Через 20 – 30 мин от начала кипения выпадает обильный белый осадок, который после окончания реакции и охлаждения реакционной смеси, отфильтровывают, трижды промывают ледяной водой, порциями по 20 мл и сушат при 100 °С.
Выход 8,8 – 9,0 г (91 – 93 %). Перекристаллизованный из спирта продукт имеет Тпл 210 – 211 °С.
Пояснения к синтезу
Пиридин сравнительно легко вступает в реакции электрофильного присоединения по атому азота. Бромированый ацетофенон на атоме углерода группы СН2 под электроноакцепторным действием соседнего атома брома и карбонильной группы несет существенный положительный заряд и проявляет свойства электрофила.
В силу электроноакцепторного влияния положительно заряженного азота 2-метил-1-фенацилпиридиний бромид является достаточно сильной СН-кислотой. Кислотный разрыв связи С-Н метильной группы происходит под действием гидрокарбоната натрия:
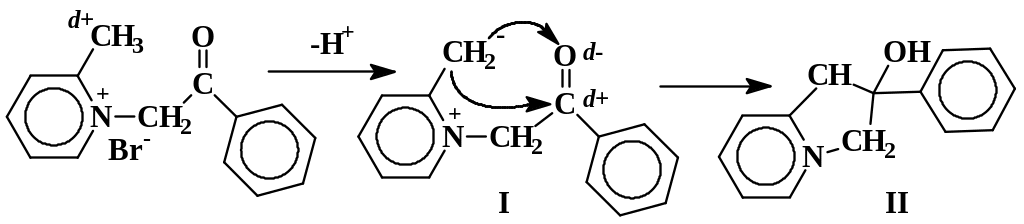
Разумеется, отрицательный заряд в значительной степени мигрирует с группы СН2 на атом азота, но структура I подчеркивает нуклеофильный характер образующегося соединения и демонстрирует суть последующей реакции циклизации с образованием спирта II, дегидратация которого дает конечный продукт – фенилизоиндолизин.
