
- •Химический состав нефтей
- •Классификация нефтей
- •Химические классификации.
- •Геохимические и генетические классификации.
- •Технологические классификации.
- •СВОЙСТВА НЕФТЕЙ
- •Физико-химические свойства нефтей
- •Плотность.
- •Молекулярная масса.
- •Вязкость*.
- •Теплопроводность.
- •Теплоемкость.
- •Теплота испарения.
- •Энтальпия (теплосодержание).
- •Оптическая активность.
- •Электрические свойства.
- •Коллоидные свойства нефтей
- •Коллоидно-дисперсное строение нефтяных систем.
- •ПРОИСХОЖДЕНИЕ НЕФТИ
- •ЛИТЕРАТУРА
- •Перегонка и ректификация
- •Азеотропная ректификация.
- •Экстракция и экстрактивная ректификация.
- •Адсорбционная хроматография
- •Термодиффузия
- •Диффузия через мембраны
- •Кристаллизация и экстрактивная кристаллизация
- •Образование аддуктов и комплексов
- •МЕТОДЫ ВЫДЕЛЕНИЯ И РАЗДЕЛЕНИЯ НЕУГЛЕВОДОРОДНЫХ КОМПОНЕНТОВ
- •Экологические и технологические аспекты выделения
- •Выделение гетероатомных соединений средних фракций
- •Серусодержащие соединения.
- •Образование солей и комплексов.
- •Азотсодержащие соединения.
- •Нейтральные кислородсодержащие соединения.
- •Выделение смолисто-асфальтеновых веществ
- •Разделение смолисто-асфальтеновых веществ
- •ЛИТЕРАТУРА
- •СПОСОБЫ ВЫРАЖЕНИЯ СОСТАВА НЕФТЯНЫХ ФРАКЦИЙ
- •МЕТОДЫ АНАЛИЗА ИНДИВИДУАЛЬНОГО СОСТАВА
- •Газовая хроматография
- •МЕТОДЫ АНАЛИЗА ГРУППОВОГО СОСТАВА
- •Масс-спектрометрия и хромато-масс-спектрометрия
- •Спектральный анализ
- •МЕТОДЫ АНАЛИЗА МИКРОЭЛЕМЕНТОВ
- •МЕТОДЫ СТРУКТУРНО-ГРУППОВОГО АНАЛИЗА
- •Анализ легких и средних фракций
- •Анализ смолисто-асфальтеновых веществ
- •Определение молекулярной массы асфальтенов и смол.
- •Рентгеноструктурный анализ.
- •Структура ароматических фрагментов.
- •Структура циклоалкановых фрагментов.
- •Структура алифатических фрагментов.
- •Структура фрагментов, содержащих гетеро атомы и микроэлементы.
- •Интегральный структурный анализ.
- •ЛИТЕРАТУРА
- •АЛКАНЫ
- •Физические свойства
- •Теплофизические свойства.
- •Фазовые превращения.
- •Физико-химические свойства
- •Химические превращения
- •ЦИКЛОАЛКАНЫ
- •Физические свойства
- •Химические превращения
- •АРЕНЫ
- •Состав аренов нефтей различных месторождений
- •Физико-химические свойства
- •Химические превращения
- •ГЕТЕРОАТОМНЫЕ СОЕДИНЕНИЯ СРЕДНИХ ФРАКЦИИ
- •Серусодержащие соединения
- •СМОЛИСТО-АСФАЛЬТЕНОВЫЕ ВЕЩЕСТВА
- •Физические свойства .
- •Физико-химические свойства
- •Химические превращения
- •МИКРОЭЛЕМЕНТЫ
- •ЛИТЕРАТУРА
- •АЛКАНЫ
- •Природные горючие газы.
- •Жидкие алканы.
- •Твердые алканы.
- •Белки биологического синтеза.
- •ЦИКЛОАЛКАНЫ
- •Циклогексан и продукты его химических превращений.
- •Другие циклоалканы и продукты их химических превращений.
- •АРЕНЫ
- •ГЕТЕРОАТОМНЫЕ СОЕДИНЕНИЯ СРЕДНИХ ФРАКЦИИ
- •Серусодержащие соединения.
- •Азотсодержащие соединения.
- •СМОЛИСТО-АСФАЛЬТЕНОВЫЕ ВЕЩЕСТВА
- •ЛИТЕРАТУРА

АЛКАНЫ
Алканы составляют значительную часть углеводородов нефтей всех месторождений и природных горючих газов.
Содержание алканов меняется в нефтях различных месторождений. Ниже представлено массовое содержание алканов в нефтяном дистилляте, перегоняющемся до 500 °C, нефтей разных месторождений (в %):
Балахнинская |
4,3 |
Грозненская |
23,7 |
Озексуарская |
50,0 |
Ромашкинская, пенсильванская (США), |
|
Южного Борнео (Индонезия) |
Более 50 |
Важнейший источник низкомолекулярных алканов — природные и попутные нефтяные горючие газы [1, 2].
По данным 1975 г. разведанные мировые запасы природного газа, подготовленные к эксплуатации, превышают 50*1012 м3, а прогнозные составляют более 200*1012 м3. Ежегодно в мире добывают свыше 1,5*1012 м3 природного газа. Разведанные и пригодные к эксплуатации запасы природного газа в СССР превышают 15*1012 м3 [3, 4].
В газовых месторождениях содержится природный газ под высоким давлением, достигающим 25—30 МПа, благодаря чему в нем растворены жидкие при нормальных условиях углеводороды с большой молекулярной массой. Содержание конденсата в газе зависит от его состава, пластового давления и температуры. Чем выше температура, тем растворимость жидких углеводородов в газе больше, их содержание в газе отдельных месторождений сильно различается. В основном, конденсата в газе содержится в пределах 40—600 см3/м3 [5]. В газоконденсатных месторождениях с большей глубиной, чем 1500 м, горючий газ и углеводороды находятся в однофазном состоянии — тяжелые компоненты полностью растворены в массе легких газообразных компонентов.
По мере падения давления из газа выделяется конденсат. В первую очередь, конденсируются более тяжелые углеводороды, а затем легкие. Давление, при котором начинается выделение конденсата из газа, называется давлением начала конденсации. Конденсат может выделяться как на поверхности из добытого газа, так и в пласте при снижении давления. В последнем случае он впитывается породой пласта, из-за чего значительная его часть может оставаться в пласте безвозвратно. Из скважины газ с парами более тяжелых углеводородов поступает в конденсатную установку в которой при соответствующих давлении и температуре выделяются жидкие продукты. Полученный «сухой» газ сжимается компрессорами до давления, на 12—20 % превышающего давление в скважинах, и под этим давлением нагнетается через специальные скважины в пласт, что интенсифицирует отбор нефти. Избыток такого газа используют как топливо и химическое сырье.
176
Газовый конденсат представляет смесь бензиновых и кepocино-газойлевых фракций [7]. Он может быть существенной добавкой к моторным топливам, получаемым непосредственно из нефти [6] (табл.48).
ТАБЛИЦА 48. Химический состав природного газа различных месторождений
|
Редкие |
|
Объемное содержание, % |
|
|||
Месторождение |
газы (Не, Ar и |
|
|
|
|
|
|
CH4 |
C2H6 |
C3H8 |
С4 и |
CO2 |
|||
|
др. |
||||||
|
выше |
||||||
|
|
|
|
|
|
||
Чисто газовые |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Уренгойское, Медвежье |
1,5 |
97,9 |
0,2 |
0,1 |
|
0,3 |
|
Дашавское |
0,6 |
98,9 |
0,3 |
— |
— |
0,2 |
|
|
|
|
|
|
|
|
|
Саратовское |
3,0 |
94,7 |
1,8 |
0,2 |
0,1 |
0,2 |
|
Ставропольское |
1,0 |
98,3 |
0,3 |
0,1 |
— |
0,3 |
|
|
|
|
|
|
|
|
|
Газоконденсатные |
|
|
|
|
|
- |
|
Вуктыльское |
4,3 |
79,8 |
8,7 |
3,9 |
8,2 |
0,1 |
|
Газлинское |
1,9 |
94,4 |
2,6 |
0,3 |
0,6 |
0,2 |
|
Шебелинское |
0,8 |
93,3 |
3,5 |
0,9 |
1,4 |
0,1 |
|
Оренбургское |
7,2 |
87,6 |
3,5 |
1,2 |
0,5 |
|
|
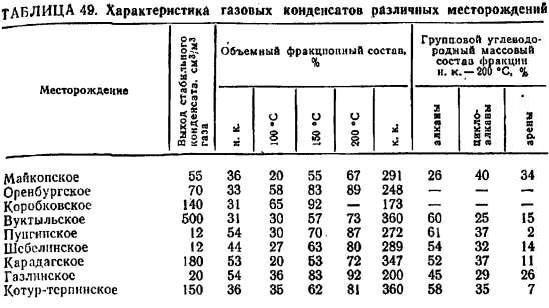
В газах газоконденсатных месторождений, в отличие от газов, чисто газовых месторождений, содержатся различные углеводороды с четырьмя и более атомами в молекуле (табл. 49).
Из данных таблицы следует, что конденсаты на 70—90 % сосстоят из бензиновых фракции (30—200 °C) и на 10—30% из дизельных фракций (200—360 °C).
Однако таким высоким концом кипения характеризуются далеко не все конденсаты. Многие из них полностью перегоняются при температуре значительно ниже 360 °С.
Из нефти и горючих газов выделены все алканы нормального строения, от метана до тритриаконтана (С33Н68) включительно. Их объемное содержание в нефти возрастало от 1,8 для C6 до 2,3 % для С7, а затем постепенно снижалось до 0,09 % для С33 [9]. Формирование алканов в недрах рассматривается в аспекте общего генезиса нефти.
177

Однако известны работы, в которых исследуется вопрос образования алканов самостоятельно. Примером является работа [8], в которой рассматривается возможный путь образования алканов изопреноидной структуры (изодраны).
Изопреноиды имеют строение, характерное для насыщенной цепи полиизопрена, например, 2,6-диметилалканы С9 — C13, или 2,6,10триметилалканы C14—C18, или 2,6,10,14-тетраметилалканы, среди которых наиболее интересные для понимания вопросов генезиса алканов в нефти пристан (C19) и фитан (С20). К числу изопреноидов отчасти могут быть отнесены и 2-метилалканы С4—C8.
Внефтях изопреноидов содержится 2—3%, около 1/3 приходится иа пристан и фитан. Основная их масса сосредоточена во фракции 150—350 °C с изопреиоидами С11 —С20.
Втакой фракции больше всего пристана и фитана, а меньше всего 2,6-диметилдекана и 2,6,10-триметилдодекана.
На рис. 12 приведена предполагаемая схема термокаталитической деструкции фитола С20Н39ОН с образованием алканов изопреноидных структур (фитол, как известно, входит в состав хлорофилла). Закономерное количественное распределение
образовавшихся изопреноидов указывает на фитол, как на |
один из основных |
источников формирования алканов изопреноидного типа, |
а следовательно на |
органический характер их происхождения в составе нефти. |
|
Физические свойства
Атомы углерода в молекулах алканов соединены между собой простыми связями в незамкнутые линейные или зигзагообразные разветвленные цепи, лежащие в одной плоскости. Длина свяей атомов С—С составляет 0,154 нм, С—Н — 0,109 нм, угол между связями С—С—С в газообразном состоянии — 109 °28'. В кристаллическом углеводороде угол на 2°, а в некоторых случаях, больше превышает это значение.
Атомы водорода в группах CH2 расположены попарно в плоскостях, перпендикулярных плоскости зигзагообразной цепи, образованной атомами углерода. Молекула алкана нормального строения представляет собой тетраэдр, в центре которого находится атом углерода, а валентные связи направлены к его вepшинам (рис. 1).
178
В нефти могут присутствовать все возможные изомеры алканов, хотя многие из них в чрезвычайно малых количествах (следы). Больше всего содержится 2-метилизомеров всех типов, за ними следуют 3-метил- и 4-метилизомеры. В любой данной группе изомеров основная часть состоит из изомеров с одним разветвлением. Например, в «средней» нефти США содержание каждого типа изомеров разветвленных алканов С9 содержится с одним разветвлением 0,1 %, с двумя 0,01 %, с тремя 0,001 %, с четырьмя
—следы [9]. Наиболее полно выделены и изучены изоалканы бензиновых фракций.
Различие в свойствах алканов нормального и изомерного строения можно проиллюстрировать на примере температуры кипения. Первые кипят при более высокой температуре, чем изомерные аналоги по молекулярной массе.
|
Tкип. °С |
|
Tкип. °С |
|
|
|
|
|
|
|
|
Гексан |
69 |
Диизопропилметан |
58 |
Метилдиэтилметан |
64 |
Триметилэтилметан |
49 |
Этилизобутилметан |
62 |
|
|
Для образования различных конформаций алканов требуется энергия активации 12,6 кДж/моль, в то время как для изомерии иного типа требуется гораздо большая энергия активации. В случае этана может быть лишь одна устойчивая конформация. Разность энергии между нею и заслоненной формой 11,8 кДж/моль.
Алканы отличаются от углеводородов иного строения относительно большим содержанием водорода в молекуле.
Энергия разрыва связей в молекулах алканов зависит от их природы (в кДж/моль) :
СН3—H - 428,4; CH3CH2—H - 389,9; CH3—CH3 - 333,7
Несмотря на то, что энергия диссоциации связей С—С меньше энергии диссоциации связи С—Н, распад низших алканов (этан, пропан, бутан) происходит по связи С—Н, что объясняется отсутствием стерического фактора. Начиная с пентана распад происходит преимущественно по связям С—С. Большая молекулярная масса и степень разветвления молекулы обусловливает повышение ее реакционной способности. Скорость распада высокомолекулярного алкана по отношению к низкомолекулярному алкану может отличаться на порядок.
Высокие температуры и низкие давления способствуют расщеплению алканов ближе к концам молекулы, с повышенным газообразованием. При умеренных температурах (500 °C) и высоких давлениях место разрыва связи С—С перемещается к середине молекулы, что приводит к увеличению выхода жидких продуктов. Поэтому для получения большего выхода реакционноспособных низкомолекулярных алканов процесс ведут в газовой фазе при высоких температурах и низких давлениях (пиролиз).
Алканы находятся в нефти в молекулярном и ассоциированном состоянии. Энергия межмолекулярного взаимодействия составляет от десятых долей до нескольких килоджоулей на 1 моль, что намного меньше энергии разрыва связей. Алканы, независимо от строения цепи, неполярны. Объясняется это тем, что моменты всех
179
