
- •1. Основные положения статистической термодинамики
- •1.1. Понятия и начала феноменологической термодинамики.
- •1.2. Микроскопическое (механическое) описание классических систем.
- •1.3. Особенности представления квантовых систем
- •1.4. Вероятность нахождения системы в элементе фазового пространства. Метод ансамблей Гиббса.
- •1.5. Макроскопические величины как фазовые средние
- •1.6. Распределение в системах с постоянным числом частиц
- •1.6.2. Распределения Гиббса.
- •1.6.3. Квазиклассическое приближение.
- •1.7. Свойства распределения Гиббса
- •1.8. Большое каноническое распределение Гиббса
- •2. Статистика идеального газа
- •2.1. Идеальный газ как модель статистической системы
- •2.2. Распределение Максвелла
- •2.3. Столкновения молекул со стенкой сосуда. Давление
- •2.4. Характерные величины идеального газа
- •2.5. Столкновение молекул между собой
- •2.6. Длина свободного пробега
- •2.7. Идеальный газ во внешнем поле
- •2.8. Число и функция состояний идеального газа
- •2.9. Классическая теория теплоемкости газа двухатомных молекул
- •2.10. Квантовая теория теплоемкости газа двухатомных молекул
- •2.11. Распределения в квантовых системах
- •3. Законы термодинамики
- •3.1. Статистическое обоснование первого начала термодинамики
- •3.2. Второе начало термодинамики
- •3.3. Вечный двигатель второго рода. Максимальная работа процессов
- •3.4. Полезная работа тепловых машин
- •3.5. Метод термодинамических потенциалов
- •3.6. Термодинамические коэффициенты. Критерии устойчивости равновесия
- •3.7. Статистическое вычисление термодинамических величин
- •3.8. Третье начало термодинамики (теорема Нернста)
- •3.9. Применения термодинамики
- •4. Статистика сложных систем.
- •4.1. Модель кристаллического твердого тела. Уравнение движения атомов
- •4.2. Дисперсионное уравнение нормальных колебаний кристалла
- •4.3. Кристалл как система линейных гармонических осцилляторов
- •4.4. Статистическая сумма и энергия кристалла (в гармоническом приближении)
- •4.5. Теория теплоемкости Дебая
- •4.6. Электронный газ в металлах
- •4.7. Зависимость энергии электрона от волнового вектора. Эффективная масса
- •4.8. Теория парамагнетизма. Природа и характеристики магнетизма.
- •4.9. Равновесное излучение.
- •4.10. Системы с кулоновским взаимодействием частиц.
- •5. Теория малых флуктуаций
- •5.1. Определение и значение флуктуаций
- •5.2. Мера вероятности и масштаб флуктуаций
- •5.3. Флуктуации термодинамических величин в однородной среде
- •5.4. Предельная чувствительность измерительных приборов
- •5.5. Рассеяния света флуктуациями
- •6. Элементы теории физической кинетики
- •6.1. Определения и характеристики необратимых процессов
- •6.2. Теория стационарных процессов в газе свободных электронов
- •6.3. Газокинетическое уравнение Больцмана
- •6.4. Приближение времени релаксации
- •Раздел 2
- •Раздел 2
- •Раздел 3
- •Раздел 4
- •Раздел 5
- •Раздел 6
- •Список Литературы
4. Статистика сложных систем.
4.1. Модель кристаллического твердого тела. Уравнение движения атомов
Твердыми называются тела, отличающиеся постоянством формы и объема. Они делятся на кристаллические и аморфные. Последние характеризуются хаотическим распределением атомов (молекул). В кристаллах атомы (молекулы) расположены регулярно, что приводит к пространственной периодичности их свойств.
Основное энергетическое состояние твердого тела – это регулярное распределение атомов (кристалл), поэтому с термодинамической точки зрения аморфное тело всегда находится в некотором неравновесном (метастабильном) состоянии. В обычных условиях оно может поддерживаться сколь угодно долго.
Тепловые свойства твердых тел определяются главным образом характером движения микрочастиц (атомов, молекул, ионов). Движение электронов и ядер можно рассматривать независимо. Это обусловлено большим различием их масс, скоростей движения; по отношению к электронам ядра практически недвижимы (адиабатическое приближение).
Согласно современной
теории кристаллов, структурные единицы
(атомы или молекулы) находятся в узлах
кристаллической решетки. Основу ее
симметрии составляет пространственная
периодичность – свойство решетки
совмещаться сама с собой при параллельных
переносах (трансляциях), поворотах и
отражениях. Различают ортогональную,
гексагональную, гранецентрированную
и производные от них структуры решеток.
Рентгенографические измерения показали,
что расстояния между атомами в кристаллах
весьма малы, они того же порядка
(10 – 8 см), что и расстояния
между атомами в молекулах. Расстояние
между молекулами в кристаллах (построенных
из молекул) всего в два-три раза больше
внутримолекулярных расстояний.
Силы, связывающие между собой атомы или
молекулы, почти полностью имеют
электростатическую природу. Роль
магнитных взаимодействий весьма
незначительна. Действительно, энергия
электростатического взаимодействия
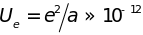 эрг
(
эрг
(![]() – заряд электрона,
– межатомное
расстояние), а магнитного –
– заряд электрона,
– межатомное
расстояние), а магнитного –
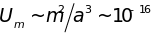 эрг
(наибольший магнитный момент
эрг
(наибольший магнитный момент
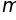 того же порядка,
что и электронный, и приближенно равен
того же порядка,
что и электронный, и приближенно равен
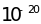 эрг/гс).
эрг/гс).
В силу близкого
расположения структурных единиц
кристалла энергия взаимодействия между
ними чрезвычайно велика, намного больше
энергии теплового движения
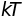 .
По порядку величины она соответствует
взаимодействию между атомами в молекуле.
Поэтому кристалл можно рассматривать
как одну гигантскую молекулу с огромным
числом связанных атомов, как обратный
предельный случай молекулярного газа
(в газах энергия взаимодействия между
частицами намного меньше
).
При такой ситуации единственно возможным
видом движения связанных частиц в
кристалле – их колебание около положений
равновесия. Предполагается, что амплитуда
колебаний весьма мала по сравнению с
расстояниями между атомами. В этом
случае потенциальная энергия колебаний
является квадратичной функцией смещения
и, согласно классической статистике,
на каждую степень свободы колебательного
движения приходится средняя энергия
.
По порядку величины она соответствует
взаимодействию между атомами в молекуле.
Поэтому кристалл можно рассматривать
как одну гигантскую молекулу с огромным
числом связанных атомов, как обратный
предельный случай молекулярного газа
(в газах энергия взаимодействия между
частицами намного меньше
).
При такой ситуации единственно возможным
видом движения связанных частиц в
кристалле – их колебание около положений
равновесия. Предполагается, что амплитуда
колебаний весьма мала по сравнению с
расстояниями между атомами. В этом
случае потенциальная энергия колебаний
является квадратичной функцией смещения
и, согласно классической статистике,
на каждую степень свободы колебательного
движения приходится средняя энергия
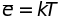 .
Поскольку число колебательных степеней
свободы у кристалла, содержащего
.
Поскольку число колебательных степеней
свободы у кристалла, содержащего
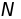 атомов, равно
атомов, равно
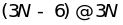 ,
то внутренняя энергия кристалла и его
молярная теплоемкость равны
,
то внутренняя энергия кристалла и его
молярная теплоемкость равны
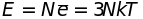 ,
,
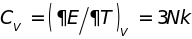 .
.
Последняя не зависит от температуры и индивидуальных свойств кристалла. Впервые такую особенность твердых тел выявили экспериментально П. Дюлонг и А. Пти (1819 г.). Закон Дюлонга и Пти точно описывает теплоемкость многих атомных кристаллов при высоких температурах. Нарушение этого закона имеет место при низких температурах, когда становится неприемлем классический подход, используемый при выводе указанных выше формул.
Характер
колебаний отдельного атома кристалла
оказывается весьма сложным, и точное
его описание представляет серьезные
трудности. Один из приближенных методов
заключается в том, что вместо индивидуальных
колебаний частиц рассматривают их
коллективное движение в пространственно
упорядоченной системе. Такой подход
оправдывается мощными силами связи:
колебания одной частицы немедленно
передается соседям, и в кристалле
возбуждается коллективное движение в
форме упругой волны, охватывающей все
частицы. Наглядное представление о
характере теплового движения атомов в
кристалле дает его одномерная (фиктивная)
модель, а именно: цепочка из
атомов, расположенных вдоль линии на
равных расстояниях
![]() друг от друга. Пронумеруем атомы в
цепочке от
друг от друга. Пронумеруем атомы в
цепочке от
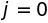 до
до
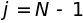 .
При смещении
-го
атома из положения равновесия
.
При смещении
-го
атома из положения равновесия
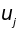 (вправо или влево) он будет испытывать
силу отталкивания со стороны соседа, к
которому приблизился, и притяжение со
стороны другого соседа. Действие этих
сил приведет к смещению
(вправо или влево) он будет испытывать
силу отталкивания со стороны соседа, к
которому приблизился, и притяжение со
стороны другого соседа. Действие этих
сил приведет к смещению
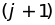 -го
атома вправо на расстояние
-го
атома вправо на расстояние
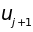 ,
а
,
а
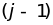 -го
атома на расстояние
-го
атома на расстояние
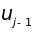 .
Эти атомы будут действовать на следующих
соседей:
.
Эти атомы будут действовать на следующих
соседей:
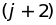 ,
,
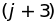 ,…,
,…,
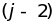 ,
,
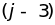 ,
…, и в результате вся цепочка атомов
придет в движение. Силы, действующие на
-ый
атом со стороны
,
…, и в результате вся цепочка атомов
придет в движение. Силы, действующие на
-ый
атом со стороны
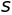 -го
атома, пропорциональны их относительному
смещению
-го
атома, пропорциональны их относительному
смещению
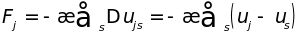 .
Поскольку силы межмолекулярного
взаимодействия быстро убывают с
расстоянием, то можно учитывать только
взаимодействия с ближайшими соседями.
В этом приближении уравнение движения
произвольного
-го
атома (
.
Поскольку силы межмолекулярного
взаимодействия быстро убывают с
расстоянием, то можно учитывать только
взаимодействия с ближайшими соседями.
В этом приближении уравнение движения
произвольного
-го
атома (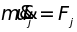 )
принимает вид
)
принимает вид
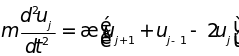 . (4.1)
. (4.1)
В качестве граничных
условий будем считать, что крайние атомы
(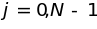 )
неподвижны:
)
неподвижны:
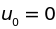 ,
,
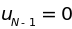 .
.
Для такого предположения нет оснований, но оно оправданно в виду статистического характера системы с большим числом частиц, при котором ее свойства в равновесном состоянии не зависят от начальных и граничных условий.
